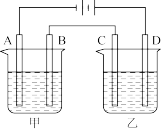
某课外活动小组用如图所示装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则A极的电极反应式为___________ 。
(2)若开始时开关K与b极连接,则B极的电极反应式为___________ 。
(3)若开始时开关K与b连接,下列说法正确的是___________(填字母)。
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
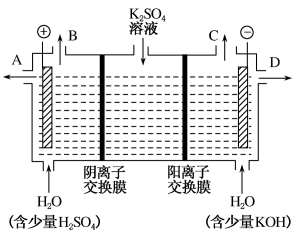
①该电解槽的阳极反应式为___________ 。
②右侧电极发生的是___________ 反应(填“氧化”或“还原”);从A出口流出的物质是___________ 从D出口流出的物质是___________ 。

(1)若开始时开关K与a连接,则A极的电极反应式为
(2)若开始时开关K与b极连接,则B极的电极反应式为
(3)若开始时开关K与b连接,下列说法正确的是___________(填字母)。
| A.溶液中Na+向A极移动 |
| B.从A极处逸出的气体能使湿润的KI-淀粉试纸变蓝 |
| C.反应一段时间后加适量盐酸可恢复到电解前电解质溶液的浓度 |
| D.若标准状况下B极产生2.24L气体,则溶液中转移0.2mol电子 |

①该电解槽的阳极反应式为
②右侧电极发生的是
更新时间:2021-10-19 01:11:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】我国首创以铝─空气─海水电池为能源的新型海水标志灯。该灯以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流。只要把灯放入海水中数分钟,就会发出耀眼的白光,其能量比干电池高20─50倍(海水呈弱碱性),请回答:该电源负极材料是_____ ,正极主要的反应物质是_____ ,总反应方程为:____________________
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据原电池原理和设计思路,将反应Fe+CuSO4=FeSO4+Cu设计成原电池,画出装置图,并写出正负极反应式。负极反应:_______ ;正极反应:______ 装置图_______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图。据此回答下列问题:
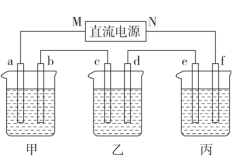
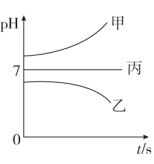
(1)M为电源的__________ 极(填“正”或“负”)。
(2)写出甲烧杯中反应的化学方程式____________________ 。
(3)有人设想用图一所示原电池为直流电源完成上述电解。则锌电极相当于直流电源的_________ (填“M”或“N”)极。

(4)有人设想用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化为重要化工原料。该设想中负极的电极反应式为__________________ 。
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图。据此回答下列问题:


(1)M为电源的
(2)写出甲烧杯中反应的化学方程式
(3)有人设想用图一所示原电池为直流电源完成上述电解。则锌电极相当于直流电源的

(4)有人设想用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化为重要化工原料。该设想中负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,A、B、C、D均为石墨电极,E、F分别为短周期相邻两种活泼金属元素的单质,且E能与NaOH溶液反应。按图示接通电路,反应一段时间。
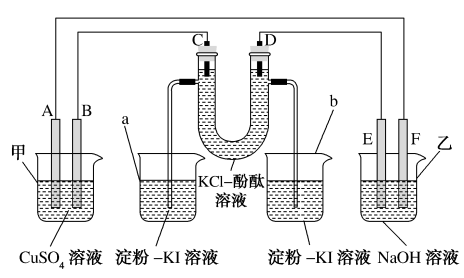
(1)甲池是_______ (填“原电池”或“电解池”)装置,电极A的名称是_______ 。
(2)C极为_______ (填“阴极”或“阳极”),电极反应式为_______ 。
(3)烧杯中溶液会变蓝的是_______ (填“a”或“b”)。
(4)甲池中总反应的离子方程式为_______ 。
(5)乙池中总反应的化学方程式为_______ 。

(1)甲池是
(2)C极为
(3)烧杯中溶液会变蓝的是
(4)甲池中总反应的离子方程式为
(5)乙池中总反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为离子交换膜。请按要求回答相关问题:
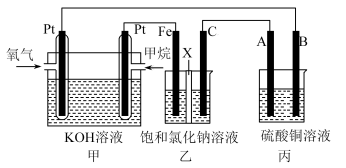
(1)甲烷燃料电池负极反应式是___________ 。
(2)Fe电极的电极反应式为___________ 。
(3)X选择___________ 离子交换膜(填“阴”,“阳”)。
(4)丙模拟粗铜的精炼,那么粗铜放在___________ (填“A”,“B”)极,反应结束后硫酸铜溶液的浓度___________ (填“变大”,“变小”,“不变”)。
(5)若在标准状况下,有11.2 L氧气参加反应,则乙装置中铁极上生成的气体体积为___________ L。
(6)写出图中电解饱和食盐水的总的化学反应方程式___________ 。

(1)甲烷燃料电池负极反应式是
(2)Fe电极的电极反应式为
(3)X选择
(4)丙模拟粗铜的精炼,那么粗铜放在
(5)若在标准状况下,有11.2 L氧气参加反应,则乙装置中铁极上生成的气体体积为
(6)写出图中电解饱和食盐水的总的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,某同学设计一个燃料电池并探究氯碱工业原理和电解CuSO4溶液,其中乙装置中X为阳离子交换膜。

根据要求回答相关问题:
(1)通入氧气的电极为___ (填“正极”或“负极”),负极的电极反应式为___ 。
(2)铁电极为___ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为___ 。
(3)乙装置中电解的总反应的离子方程式为___ 。
(4)若在标准状况下,有1.12L氧气参加反应,丙装置中阴极增重的质量为___ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)乙装置中电解的总反应的离子方程式为
(4)若在标准状况下,有1.12L氧气参加反应,丙装置中阴极增重的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮及其化合物在工农业生产和生命活动中起着重要的作用。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一 个十年行动纲领。氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的价电子轨道表示式___________ ;基态铬、氮原子的未成对电子数之比为___________ 。
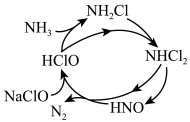
(2)NH3也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图所示(其中H2O和NaCl 略去)。NaClO 氧化NH3的总反应化学程式为___________ 。
(3)改变 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的
对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的 值约为
值约为___________ 。

(4)室温下,用水稀释0.1mol·L-1氨水,溶液中随着水量的增加而减小的是___________。
(5)25°C时,将amol NH4NO3溶于水,向该溶液中滴加bL氨水后溶液呈中性,滴加氨水的过程中水的电离平衡将___________ (填 “正向”、“逆向”或“不”)移动。
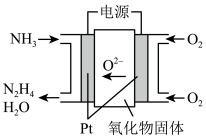
(6)工业上利用NH3制备联氨(N2H4)装置如下图,其阳极电极反应式为___________ 。
(1)“中国制造2025”是中国政府实施制造强国战略第一 个十年行动纲领。氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的价电子轨道表示式
(2)NH3也是造成水体富营养化的重要原因之一,用NaClO溶液氧化可除去氨气。其反应机理如图所示(其中H2O和NaCl 略去)。NaClO 氧化NH3的总反应化学程式为

(3)改变
 对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的
对溶液中NaClO去除氨气效果与余氯(溶液中+1价氯元素的含量)的影响如图所示,则除氨气过程中最佳的 值约为
值约为
(4)室温下,用水稀释0.1mol·L-1氨水,溶液中随着水量的增加而减小的是___________。
A.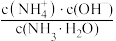 ) ) | B.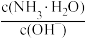 |
| C.c(H+) | D.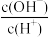 |
(6)工业上利用NH3制备联氨(N2H4)装置如下图,其阳极电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.一种利用电化学原理治污的装置如下图,其反应原理是6NO2+8NH3=7N2+12H2O
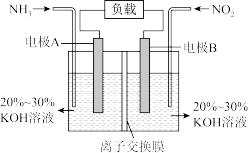
(1)A电极的电极反应式为___________ 。
(2)下列关于该电池说法正确的是___________(填序号)。
II.全钒液流电池(VFB)是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图为VFB放电工作原理。
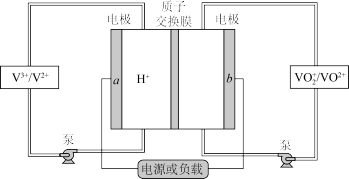
(3)电极b为___________ 极(填“正”或“负”)。充电时,该电极的反应为___________ 。
(4)若负载为如图2所示的装置,A、B、C、D均为石墨电极。
①甲槽是电极电解饱和食盐水的装置,产生40 g NaOH时,VFB电池中消耗___________ mol H+。
②乙槽为200 mLCuSO4溶液,当C电极析出0.64 g物质时,则乙槽中生成的H2SO4的物质的量为___________ mol。
③若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为___________ (用NA表示)
(5)锂离子电池的一种工作方式为Li+在电池两极的嵌入或迁出,以石墨做正极时,充电过程中,Li+在该石墨电极上___________ (填“嵌入”或“迁出”)。

(1)A电极的电极反应式为
(2)下列关于该电池说法正确的是___________(填序号)。
| A.电子从右侧电极经过负载后流向左侧电极 |
| B.为使电池持续放电,离子交换膜需选用阴离子交换膜 |
| C.电池工作一段时间,溶液的pH不变 |
| D.当有44.8 LNO2被处理时,转移电子的物质的量为8 mol |
II.全钒液流电池(VFB)是目前最成熟的液流电池技术。它通过钒离子价态的相互转化实现能量的存储和释放。下图为VFB放电工作原理。

(3)电极b为
(4)若负载为如图2所示的装置,A、B、C、D均为石墨电极。

①甲槽是电极电解饱和食盐水的装置,产生40 g NaOH时,VFB电池中消耗
②乙槽为200 mLCuSO4溶液,当C电极析出0.64 g物质时,则乙槽中生成的H2SO4的物质的量为
③若通电一段时间后,向所得的乙槽溶液中加入0.2 mol的Cu(OH)2才能恰好恢复到电解前的浓度,则电解过程中转移的电子数为
(5)锂离子电池的一种工作方式为Li+在电池两极的嵌入或迁出,以石墨做正极时,充电过程中,Li+在该石墨电极上
您最近一年使用:0次




