下列关于实验现象的描述不正确的是
| A.海水为电解质溶液,铁、铜做电极,铁腐蚀的速率为:铁做阳极>铁做负极 |
| B.在钢铁制品中加入一些铬或镍制成合金,可有效防止金属腐蚀 |
| C.铅蓄电池放电时负极质量减轻,充电时阳极质量增加 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
更新时间:2021-10-19 12:33:25
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】关于原电池和电解池的叙述正确的是
| A.原电池中失去电子的电极为阴极 |
| B.原电池的负极、电解池的阳极都发生氧化反应 |
| C.原电池的两极一定是由活动性不同的两种金属组成 |
| D.电解时电解池的阴极一定是阴离子放电 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某原电池反应的离子方程式为:Zn+2H+=Zn2++H2↑,关于此原电池下列说法正确的是
| A.HNO3可作电解质溶液 | B.在电解质溶液中电子从正极流向负极 |
| C.锌极质量不变 | D.该原电池的正极材料可以为铁 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列有关材料的说法错误的是
| A.铁制品在潮湿空气中更易锈蚀 |
| B.二氧化硅常用于制造光导纤维 |
| C.实验室中经过滤可得到纳米碳酸钙固体 |
| D.聚乙烯可作食品包装材料 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是
| A.镀锡的铁片镀层破损后,腐蚀速率加快 |
| B.Fe在食盐水中被腐蚀,其负极反应为O2 +2H2O + 4e-=4OH- |
| C.可用被保护金属与直流电源负极相接的方法来减慢腐蚀速率 |
| D.电解法精炼铜时,阳极材料应用粗铜 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下图装置中电流计指针偏转,且M棒变细,N棒变粗。由此判断表中所列M、N、P物质,与实验现象相符的是( )
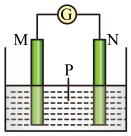

| M | N | P | |
| A | Al | Mg | NaOH溶液 |
| B | Fe | Ag | AgNO3溶液 |
| C | Zn | Cu | H2SO4溶液 |
| D | Fe | Cu | 浓硝酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】把a,b,c三块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;b、c相连时,c不易被腐蚀。则三种金属的活动性由强到弱的顺序为
| A.a>b>c | B.a>c>b | C.c>b>a | D.b>c>a |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】铁—铬液流电池是近年新投产、较好利用储(放)能技术的新型电池。该电池总反应为 。下列有关说法错误的是
。下列有关说法错误的是
 。下列有关说法错误的是
。下列有关说法错误的是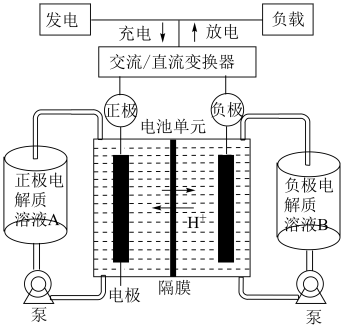
| A.放电时正极电解质溶液酸性增强 |
B.储能时原正极上的电极反应为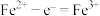 |
C.负极区电解质溶液中存在 与 与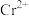 的相互转化 的相互转化 |
D.在相同条件下,离子的氧化性: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2,下列说法中不正确的是
| A.原电池放电时,负极上发生反应的物质是Zn |
| B.负极发生的反应是Zn+2OH--2e-=Zn(OH)2 |
| C.工作时,负极区溶液碱性减弱,正极区溶液碱性增强 |
| D.溶液中OH-向正极移动,K+、H+向负极移动 |
您最近一年使用:0次

 ,并利用实验室材料制备原电池.下列关于该原电池的组成及现象描述正确的是(
,并利用实验室材料制备原电池.下列关于该原电池的组成及现象描述正确的是( 溶液
溶液 溶液
溶液 溶液
溶液

