研究NOx、CO等大气污染物的测量及处理具有重要意义。
(1)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被CO还原成N2排除。写出NO被CO还原的化学方程式:___________ 。
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
已知:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H=-905.5kJ•mol-1 N2(g)+O2(g)
4NO(g)+6H2O(g)△H=-905.5kJ•mol-1 N2(g)+O2(g) 2NO(g)△H=+180kJ•mol-1
2NO(g)△H=+180kJ•mol-1
完成该方法中主要反应的热化学方程式4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H
4N2(g)+6H2O(g) △H___________ 。
(3)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是___________ 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式:___________ 。
(1)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被CO还原成N2排除。写出NO被CO还原的化学方程式:
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
已知:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)△H=-905.5kJ•mol-1 N2(g)+O2(g)
4NO(g)+6H2O(g)△H=-905.5kJ•mol-1 N2(g)+O2(g) 2NO(g)△H=+180kJ•mol-1
2NO(g)△H=+180kJ•mol-1完成该方法中主要反应的热化学方程式4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H
4N2(g)+6H2O(g) △H(3)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是
②写出NiO电极的电极反应式:
更新时间:2021-10-22 11:56:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】2022年6月5日10时44分,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭在酒泉卫星发射中心点火发射,成功将飞船运送到预定轨道。肼(N2H4)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。_______ ;消耗16g液态肼放出的热量为_______ 。
(2)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-544kJ/mol,用如下图示表示该反应时:_______ (填“I”或“II”)处物质,(b-a)kJ/mol表示该反应的_______ 。使用合适的催化剂,_______ (填“能"或“不能")改变该反应的焓变。
(3)已知:N2(g)+2O2(g)=2NO2(g) ΔH=+68kJ·mol-1,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为_______ 。
(4)火箭如果用压缩NO2作氧化剂,发射时尾部有大量的红棕色气体产生,此颜色比压缩NO2颜色更深,原因是_______ (用化学方程式表示)。


(2)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-544kJ/mol,用如下图示表示该反应时:
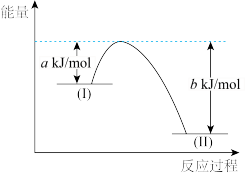
(3)已知:N2(g)+2O2(g)=2NO2(g) ΔH=+68kJ·mol-1,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
(4)火箭如果用压缩NO2作氧化剂,发射时尾部有大量的红棕色气体产生,此颜色比压缩NO2颜色更深,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①2CH3OH(1)+ 3O2(g)= 2CO2(g)+ 4H2O(g)ΔH1 = –1275.6 kJ·mol– 1
②2CO(g)+ O2(g)= 2CO2(g) ΔH2 = –566.0 kJ·mol– 1
③H2O(g)= H2O(1) ΔH3 = –44.0 kJ·mol– 1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___________________ 。
(2)生产甲醇的原料CO和H2来源于:CH4(g)+ H2O(g) CO(g)+ 3H2(g)
CO(g)+ 3H2(g)
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则,Pl_______ P2;A、B、C三点处对应平衡常数(KA、KB、KC)的由大到小的顺序为__________ 。(填“<”、“>”“=”)
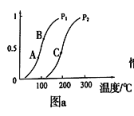
②100℃时,将1 mol CH4和2 mol H2O通入容积为100 L的反应室,如果5min达到平衡时CH4的转化率为0.5,则v(H2)=________________ 100℃时该反应的平衡常数K =_________ 。反应达到平衡的标志是:_____________ 。
A.容器内气体密度恒定
B.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
C.容器的压强恒定
D.3v正(CH4)= v逆(H2)
③为了加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有________ (填编号)。
A.升高温度 B.缩小容器体积 C.再充入CH4气体 D.使用合适的催化剂
(1)已知:①2CH3OH(1)+ 3O2(g)= 2CO2(g)+ 4H2O(g)ΔH1 = –1275.6 kJ·mol– 1
②2CO(g)+ O2(g)= 2CO2(g) ΔH2 = –566.0 kJ·mol– 1
③H2O(g)= H2O(1) ΔH3 = –44.0 kJ·mol– 1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)生产甲醇的原料CO和H2来源于:CH4(g)+ H2O(g)
 CO(g)+ 3H2(g)
CO(g)+ 3H2(g)①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则,Pl

②100℃时,将1 mol CH4和2 mol H2O通入容积为100 L的反应室,如果5min达到平衡时CH4的转化率为0.5,则v(H2)=
A.容器内气体密度恒定
B.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
C.容器的压强恒定
D.3v正(CH4)= v逆(H2)
③为了加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有
A.升高温度 B.缩小容器体积 C.再充入CH4气体 D.使用合适的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】肼(N2H4),又称联氨,主要用作火箭和喷气发动机的燃料部分。
(1)已知:N2H4(g)+H2(g) =2NH3(g) △H=-41.8 KJ•mol-1
N2(g)+3H2(g) 2NH3(g) △H=-92 KJ•mol-1
2NH3(g) △H=-92 KJ•mol-1
2H2(g)+O2(g) =2H2O(g) △H=-483.6 KJ•mol-1
请写出肼与氧气反应生成氮气和水蒸气的热化学方程式______________________________ ;
(2)同时,肼也可作为新型燃料电池的燃料。请利用肼、氧气与氢氧化钾溶液组成碱性燃料电池,写出该电池负极的电极反应式__________________________ ,当电路中转移0.6mol电子时,正极消耗的氧气体积为___________ L(标准状况下)。
(1)已知:N2H4(g)+H2(g) =2NH3(g) △H=-41.8 KJ•mol-1
N2(g)+3H2(g)
 2NH3(g) △H=-92 KJ•mol-1
2NH3(g) △H=-92 KJ•mol-12H2(g)+O2(g) =2H2O(g) △H=-483.6 KJ•mol-1
请写出肼与氧气反应生成氮气和水蒸气的热化学方程式
(2)同时,肼也可作为新型燃料电池的燃料。请利用肼、氧气与氢氧化钾溶液组成碱性燃料电池,写出该电池负极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】从H+、Cu2+、Na+、SO42-、Cl-五种离子中恰当地组成电解质,按下列要求进行电解:
(1)以石墨为电极进行电解,使电解质质量减少,水质量不变,可采用的电解质有__________
(2)以石墨为电极进行电解,使电解质质量不变,水质量减少,可采用的电解质有_________
(3)以石墨为电极进行电解,使电解质和水的质量都减少,可采用的电解质有__________
(1)以石墨为电极进行电解,使电解质质量减少,水质量不变,可采用的电解质有
(2)以石墨为电极进行电解,使电解质质量不变,水质量减少,可采用的电解质有
(3)以石墨为电极进行电解,使电解质和水的质量都减少,可采用的电解质有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题:
(1)高铁酸钾( )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图所示是高铁电池的模拟实验装置。
)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图所示是高铁电池的模拟实验装置。

①该电池放电时正极产生 沉淀,正极电极反应为
沉淀,正极电极反应为___________ 。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向___________ (填“左”或“右”)移动;
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________ 。

(2)氯碱工业电解饱和食盐水制烧碱时必须阻止 移向阳极,目前采用阳离子交换膜将两极溶液分开(如图)。
移向阳极,目前采用阳离子交换膜将两极溶液分开(如图)。

①C、D分别是直流电源的两电极,C是电源___________ 极。
②电解一段时间后,A口导出___________ 。
③阳离子交换膜的作用是___________ 。
(1)高铁酸钾(
 )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图所示是高铁电池的模拟实验装置。
)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图所示是高铁电池的模拟实验装置。
①该电池放电时正极产生
 沉淀,正极电极反应为
沉淀,正极电极反应为②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

(2)氯碱工业电解饱和食盐水制烧碱时必须阻止
 移向阳极,目前采用阳离子交换膜将两极溶液分开(如图)。
移向阳极,目前采用阳离子交换膜将两极溶液分开(如图)。
①C、D分别是直流电源的两电极,C是电源
②电解一段时间后,A口导出
③阳离子交换膜的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲烷是一种重要的化工原料,广泛应用于民用和工业中。电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段,其装置如图所示。

①电解池工作过程中,图中Pt电极附近溶液的pH__ (填“变大”或“变小”)。
②该电解池的阴极电极反应式为__ 。

①电解池工作过程中,图中Pt电极附近溶液的pH
②该电解池的阴极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):

(1)电解质溶液为稀硫酸时,灯泡______ (填“亮”或“不亮”,填“亮”做 a 题,填“不亮”做 b题)。
a.若灯泡亮, Al 电极上发生的反应为______ 。
b.若灯泡不亮, 其理由为______。
(2)电解质溶液为 NaOH 溶液时,灯泡______ (填“亮”或“不亮”,填“亮”做 a 题,填“不亮”做 b 题)。
a.若灯泡亮, Al 电极上发生的反应为______ 。
b.若灯泡不亮, 其理由为______。
Ⅱ. CH4 既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷的电子式为______ 。
(2)以 CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理下图所示,则通入 a 气体的电极名称为______ , 通入 b 气体的电极反应式______ 。(质子交换膜只允许 H+通过)


(1)电解质溶液为稀硫酸时,灯泡
a.若灯泡亮, Al 电极上发生的反应为
b.若灯泡不亮, 其理由为______。
(2)电解质溶液为 NaOH 溶液时,灯泡
a.若灯泡亮, Al 电极上发生的反应为
b.若灯泡不亮, 其理由为______。
Ⅱ. CH4 既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷的电子式为
(2)以 CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理下图所示,则通入 a 气体的电极名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:
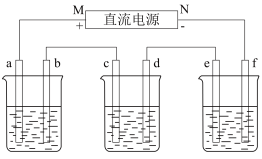
(1)b极上的电极反应式为__ ,甲电池的总反应化学方程式是__ 。
(2)在粗铜的电解过程中,图中c电极的材料是__ (填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为__ ;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是__ ,电解一段时间后,电解液中的金属离子有__ 。
(3)如果要在铁制品上镀镍(二价金属),则e电极的材料是__ (填“铁制品”或“镍块”,下同),f电极的材料是__ 。
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为__ 。

甲 乙 丙
(1)b极上的电极反应式为
(2)在粗铜的电解过程中,图中c电极的材料是
(3)如果要在铁制品上镀镍(二价金属),则e电极的材料是
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为
您最近一年使用:0次




