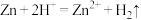NO2是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2进行回收利用,装置中a、b均为多孔石墨电极。下列说法错误的是
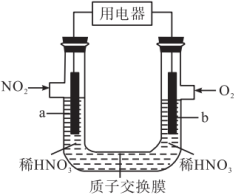

| A.a为电池的负极,发生氧化反应 |
| B.电子流向a电极→用电器→b电极→溶液→a电极 |
| C.一段时间后,a极附近HNO3浓度增大 |
| D.电池总反应为4NO2+O2+2H2O=4HNO3 |
21-22高二上·安徽·阶段练习 查看更多[2]
更新时间:2021-11-01 15:55:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】液流电池因其具有可深度充放电、可模块化调控、不受地理环境限制等优点,已成为大规模储能领域中备受重视的储能器件。其中锌/溴液流电池作为新能源储能技术的代表,功率性能极佳且造价低廉。三单体串联锌/溴液流电池工作原理如图所示:
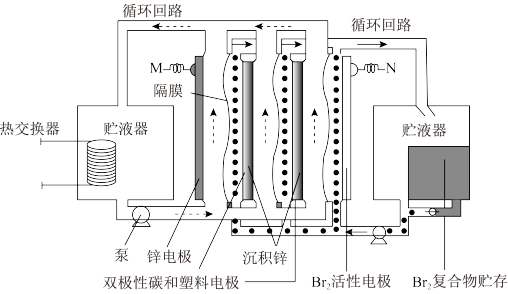
下列说法正确的是

下列说法正确的是
| A.放电时,N极为负极 |
B.放电时,左侧贮液器中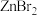 的浓度不断减小 的浓度不断减小 |
| C.隔膜允许阳离子通过,也允许阴离子通过 |
D.充电时,M极的电极反应式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于实验现象的描述不正确的是
| A.原电池放电时,电流的方向是从正极到负极 |
| B.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| C.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某同学按如图所示的装置做实验,并把实验情况记录于下面,其中叙述合理的是
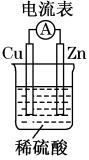
①锌为正极,铜为负极 ②电解质溶液中H+浓度不变 ③电流表的指针发生偏转 ④铜极上有气泡产生 ⑤锌极上有大量气泡产生 ⑥溶液中的阳离子向正极移动

①锌为正极,铜为负极 ②电解质溶液中H+浓度不变 ③电流表的指针发生偏转 ④铜极上有气泡产生 ⑤锌极上有大量气泡产生 ⑥溶液中的阳离子向正极移动
| A.①②③ | B.③④⑤ | C.③④⑥ | D.②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.通过构成原电池将反应的化学能全部转化为电能 |
B.钢铁在潮湿的环境中易腐蚀,是因为钢铁里的铁和少量的碳与表面的水膜形成了无数微小原电池,其中负极发生的反应为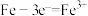 |
| C.在电解池中电子由阳极流向外接电源的正极,从外接电源的负极流向阴极 |
D.电解精炼铜时,若阳极质量减少64g,则转移到阴极的电子等于2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
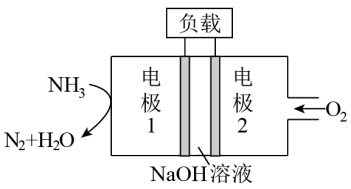
【推荐1】某一环保电池可以消除污染,并产生参与大气循环的物质,装置如图所示。下列说法不正确的是
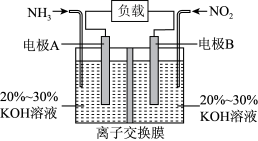

| A.电极A极反应式为2NH3-6e-=N2+6H+ |
| B.为使电池持续放电,离子交换膜需选用阴离子交换膜 |
| C.当有4.48LNO2(标准状况)被处理时,转移电子为0.8mol |
| D.该电池既能实现有效消除氮氧化物的排放,又能充分利用化学能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某原电池装置如图所示。下列有关叙述中,正确的是
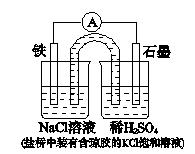

| A.Fe作正极,发生氧化反应 |
| B.负极反应: 2H+ + 2e-=H2↑ |
| C.工作一段时间后,两烧杯中溶液pH均不变 |
| D.工作一段时间后,NaCl溶液中c(Cl-)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
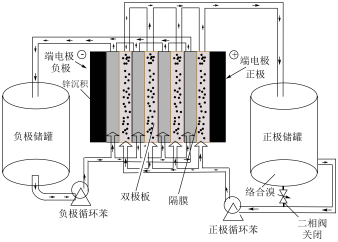
【推荐1】中科院大连化物所储能技术研究部将锌溴液流电池电堆面容量提高至140mAh/cm2,从而大幅度提高了电池能量密度。其原理如图所示(已知:络合溴为Br 、Br
、Br 等),下列说法正确的是
等),下列说法正确的是
 、Br
、Br 等),下列说法正确的是
等),下列说法正确的是
A. 端电极电势比 端电极电势比 端电极电势低 端电极电势低 |
B.放电时,负极电极反应为 |
| C.充电时,负极材料每增重65g,正极发生还原反应产生160g Br2 |
| D.放电时,电极表面之间的微孔隔膜阻止了络合溴向锌沉积物的扩散,减少了电池的自放电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】中国科学院福建物质结构研究所基于二氧化碳和甲酸的相互转化反应设计并实现了一种可逆的水系金属二氧化碳电池,结构如图所示。下列说法错误的是
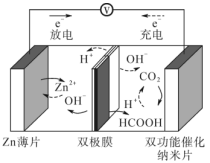

| A.双极膜、双功能催化纳米片等材料是保证电池功能的重要条件 |
| B.放电时,H+移向正极,正极区溶液酸性不变 |
C.充电时,阳极反应式为 |
| D.若用该电池电解饱和食盐水,理论上消耗CO2的物质的量与产生Cl2的物质的量相同 |
您最近一年使用:0次

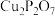 催化剂可以用于建构
催化剂可以用于建构 二次电池,装置如图所示。双极膜中水电离的
二次电池,装置如图所示。双极膜中水电离的 和
和 在电场作用下可以向两极迁移。下列说法正确的是
在电场作用下可以向两极迁移。下列说法正确的是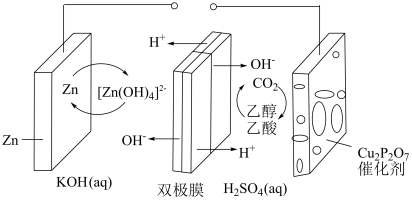
 流向
流向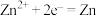
 的物质的量之比为5∶2
的物质的量之比为5∶2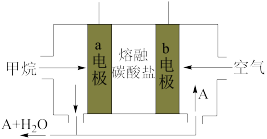

 移向b电极
移向b电极 电子,则该电池消耗
电子,则该电池消耗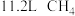
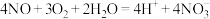
 溶液中通入
溶液中通入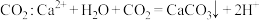
 溶液与足量
溶液与足量 溶液混合:
溶液混合: