从元素化合价升降的角度认识氧化还原反应
对于反应Fe+CuSO4=FeSO4+Cu,铜元素化合价___________ ,CuSO4发生___________ 反应,被还原;铁元素化合价___________ ,Fe发生___________ 反应,被氧化。
结论:凡是有元素化合价升降的化学反应都是氧化还原反应。氧化还原反应的重要特征是反应前后有元素的___________ 。
对于反应Fe+CuSO4=FeSO4+Cu,铜元素化合价
结论:凡是有元素化合价升降的化学反应都是氧化还原反应。氧化还原反应的重要特征是反应前后有元素的
21-22高一上·全国·课前预习 查看更多[2]
更新时间:2021-11-29 12:37:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】NaOH是重要的化工原料,研究其制备、贮存检验及应用具有重要意义。
(1)已知:I.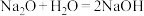 ,II.
,II.  。
。
①上述反应中属于氧化还原反应的是_______ (填编号)。
②用双线桥表示上述氧化还原反应:_______ 。
③指出其中的氧化剂是_______ ,氧化产物是_______ 。
(2)向饱和Na2CO3中通入足量CO2的化学方程式:_______ 。
(3)NaOH在保存过程中易变质生成Na2CO3,请写出发生变质的化学方程式:_______ 。
(4)若一定质量的NaOH在变质前后分别与足量的稀硝酸反应,则消耗HNO3的质量_______ (填“变质前多”“变质后多”或“一样多”)。
(1)已知:I.
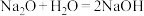 ,II.
,II.  。
。①上述反应中属于氧化还原反应的是
②用双线桥表示上述氧化还原反应:
③指出其中的氧化剂是
(2)向饱和Na2CO3中通入足量CO2的化学方程式:
(3)NaOH在保存过程中易变质生成Na2CO3,请写出发生变质的化学方程式:
(4)若一定质量的NaOH在变质前后分别与足量的稀硝酸反应,则消耗HNO3的质量
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】化学与日常生活、医药、环保等密不可分。
(1)医药行业的毒胶囊事件曾被央视《每周质量报告》曝光。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
①胶体中的分散质直径范围是___________ nm。
②元素铬(Cr)的几种化合物存在转化关系: 固体
固体 溶液(绿色)
溶液(绿色) 溶液(黄色)
溶液(黄色) 溶液(橙红色),从物质分类角度
溶液(橙红色),从物质分类角度 属于
属于___________ (“氧化物”、“钾盐”、“碱”);甲、乙、丙中属于氧化还原反应的步骤是___________ 。
(2)“象牙膏”的大实验是向30%的 溶液中加入少量
溶液中加入少量 和表面活性剂,产生大量气泡,像挤出特大号的牙膏一样。制取过氧化氢的过程如下:硫酸重晶石(
和表面活性剂,产生大量气泡,像挤出特大号的牙膏一样。制取过氧化氢的过程如下:硫酸重晶石( )
) 碳酸钡
碳酸钡 氧化钡
氧化钡 过氧化钡
过氧化钡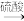 过氧化氢。
过氧化氢。
①过氧化钡的化学式是___________ 。
②用氧化钡制取过氧化钡的反应属于___________ (填字母)反应。
a.化合 b.分解 c.氧化还原
③用过氧化钡( )制取过氧化氢的化学方程式是
)制取过氧化氢的化学方程式是___________ 。
(3)六价铬对人体有毒,含铬废水要经过化学处理后才能排放,方法是用绿矾( )把废水中六价铬还原成三价铬离子,再加入过量的石灰水,使铬离子生成
)把废水中六价铬还原成三价铬离子,再加入过量的石灰水,使铬离子生成 沉淀。
沉淀。 的作用是
的作用是___________ (填写“氧化剂”、“还原剂”)。
(1)医药行业的毒胶囊事件曾被央视《每周质量报告》曝光。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
①胶体中的分散质直径范围是
②元素铬(Cr)的几种化合物存在转化关系:
 固体
固体 溶液(绿色)
溶液(绿色) 溶液(黄色)
溶液(黄色) 溶液(橙红色),从物质分类角度
溶液(橙红色),从物质分类角度 属于
属于(2)“象牙膏”的大实验是向30%的
 溶液中加入少量
溶液中加入少量 和表面活性剂,产生大量气泡,像挤出特大号的牙膏一样。制取过氧化氢的过程如下:硫酸重晶石(
和表面活性剂,产生大量气泡,像挤出特大号的牙膏一样。制取过氧化氢的过程如下:硫酸重晶石( )
) 碳酸钡
碳酸钡 氧化钡
氧化钡 过氧化钡
过氧化钡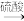 过氧化氢。
过氧化氢。①过氧化钡的化学式是
②用氧化钡制取过氧化钡的反应属于
a.化合 b.分解 c.氧化还原
③用过氧化钡(
 )制取过氧化氢的化学方程式是
)制取过氧化氢的化学方程式是(3)六价铬对人体有毒,含铬废水要经过化学处理后才能排放,方法是用绿矾(
 )把废水中六价铬还原成三价铬离子,再加入过量的石灰水,使铬离子生成
)把废水中六价铬还原成三价铬离子,再加入过量的石灰水,使铬离子生成 沉淀。
沉淀。 的作用是
的作用是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】铁是人类较早使用的金属之一,如图为铁及其化合物的“价—类”二维图。
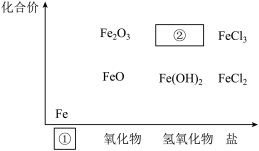
(1)填写二维图缺失的类别①___ 和化学式②___ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2②Fe③NaOH④H2SO4⑤AgNO3。从物质类别上看,FeCl3属于___ ,可能与___ 发生反应(填序号);从化合价角度看,Fe3+具有___ 性,可能与___ 发生反应(填序号)。
(3)下列含铁元素物质既有氧化性又有还原性的是___ (用字母代号填)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(4)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是___ 。
(5)检验溶液中存在Fe3+的试剂是___ ,证明Fe3+存在的现象是___ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:①Cl2②Fe③NaOH④H2SO4⑤AgNO3。从物质类别上看,FeCl3属于
(3)下列含铁元素物质既有氧化性又有还原性的是
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(4)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
(5)检验溶液中存在Fe3+的试剂是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】配平下列反应方程式。
(1)普通配平类
①_______
_______FeSO4 + _______KNO3 + _______H2SO4=_______K2SO4 + _______Fe2(SO4)3 +_______NO↑ +_______H2O
②_______
_______KI + _______KIO3 +_______H2SO4=_______I2 +_______K2SO4 +_______H2O
③_______
_______MnO +_______H+ +_______Cl-=_______Mn2+ +_______Cl2↑+_______H2O
+_______H+ +_______Cl-=_______Mn2+ +_______Cl2↑+_______H2O
④_______
_______NH3 +_______O2 _______NO+ _______H2O
_______NO+ _______H2O
(2)缺项配平类
①_______
_______ClO- +_______Fe(OH)3 +_______=_______Cl- +_______FeO + _______H2O
+ _______H2O
②_______
_______MnO +_______H2O2 +_______=_______Mn2+ + _______O2↑ +_______H2O
+_______H2O2 +_______=_______Mn2+ + _______O2↑ +_______H2O
③某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al2O3、C、N2、AlN、CO。请将反应物与生成物分别填入以下空格内,并配平。_______
 +
+ +
+ →
→ +
+
(1)普通配平类
①
_______FeSO4 + _______KNO3 + _______H2SO4=_______K2SO4 + _______Fe2(SO4)3 +_______NO↑ +_______H2O
②
_______KI + _______KIO3 +_______H2SO4=_______I2 +_______K2SO4 +_______H2O
③
_______MnO
 +_______H+ +_______Cl-=_______Mn2+ +_______Cl2↑+_______H2O
+_______H+ +_______Cl-=_______Mn2+ +_______Cl2↑+_______H2O④
_______NH3 +_______O2
 _______NO+ _______H2O
_______NO+ _______H2O(2)缺项配平类
①
_______ClO- +_______Fe(OH)3 +_______=_______Cl- +_______FeO
 + _______H2O
+ _______H2O②
_______MnO
 +_______H2O2 +_______=_______Mn2+ + _______O2↑ +_______H2O
+_______H2O2 +_______=_______Mn2+ + _______O2↑ +_______H2O③某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al2O3、C、N2、AlN、CO。请将反应物与生成物分别填入以下空格内,并配平。
 +
+ +
+ →
→ +
+
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】铁及其化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)下列微粒中,既有氧化性又有还原性的是_____________________ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中_______ 是还原剂(填“维生素C”或“Fe3+”)。
(3)向FeSO4溶液中滴加NaOH溶液时的现象是:生成的白色絮状沉淀迅速变成___________ 色,最后变成_________ 色。
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”将铜箔腐蚀,反应原理_____________________________ (用离子方程式表示)。
(1)下列微粒中,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中
(3)向FeSO4溶液中滴加NaOH溶液时的现象是:生成的白色絮状沉淀迅速变成
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”将铜箔腐蚀,反应原理
您最近半年使用:0次

 】和木炭,在
】和木炭,在 左右进行冶炼,可能涉及的反应有:
左右进行冶炼,可能涉及的反应有: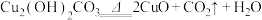 ;②
;② ;
; ;
; 。
。

