如图是一个用石墨作电极,电解稀 溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。
溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。
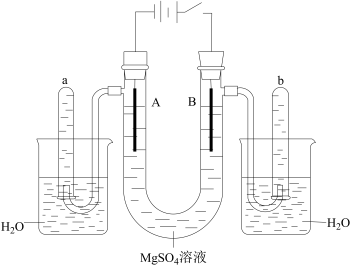
(1)在电解过程中,有关电极附近溶液颜色变化的叙述中正确的是___________ (填序号)。
①A管溶液由红色变为黄色;
②B管溶液由红色变为黄色;
③A管溶液不变色;
④B管溶液不变色。
(2)写出A管中发生的电极反应:___________ 。
(3)写出B管中发生的电极反应:___________ 。
(4)检验a管中气体的方法是___________ 。
(5)检验b管中气体的方法是___________ 。
 溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。
溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。
(1)在电解过程中,有关电极附近溶液颜色变化的叙述中正确的是
①A管溶液由红色变为黄色;
②B管溶液由红色变为黄色;
③A管溶液不变色;
④B管溶液不变色。
(2)写出A管中发生的电极反应:
(3)写出B管中发生的电极反应:
(4)检验a管中气体的方法是
(5)检验b管中气体的方法是
更新时间:2021-12-02 10:43:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化主要形式是___ ,在导线中电子流动方向为___ (用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___ 。
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为___ (填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___ 。
③若A极产生7.00gN2,则此时B极产生___ LH2(标准状况下)。

(1)氢氧燃料电池的能量转化主要形式是
(2)正极反应的电极反应方程式为
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为
②该系统工作时,A极的电极反应式为
③若A极产生7.00gN2,则此时B极产生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】用下图甲所示装置电解饱和食盐水制Cl2、H2和NaOH。

(1)b为电源的______ 极,Cu极的电极反应式为________ 。
(2)某同学在进行上述实验时,发现铜电极下方产生红色沉淀,石墨电极上产生无色无味的气体,则该同学将石墨连接到了电源的______ 极。
(3)电解粗铜制精铜时,可采用NO2、O2和熔融NaNO3制作的燃料电池作电源,其原理如图,该电池在使用过程中石墨 I电极上生成氧化物Y,则其正极的电极反应为:__________ 。


(1)b为电源的
(2)某同学在进行上述实验时,发现铜电极下方产生红色沉淀,石墨电极上产生无色无味的气体,则该同学将石墨连接到了电源的
(3)电解粗铜制精铜时,可采用NO2、O2和熔融NaNO3制作的燃料电池作电源,其原理如图,该电池在使用过程中石墨 I电极上生成氧化物Y,则其正极的电极反应为:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电化学原理在污染治理方面有着重要的作用。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和SO :
:
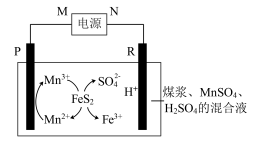
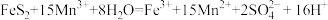
已知:两电极为完全相同的惰性电极。
回答下列问题:
(1)M为电源的___________ (填“正极”或“负极”)。
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式___________ 。
(3)电解池工作时,混合液中SO 的物质的量
的物质的量___________ (填“变大”、“变小”或“不变”)。
(4)电解过程中,混合溶液中的pH将___________ (填“变大”、“变小”或“不变”),理由是___________ 。
Ⅱ.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图。
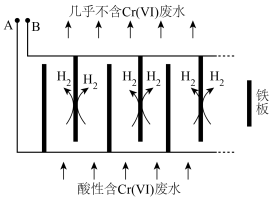
(5)电解开始时,A 极上主要发生的电极反应式为___________ 。
(6)产生的Fe2+将Cr2O 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为___________ 。
(7)随着电解的进行,阳极铁板会发生钝化,表面形成FeO•Fe2O3的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失。结合有关反应,解释钝化膜消失的原因:___________ 。
Ⅲ.微生物电池可用来处理废水中的对氯苯酚,原理如图所示。
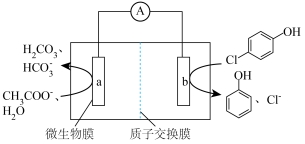
(8)该电池放电时,H+向___________ (填“a”或“b”)极迁移。
(9)a极上生成H2CO3的电极反应为___________ 。
(10)已知b极的电极反应为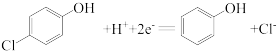 ,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为___________ mol(溶液体积变化忽略不计)。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示,利用电极反应将Mn2+转化为Mn3+,Mn3+再将煤中的含硫物质(主要成分是FeS2)氧化为Fe3+和SO
 :
: 
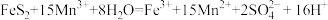
已知:两电极为完全相同的惰性电极。
回答下列问题:
(1)M为电源的
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(3)电解池工作时,混合液中SO
 的物质的量
的物质的量(4)电解过程中,混合溶液中的pH将
Ⅱ.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图。

(5)电解开始时,A 极上主要发生的电极反应式为
(6)产生的Fe2+将Cr2O
 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为(7)随着电解的进行,阳极铁板会发生钝化,表面形成FeO•Fe2O3的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失。结合有关反应,解释钝化膜消失的原因:
Ⅲ.微生物电池可用来处理废水中的对氯苯酚,原理如图所示。

(8)该电池放电时,H+向
(9)a极上生成H2CO3的电极反应为
(10)已知b极的电极反应为
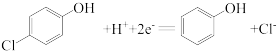 ,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
,经处理后的水样中要求对氯苯酚的含量小于m mol/L。若废水中对氯苯酚的含量是n mol/L,则处理1 m3废水,至少添加CH3COO-的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组的同学用如图所示装置(甲、乙、丙三池中的溶质均足量)研究有关电化学的问题,当闭合该装置的开关K时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为_______ (填“原电池”“电解池”或“电镀池”), A电极的电极反应式为_____ .
(2)丙池中F电极为______ (填“正极”“负极”“阴极”或“阳极”),该池中发生总反应的化学方程式为________
(3)若丙池中两端的电极不变,将其溶液换成NaCl溶液,则开关闭合一段时间后,丙池中溶液的PH将____ (填“增大”“减小”或“不变”)。
(4)当乙池中C极质量减轻4.32 g时,甲池中B电极理论上消耗O2的体积为____ mL(标准状况)。

请回答下列问题:
(1)甲池为
(2)丙池中F电极为
(3)若丙池中两端的电极不变,将其溶液换成NaCl溶液,则开关闭合一段时间后,丙池中溶液的PH将
(4)当乙池中C极质量减轻4.32 g时,甲池中B电极理论上消耗O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图中C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。回答下列问题:

(1)A极为电源_______ 极(填“正”或“负”)。
(2)甲装置中C电极的现象是_______ 。
(3)乙装置中的阴极产物为_______ ,乙装置中电解总反应的离子方程式为_______ 。
(4)装置丙用于铁上镀锌,G应该是_______ (填名称),电镀液的成分是_______ 。
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的微粒,则装置丁中的现象是_________ 。

(1)A极为电源
(2)甲装置中C电极的现象是
(3)乙装置中的阴极产物为
(4)装置丙用于铁上镀锌,G应该是
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的微粒,则装置丁中的现象是
您最近一年使用:0次



