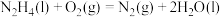下列说法不正确的是
| A.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) △H<0 |
| B.若将等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量多 |
| C.101 kPa时,2H2(g)+ O2(g)= 2H2O(l) △H=﹣572 kJ•mol﹣1,则H2的燃烧热为572 kJ•mol-1 |
D.已知 O2(g)=O(g) △H=+249 kJ•mol﹣1,则O=O键的键能为498 kJ•mol-1 O2(g)=O(g) △H=+249 kJ•mol﹣1,则O=O键的键能为498 kJ•mol-1 |
更新时间:2021-11-11 15:09:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在催化剂作用下,以 和
和 为原料进行合成
为原料进行合成 的实验。保持压强一定,将起始
的实验。保持压强一定,将起始
 的混合气体通过装有催化剂的反应管,测得出口处
的混合气体通过装有催化剂的反应管,测得出口处 的转化率和
的转化率和 的选择性[
的选择性[
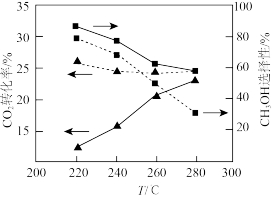
 ]与温度的关系如图所示(图中虚线表示平衡时
]与温度的关系如图所示(图中虚线表示平衡时 的转化率或
的转化率或 的选择性)。
的选择性)。
已知反应管内发生的反应为:
反应1:

反应2:

下列说法正确的是
 和
和 为原料进行合成
为原料进行合成 的实验。保持压强一定,将起始
的实验。保持压强一定,将起始
 的混合气体通过装有催化剂的反应管,测得出口处
的混合气体通过装有催化剂的反应管,测得出口处 的转化率和
的转化率和 的选择性[
的选择性[
 ]与温度的关系如图所示(图中虚线表示平衡时
]与温度的关系如图所示(图中虚线表示平衡时 的转化率或
的转化率或 的选择性)。
的选择性)。
已知反应管内发生的反应为:
反应1:


反应2:


下列说法正确的是
A. 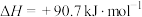 |
B.220℃~280℃时,出口处一定存在: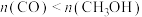 |
C.220℃~280℃,保持其他条件不变,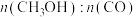 随温度的升高而增加 随温度的升高而增加 |
D.为提高 的产率,应研发高温下催化活性更强的催化剂 的产率,应研发高温下催化活性更强的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在25℃和101kPa的条件下:
对于反应H2(g)+Cl2(g)=2HCl(g)的能量变化描述正确的是
化学键 | H-H | Cl-Cl | H-Cl |
键能(kJ/mol) | 436 | 243 | 431 |
| A.断开1molH2中的H-H键需要放出436kJ的能量 |
| B.生成2molHCl中的H-Cl键需要放出431kJ的能量 |
| C.由键能数据分析,该反应属于吸热反应 |
| D.2molHCl(g)的能量比1molH2(g)和1molCl2(g)的总能量低 |
您最近一年使用:0次
【推荐3】二氧化碳加氢合成二甲醚(CH3OCH3)具有重要的现实意义和广阔的应用前景。该方法主要涉及下列反应:
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
反应Ⅲ:2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5kJ·mol-1
下列说法不正确的是
反应Ⅰ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-49.0 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
反应Ⅲ:2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH3=-24.5kJ·mol-1
下列说法不正确的是
| A.CO2大量排放可导致温室效应 |
| B.干冰升华吸热是因为CO2分子中共价键发生断裂 |
C.反应I的平衡常数可表示为K = |
| D.反应2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)的ΔH= -122.5kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法或表示方法正确的是
A.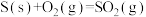 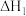 ; ;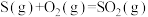 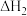 , ,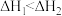 |
B.已知相同质量白磷的能量比红磷高,则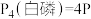 (红磷), (红磷),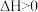 |
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为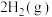  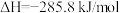 |
D.在稀溶液中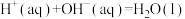  ,若将含1molH2SO4与含2mol NaOH的稀溶液混合,放出的热量等于114.6kJ ,若将含1molH2SO4与含2mol NaOH的稀溶液混合,放出的热量等于114.6kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列化学反应表示正确的是
A.电解饱和NaCl溶液: |
B.钢铁发生吸氧腐蚀的正极反应式: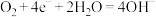 |
C.纯碱溶液呈碱性的原因: |
D.表示氢气燃烧热的热化学方程式: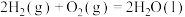  |
您最近一年使用:0次
【推荐1】相关有机物分别与氢气发生加成反应生成1mol环己烷(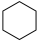 )的能量变化如图所示:
)的能量变化如图所示:
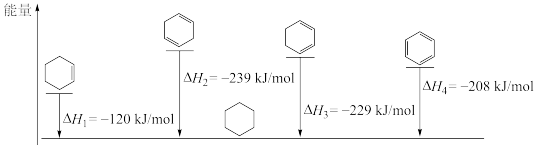
下列推理不正确 的是
 )的能量变化如图所示:
)的能量变化如图所示:
下列推理
| A.2ΔH1≈ΔH2,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比 |
| B.ΔH2<ΔH3,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定 |
| C.3ΔH1<ΔH4,说明苯分子中不存在三个完全独立的碳碳双键 |
| D.ΔH3-ΔH1<0,ΔH4-ΔH3>0,说明苯分子具有特殊稳定性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关说法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
B.已知C(石墨,s)= C(金刚石,s)  ,故金刚石比石墨稳定 ,故金刚石比石墨稳定 |
| C.放热且熵增加的反应须高温才能正向自发进行 |
| D.升高温度能增大单位体积内的活化分子数,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下表是一些常见有机物的燃烧热数值表:
根据表格分析,下列表述正确的是
| 化合物 | 燃烧热/(kJ·mol-1) | 化合物 | 燃烧热/(kJ·mol−1) |
| 甲烷 | 891.0 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 异戊烷 | 3 531.3 |
根据表格分析,下列表述正确的是
| A.丙烷的燃烧热为-2221.5 kJ·mol−1 |
| B.稳定性:正丁烷>异丁烷 |
| C.乙烷燃烧的热化学方程式为2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol−1 |
| D.相同物质的量的烷烃CnH2n+2,n越大,燃烧放出的热量越多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.吸热反应一定需要加热才能进行 |
| B.已知C(石墨,s)=C(金刚石,s) ΔH >0,则金刚石比石墨稳定 |
| C.已知C(s)+O2(g)=CO2(g) ΔH1 ; C(s)+1/2O2(g)=CO(g)ΔH2,则ΔH1>ΔH2 |
| D.已知2CO2(g)=2CO(g)+O2(g)△H=+566 kJ/mol 则CO的燃烧热ΔH =-283.0kJ/mol |
您最近一年使用:0次
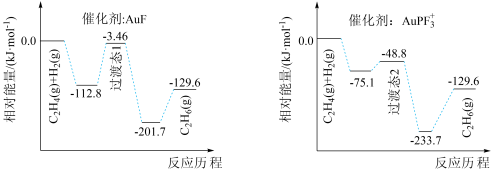
【推荐2】我国科学家研究了不同含金化合物催化乙烯加氢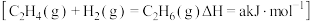 的反应历程如下图所示,下列说法正确的是
的反应历程如下图所示,下列说法正确的是
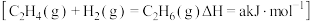 的反应历程如下图所示,下列说法正确的是
的反应历程如下图所示,下列说法正确的是
| A.1 mol C2H4(g)与1 mol H2(g)具有的能量之和小于1 mol C2H6(g)的能量 |
| B.过渡态物质的稳定性:过渡态1<过渡态2 |
C.其余条件相同,催化剂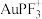 使最终产物能量更低 使最终产物能量更低 |
| D.使用不同的含金化合物作催化剂,反应的△H不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的是
| A.燃烧热的数值都会随反应物的用量不同而改变,故1mol S(s)和2mol S(s)的燃烧热不相等 |
| B.已知:2C(s)+2O2(g)=2CO2(g)ΔH=akJ/mol;2C(s)+2O2(g)=2CO(g)ΔH=bkJ/mol 则a>b |
| C.H2(g)的燃烧热为285.8kJ/mol,则表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol |
| D.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ/mol,在低温条件下不能自发进行,但在高温条件下能自发进行 |
您最近一年使用:0次

 在强碱性条件下能被NaClO氧化生成肼(
在强碱性条件下能被NaClO氧化生成肼( ),常温下
),常温下 ,也可被
,也可被 氧化生成
氧化生成 ,
, 与
与 高温条件下可制备半导体材料砷化镓,
高温条件下可制备半导体材料砷化镓,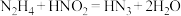
 溶液中通入HCl可以制得
溶液中通入HCl可以制得