按要求填空。
(1)有下列物质:①氢氧化钠固体,②铜丝,③氯化氢气体,④稀硫酸,⑤二氧化碳气体,⑥氨水溶液,⑦碳酸钠粉末,⑧蔗糖晶体,⑨熔融氯化钠,⑩ 晶体。请用序号填空:
晶体。请用序号填空:
i.上述状态下可导电的是___________ 。
ii.属于电解质的是___________ 。
iii.属于非电解质的是___________ 。
iv.上述状态下的电解质不能导电的是___________ 。
(2)向 溶液中逐滴加入
溶液中逐滴加入 溶液至中性,请写出发生反应的离子方程式:
溶液至中性,请写出发生反应的离子方程式:___________ 。
(3)二氧化硫是环境污染物,可用强碱吸收,写出此反应的离子方式___________ 。
(1)有下列物质:①氢氧化钠固体,②铜丝,③氯化氢气体,④稀硫酸,⑤二氧化碳气体,⑥氨水溶液,⑦碳酸钠粉末,⑧蔗糖晶体,⑨熔融氯化钠,⑩
 晶体。请用序号填空:
晶体。请用序号填空:i.上述状态下可导电的是
ii.属于电解质的是
iii.属于非电解质的是
iv.上述状态下的电解质不能导电的是
(2)向
 溶液中逐滴加入
溶液中逐滴加入 溶液至中性,请写出发生反应的离子方程式:
溶液至中性,请写出发生反应的离子方程式:(3)二氧化硫是环境污染物,可用强碱吸收,写出此反应的离子方式
更新时间:2021-11-14 09:25:52
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】阅读下列科普短文并填空
燃料电池是一种活性电池,具有能量转化率高、对环境友好等特点。例如,氢氧燃料电池在工作时,从负极连续通入①氢气,从正极连续通入②氧气,二者在电池内部(含有③H2SO4或④KOH等物质的溶液)发生反应生成⑤H2O,同时产生电能。除了H2、⑥CH4、⑦C2H5OH等也可以作为燃料电池的燃料。目前已研制成功⑧Al-⑨空气燃料电池,它可以代替汽油为汽车提供动力,也可以用做照明电源。
(1)在上述短文标有序号的物质中,属于混合物的是___ (填序号,下同);属于氧化物的是___ ;属于酸的是___ ;属于碱的是___ ;属于有机物的是___ 。
(2)从物质的类别来看,H2、O2、Al都属于___ ;请写出与O2互为同素异形体的物质的化学式___ 。
(3)除H2O外,电解质还有___ ,请写出其中一种电解质的电离方程式___ 。

燃料电池是一种活性电池,具有能量转化率高、对环境友好等特点。例如,氢氧燃料电池在工作时,从负极连续通入①氢气,从正极连续通入②氧气,二者在电池内部(含有③H2SO4或④KOH等物质的溶液)发生反应生成⑤H2O,同时产生电能。除了H2、⑥CH4、⑦C2H5OH等也可以作为燃料电池的燃料。目前已研制成功⑧Al-⑨空气燃料电池,它可以代替汽油为汽车提供动力,也可以用做照明电源。
(1)在上述短文标有序号的物质中,属于混合物的是
(2)从物质的类别来看,H2、O2、Al都属于
(3)除H2O外,电解质还有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有下列物质:①稀硫酸②小苏打③氨水④二氧化碳⑤FeCl3固体⑥稀NaOH溶液⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______ 。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______ 。
(4)能导电的物质序号为_______________ 。
(5)④与⑥充分反应后,将溶液小火蒸干,得到固体混合物。固体组成成分可能是(用化学式表示)___________________________ 。
(6)实验室用⑤制备胶体的化学方程式为__________________________________ 。如果将1molFeCl3全部制成胶体,制得的胶体________ (选填“带负电”“电中性”“带正电”),胶粒数目________ NA(选填“大于”“等于”“小于”)。
(1)上述物质中属于电解质的物质序号为
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为
(4)能导电的物质序号为
(5)④与⑥充分反应后,将溶液小火蒸干,得到固体混合物。固体组成成分可能是(用化学式表示)
(6)实验室用⑤制备胶体的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】二氧化硫是形成酸雨的“罪魁祸首”,为了保护环境,应减少SO2在大气中的排放。请回答下列问题:
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?_____ 。
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:_____ 。
②NaHSO3:_____ 。
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
①SO3是电解质还是非电解质?_____ 。
②O2是电解质还是非电解质?_____ 。
③SO3与NaOH溶液反应可生成NaHSO4.已知NaHSO4=Na++H++ ,则NaHSO4是酸类物质吗?
,则NaHSO4是酸类物质吗?_____ 。
(1)SO2与水反应可生成亚硫酸,那么SO2是电解质还是非电解质?
(2)工业尾气中的SO2常用NaOH溶液吸收,生成Na2SO3或NaHSO3,写出Na2SO3和NaHSO3的电离方程式。
①Na2SO3:
②NaHSO3:
(3)SO2在催化剂的作用下可被氧气氧化成SO3,SO3与水反应生成H2SO4。
①SO3是电解质还是非电解质?
②O2是电解质还是非电解质?
③SO3与NaOH溶液反应可生成NaHSO4.已知NaHSO4=Na++H++
 ,则NaHSO4是酸类物质吗?
,则NaHSO4是酸类物质吗?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据要求,回答下列问题:
(1)下列各组微粒:①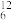 C与
C与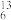 C;②O2和O3;③H(氕)、D(氘)、T(氚);④金刚石和石墨;⑤
C;②O2和O3;③H(氕)、D(氘)、T(氚);④金刚石和石墨;⑤ C和
C和 N,互为同素异形体的是
N,互为同素异形体的是__ (填序号,下同),质量数相等,但不能互称为同位素的是__ 。
(2)足量的D2O和H2O分别与等物质的量的金属钠反应,生成的氢气的质量之比为__ ,转移的电子数之比为__ 。
Ⅱ.现有以下几种物质:①稀硫酸;②熔融态硝酸钾;③硫酸铜晶体;④碳酸钠固体;⑤液态氯化氢;⑥硫酸氢钠固体;⑦CO气体;⑧饱和氯化铁溶液;⑨CO2气体;⑩铜
(3)上述物质中,属于酸性氧化物的是__ (填序号,下同),属于电解质且能导电的是__ 。
(4)⑥的水溶液可以导电的原因是__ (用电离方程式表示)。
(5)将⑧滴入沸水中可制得氢氧化铁胶体,鉴别氢氧化铁胶体制备成功的最简单的方法是__ 。
(6)为检验④中是否含有氯化钠,可取少量试样溶于水后,再进行的实验操作是__ 。
(1)下列各组微粒:①
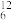 C与
C与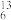 C;②O2和O3;③H(氕)、D(氘)、T(氚);④金刚石和石墨;⑤
C;②O2和O3;③H(氕)、D(氘)、T(氚);④金刚石和石墨;⑤ C和
C和 N,互为同素异形体的是
N,互为同素异形体的是(2)足量的D2O和H2O分别与等物质的量的金属钠反应,生成的氢气的质量之比为
Ⅱ.现有以下几种物质:①稀硫酸;②熔融态硝酸钾;③硫酸铜晶体;④碳酸钠固体;⑤液态氯化氢;⑥硫酸氢钠固体;⑦CO气体;⑧饱和氯化铁溶液;⑨CO2气体;⑩铜
(3)上述物质中,属于酸性氧化物的是
(4)⑥的水溶液可以导电的原因是
(5)将⑧滴入沸水中可制得氢氧化铁胶体,鉴别氢氧化铁胶体制备成功的最简单的方法是
(6)为检验④中是否含有氯化钠,可取少量试样溶于水后,再进行的实验操作是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“咯酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有①吸收性抗酸药,如NaHCO3等。②非吸收性抗酸药,如CaCO3、MgO、Al(OH)3等。
(1)上述所举抗酸药中有___ 种电解质。
(2)NaHCO3作抗酸药时发生反应的离子方程式为___ 。
(3)可溶性重金属盐可以使人中毒,请问___ (填“可以”或“不可以”)服用BaCO3来治疗胃酸(HCl)过多,理由是___ (用离子方程式表示)。
(1)上述所举抗酸药中有
(2)NaHCO3作抗酸药时发生反应的离子方程式为
(3)可溶性重金属盐可以使人中毒,请问
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为_______ 。
②下列措施能提高NO和NO2去除率的有_______ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
③若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是_______ (填化学式);排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂V2O5作用下的脱硝反应机理如图所示。
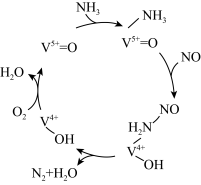
①根据如图机理,等物质的量的NO、NH3在有氧条件下的总化学方程式是_______ 。
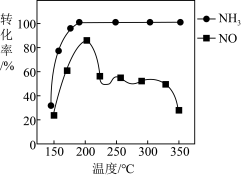
②按上述图中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是_______ 。
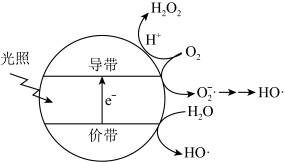
③羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上H2O直接转化为HO·;描述产生HO·的另一种过程:_______ 。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为
②下列措施能提高NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
③若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是
(2)有氧条件下,NO在催化剂作用下可被NH3还原为N2。在钒基催化剂V2O5作用下的脱硝反应机理如图所示。

①根据如图机理,等物质的量的NO、NH3在有氧条件下的总化学方程式是
②按上述图中NH3、NO和O2的比例进行催化脱硝反应。相同反应时间,NH3和NO的转化率与温度的关系如图所示,200℃后,NO转化率急剧下降的原因是

③羟基自由基(HO·)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成HO·;光照时,价带失去电子产生有强氧化性的空穴,价带上H2O直接转化为HO·;描述产生HO·的另一种过程:

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】I。指出下列粒子中带下划线元素的化合价:
(1)Na2O2___________ NH3 ___________ Ca(ClO)2 ___________ HSO
___________
II。现有下列8种物质:
①Cl2 ②钠 ③H2O ④CO2 ⑤ H2SO4 ⑥Fe(OH)3胶体 ⑦ C12H22O11(蔗糖) ⑧NaCl溶液
(2)把上述各物质按物质的分类方法填写在表格的空白处(填物质编号):
(3)写出②与③反应的化学方程式___________ ;
(4)写出⑤与Ba(OH)2溶液反应的离子方程式 ___________ 。
(1)Na2O2

II。现有下列8种物质:
①Cl2 ②钠 ③H2O ④CO2 ⑤ H2SO4 ⑥Fe(OH)3胶体 ⑦ C12H22O11(蔗糖) ⑧NaCl溶液
(2)把上述各物质按物质的分类方法填写在表格的空白处(填物质编号):
| 分类标准 | 电解质 | 非电解质 | 混合物 |
| 属于该类的物质 |
(3)写出②与③反应的化学方程式
(4)写出⑤与Ba(OH)2溶液反应的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】某校化学实验室由于长时间未使用,很多试剂药品摆放杂乱无章,现需要对其进行分类整理,现有药品:①硫酸钠固体②蔗糖溶液③铜④CH3CH2OH⑤石墨⑥液氨⑦NaHCO3溶液⑧稀硫酸⑨碳酸钠粉末⑩氢氧化铁胶体⑪Ba(OH)2固体
(1)其中属于混合物的是___________ (填标号,下同);属于单质的是___________ ;属于盐的是___________ 。
(2)上述物质状态下(除⑩外)能导电的是___________ ;属于电解质的是___________ 。
(3)将少量的⑪加入⑧中发生反应的离子方程式为___________ 。
(1)其中属于混合物的是
(2)上述物质状态下(除⑩外)能导电的是
(3)将少量的⑪加入⑧中发生反应的离子方程式为
您最近一年使用:0次




