R、W、X、Y、Z是原子序数依次增大的短周期主族元素。R的最外层电子数是内层电子数的两倍,X2W2可用于呼吸面具,Y的主族序数与周期数相等,Z的氢化物的分子式为H2Z。
(1)Z在周期表中的位置是______ 。
(2)RZ2的结构式是______ ,X2Z2的电子式是______ 。
(3)H2ZW3在水中电离的方程式为__________________ ,向H2ZW3水溶液滴入少量酸性高锰酸钾溶液,发生反应的离子方程式为__________________ 。
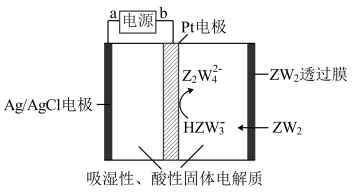
(4)某传感器可以检测空气中ZW2的含量,工作原理如图所示。则电流流向为____________ 时针方向(填“顺”或“逆”),其阴极电极反应式________________________ 。

(1)Z在周期表中的位置是
(2)RZ2的结构式是
(3)H2ZW3在水中电离的方程式为
(4)某传感器可以检测空气中ZW2的含量,工作原理如图所示。则电流流向为
更新时间:2021-12-02 15:56:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如表为元素周期表的一部分,标出了A~K共十种元素所在位置。请用元素符号或化学式 回答下列问题。
(1)10种元素中,化学性质最不活泼的是______ ,最活泼的金属是_____ 。
(2)C、E、F三种元素形成的简单离子半径最小的是_______ 。
(3)化合物C2B2的电子式为__________________ ;该化合物和AB2反应的化学方程式为__________________________________________ 。
(4)E的最高价氧化物属于________________ 性氧化物,它与氢氧化钠溶液反应的离子方程式为____________________________________________ 。
(5)D的单质在A、B形成化合物中燃烧的化学方程式为________________________ 。
(6)用电子式表示H与B组成的H2B型化合物的形成过程_____________________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | ||||||
| 3 | C | D | E | F | G | |||
| 4 | H | I | K |
(1)10种元素中,化学性质最不活泼的是
(2)C、E、F三种元素形成的简单离子半径最小的是
(3)化合物C2B2的电子式为
(4)E的最高价氧化物属于
(5)D的单质在A、B形成化合物中燃烧的化学方程式为
(6)用电子式表示H与B组成的H2B型化合物的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按照要求回答问题。
(1) 的电子式为
的电子式为_______ ,写出其用于呼吸面具做供氧剂的化学方程式:_______ 。
(2)实验室用NaOH浓溶液配制0.1 mol·L NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液_______ mL(保留一位小数),该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管、烧杯之外,还有_______ 。
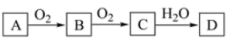
(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,则C→D的化学方程式:
,则C→D的化学方程式:_______ 。
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):_______ 。
(5)高铁酸钠( )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为_______ mol。
(1)
 的电子式为
的电子式为(2)实验室用NaOH浓溶液配制0.1 mol·L
 NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,则C→D的化学方程式:
,则C→D的化学方程式:
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):
(5)高铁酸钠(
 )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaNO2是一种白色易溶于水的固体,溶液呈碱性,其外观与氯化钠相似,有咸味,俗称工业盐;是一 种重要的化学试剂、漂白剂和食品添加剂。已知亚硝酸盐能被溴水氧化,在酸性条件下能氧化亚铁离子; 亚硝酸银是可溶于稀硝酸的白色沉淀。
请完成以下填空:
(1)N原子最外层电子的轨道排布式为_______ ;用一个事实说明氮和氧非金属强弱_______ 。
(2)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出此反应①的离子方程式并标出电子转移的方向和数目______ 。
(3)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,工业上氧化卤水中的I-提取单质I2选择了价格并不便宜的亚硝酸钠,可能的原因是_______ 。
(4)在盐酸溶液中加入亚硝酸钠溶液至中性,则c(Cl-)_____ c(HNO2)(填“<”、“>”或“=”)。
(5)设计一种鉴别亚硝酸钠和氯化钠的实验方案。_______
请完成以下填空:
(1)N原子最外层电子的轨道排布式为
(2)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出此反应①的离子方程式并标出电子转移的方向和数目
(3)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,工业上氧化卤水中的I-提取单质I2选择了价格并不便宜的亚硝酸钠,可能的原因是
(4)在盐酸溶液中加入亚硝酸钠溶液至中性,则c(Cl-)
(5)设计一种鉴别亚硝酸钠和氯化钠的实验方案。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列各题。
(1)氨气(NH3)接触氯化氢(HCl)产生白烟(NH4Cl)。写出该反应的化学方程式:____________ 。
(2)铝热反应可用于焊接铁轨。写出铝(Al)与氧化铁(Fe2O3)在高温下反应生成铁(Fe)与氧化铝(Al2O3)的化学方程式:____________ 。
(1)氨气(NH3)接触氯化氢(HCl)产生白烟(NH4Cl)。写出该反应的化学方程式:
(2)铝热反应可用于焊接铁轨。写出铝(Al)与氧化铁(Fe2O3)在高温下反应生成铁(Fe)与氧化铝(Al2O3)的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)KMnO4作为强氧化剂,其氧化性随溶液的酸性增强而增大,在酸性介质中还原产物是Mn2+,在中性或碱性介质中还原产物主要是MnO2,试写出在酸性条件下氧化H2O2的离子方程式:_______________________ 。
(2)工业上可用KClO3溶液与Na2SO3溶液在稀H2SO4存在下制得ClO2气体,试写出该反应的离子方程式:___ 。
(3)在强酸性混合稀土溶液中加入H2O2,可以将溶液中Ce3+氧化成Ce(OH)4沉淀得以分离,试写出该反应的离子方程式________________________________________________ 。
(4)H3PO2的工业制法是将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式:_________________________________ 。
(1)KMnO4作为强氧化剂,其氧化性随溶液的酸性增强而增大,在酸性介质中还原产物是Mn2+,在中性或碱性介质中还原产物主要是MnO2,试写出在酸性条件下氧化H2O2的离子方程式:
(2)工业上可用KClO3溶液与Na2SO3溶液在稀H2SO4存在下制得ClO2气体,试写出该反应的离子方程式:
(3)在强酸性混合稀土溶液中加入H2O2,可以将溶液中Ce3+氧化成Ce(OH)4沉淀得以分离,试写出该反应的离子方程式
(4)H3PO2的工业制法是将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图是电解NaCl溶液的示意图。请回答下列问题:

(1)石墨电极上的反应式为______________ ;
(2)电解一段时间后,溶液的PH_________ (填“增大”、“减小”或“不变”)。

(1)石墨电极上的反应式为
(2)电解一段时间后,溶液的PH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用电化学原理,将 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应:

(1)甲池工作时, 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用。则石墨Ⅱ是电池的
,可循环使用。则石墨Ⅱ是电池的_____ 极;石墨Ⅰ附近发生的电极反应式为___________ 。
(2)工作时,甲池内的 离子向
离子向___________ 极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的 和
和 的体积比为
的体积比为___________ 。
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为___________ 。
 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应:

(1)甲池工作时,
 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用。则石墨Ⅱ是电池的
,可循环使用。则石墨Ⅱ是电池的(2)工作时,甲池内的
 离子向
离子向 和
和 的体积比为
的体积比为(3)乙池中Fe(Ⅰ)棒上发生的电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加32 g。据此回答问题:

(1)电源的N端为_________ 极;
(2)电极b上发生的电极反应为______________________________________ ;
(3)电极f上生成的气体在标准状况下的体积______________ ;
(4)电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是____________________ ;
(5)电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液__________ ;乙溶液____________ 。

(1)电源的N端为
(2)电极b上发生的电极反应为
(3)电极f上生成的气体在标准状况下的体积
(4)电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是
(5)电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)①基态Cu原子有______ 种不同能级的电子。
②N原子中最高能级的电子的电子云轮廓图为______ 。
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是___________ 。
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价电子排布式是________ ;X3+的价电子排布式为________ 。
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子排布式为____ ,M+的价电子排布式为____ ,M2+的电子排布式为________ 。
(1)①基态Cu原子有
②N原子中最高能级的电子的电子云轮廓图为
③在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
(2)元素X位于第四周期,其基态原子有4个未成对电子,基态X2+的价电子排布式是
(3)M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子,M元素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素是组成我们生活的世界中一切物质的“原材料”。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是___________ 。
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:
(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5.其余元素的信息如图所示:___________ 。
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是___________ 。
③用电子式表示化合物XZ的形成过程是:___________ 。
④X、Y两元素的最高价氧化物对应水化物发生反应的离子方程式为___________ 。
⑤E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:___________ 。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:

(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5.其余元素的信息如图所示:

②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是
③用电子式表示化合物XZ的形成过程是:
④X、Y两元素的最高价氧化物对应水化物发生反应的离子方程式为
⑤E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在高温下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)请写出元素A的名称______ ,B的简单离子示意图______ ;D的简单离子的电子式_____ ;
(2)D元素位于周期表中____ 周期_______ 族,C2B2的电子式:____ ,所含化学键____ 。
(3)电子式表示化合物C2D的形成过程:______________ 。
(1)请写出元素A的名称
(2)D元素位于周期表中
(3)电子式表示化合物C2D的形成过程:
您最近一年使用:0次

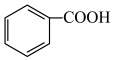
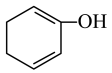 (填“>”、“<”或“=”);用一个化学方程式说明
(填“>”、“<”或“=”);用一个化学方程式说明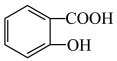 两个官能团酸性的相对强弱
两个官能团酸性的相对强弱 是离子化合物,各原子均满足
是离子化合物,各原子均满足 稳定结构,且两个氮原子环境完全相同。写出
稳定结构,且两个氮原子环境完全相同。写出 的相对分子质量时,实验数据明显大于理论值,原因是
的相对分子质量时,实验数据明显大于理论值,原因是

