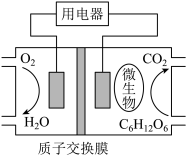
“乌铜走银”是我国非物质文化遗产之一、该工艺将部分氧化的银丝镶嵌于铜器表面,艺人用“出汗的手”边捂边揉搓铜器,铜表面逐渐变黑,银丝变得银光闪闪。下列说法正确的是
| A.“乌铜走银”可以类推:“乌铜走铝” |
| B.“乌铜走银”的反应为Ag2O+Cu=2Ag+CuO |
| C.负极反应式为Ag2O+2e-+H2O=2Ag+2OH- |
| D.每生成40g CuO时转移2mol电子 |
更新时间:2022/01/04 09:46:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】理论上,不能设计为原电池的化学反应是:
| A.2H2(g)+O2(g)═2H2O(l) |
| B.2FeCl3(aq)+Fe(s)═3FeCl3(aq) |
| C.CH4(g)+2O2(g)═CO2(g)+2H2O(l) |
| D.HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
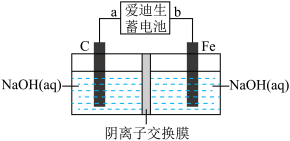
【推荐2】爱迪生发明的镍铁碱性电池的寿命是铅蓄电池的数倍,为了纪念爱迪生的付出,这种电池也叫“爱迪生蓄电池”,其反应原理为:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2,用爱迪生蓄电池制取少量Na2FeO4的装置如图所示。下列说法正确的是
Fe(OH)2+Ni(OH)2,用爱迪生蓄电池制取少量Na2FeO4的装置如图所示。下列说法正确的是
 Fe(OH)2+Ni(OH)2,用爱迪生蓄电池制取少量Na2FeO4的装置如图所示。下列说法正确的是
Fe(OH)2+Ni(OH)2,用爱迪生蓄电池制取少量Na2FeO4的装置如图所示。下列说法正确的是
| A.装置图中爱迪生蓄电池的负极是b |
| B.该电池工作一段时间充电时,生成NiO2的反应是还原反应 |
| C.电解质溶液中OH-透过阴离子交换膜从右池移到左池 |
D.Fe电极上的反应为:Fe-6e-+8OH-=FeO +4H2O +4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有人设计出利用CH4和O2反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法中正确的是
①每消耗1molCH4可以向外电路提供8mol e—
②电池放电时,溶液pH不断升高
③负极上是O2获得电子,电极反应式为:O2+2H2O+4e—=4OH—
④负极上CH4失去电子,电极反应式为:CH4+10OH——8e—= +7H2O
+7H2O
①每消耗1molCH4可以向外电路提供8mol e—
②电池放电时,溶液pH不断升高
③负极上是O2获得电子,电极反应式为:O2+2H2O+4e—=4OH—
④负极上CH4失去电子,电极反应式为:CH4+10OH——8e—=
 +7H2O
+7H2O| A.①④ | B.①③ | C.①② | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】如图是一种新型的光化学电源,当光照射N型半导体时,通入O2和H2S即产生稳定的电流并获得H2O2(H2AQ和AQ是两种有机物)。下列说法错误的是


| A.乙池中N型半导体极为电池的正极 |
| B.H+通过全氟磺酸膜从乙池进入甲池 |
| C.甲池中石墨电极上发生的电极反应为AQ+2H++2e-=H2AQ |
| D.电池工作时发生了光能、化学能、电能之间的转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为Zn+2OH--2e-= ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-。根据上述反应式,判断下列叙述中正确的是
| A.使用过程中,溶液中的OH-向Ag2O极移动 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某原电池装置如图所示,下列叙述错误的是
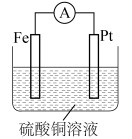
| A.Pt电极为正极 | B.电子由Pt电极经外电路流向Fe电极 |
| C.Fe电极质量减轻 | D.正极的电极反应式: |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
名校
【推荐2】为有效降低含氮化物的排放量,又能充分利用化学能,合作小组设计如图所示电池,将含氮化合物转化为无毒气体。下列说法错误的是
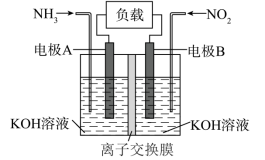
A.该电池的总反应为: |
B.若离子交换膜为阴离子交换膜(只允许阴离子通过),电池工作时 从左侧电极室通过交换膜移向右侧 从左侧电极室通过交换膜移向右侧 |
| C.电池工作一段时间后,右侧电极室溶液的碱性增强 |
| D.同温同压时,左右两侧电极室中产生的气体体积比为4:3 |
您最近一年使用:0次