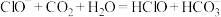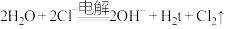钒电池是目前发展势头强劲的绿色环保储能电池之一,其工作原理如图所示,放电时电子由B极一侧向A极移动,电解质溶液含硫酸。常见的含钒阳离子颜色如下表所示。

下列说法不正确 的是

| 离子种类 | 颜色 |
 | 黄色 |
 | 蓝色 |
 | 绿色 |
 | 紫色 |
A.放电时,负极上发生反应的电极反应是: |
B.放电时, 通过离子交换膜由B极一侧向A极移动 通过离子交换膜由B极一侧向A极移动 |
C.充电时,电池总反应为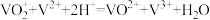 |
| D.当充电完毕后,右侧的储液罐内溶液颜色为紫色 |
更新时间:2022-01-12 22:06:17
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关原电池的叙述中正确的是( )
| A.把电能转变为化学能的装置 |
| B.活泼金属做正极,不活泼金属或非金属做负极 |
| C.外电路中电子从负极流向正极 |
| D.正极发生氧化反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某原电池的总反应的离子方程式为:2Fe3++Fe=3Fe2+,能实现该反应的原电池组成是( )
| A.正极为铜,负极为铁,电解质溶液为NaCl溶液 |
| B.正极为碳,负极为铁,电解质溶液为Fe(NO3)3溶液 |
| C.正极为铁,负极为锌,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为银,负极为铁,电解质溶液为CuSO4溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】铜—锌原电池的工作原理示意图如图,下列说法正确的是


| A.R电极的材料为锌 |
| B.电池工作时,溶液中的H+向P电极移动 |
| C.电池工作时,电解质溶液的pH逐渐增大 |
| D.P电极上的电极反应式:Cu-2e- =Cu2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据反应KMnO4+FeSO4+H2SO4-MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是


| A.石墨b是原电池的负极,乙中发生氧化反应 |
| B.电池工作时,盐桥中的K+向甲烧杯中移动 |
C.甲烧杯中的电极反应式: +5e-+8H+=Mn2++4H2O +5e-+8H+=Mn2++4H2O |
| D.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】北京冬奥会上首次使用的氢燃料电池汽车,其电池工作原理如图,下列说法正确的是

A.气体a为 | B.气体b发生了还原反应 |
| C.该装置实现了电能向化学能的转化 | D.正极室的电极反应式为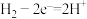 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
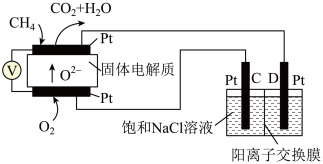
【推荐1】利用CH4燃料电池电解制备Ca(H2PO4)2,装置如图所示。下列说法正确的是


| A.a极反应:CH4+8e-+4O2-=CO2+2H2O |
| B.A、C膜均为阳离子交换膜,B膜为阴离子交换膜 |
| C.该装置开始工作时即可得到产物H2和O2 |
| D.a极上通入2.24L甲烷(标准状况),阳极室Ca2+减少0.8mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验能达到实验目的的是
| A | B | C | D |
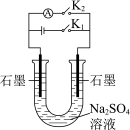 |  |  | 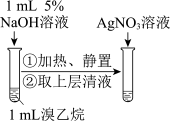 |
| 制作简单的燃料电池 | 证明乙炔具有还原性 | 制备并收集 | 检验溴乙烷的水解产物溴离子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】FFC电解法可由金属氧化物直接电解制备金属单质,西北稀有金属材料研究院利用此法成功电解制备钽粉(Ta),其原理如图所示。下列说法正确的是


| A.该装置将化学能转化为电能 |
| B.a极为电源的正极 |
| C.Ta2O5极发生的电极反应为Ta2O5 +10e− = 2Ta+5O2− |
| D.常温常压下,石墨电极上生成22.4LO2,则电路中转移的电子数为4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,NCl3是一种黄色黏稠状液体,是制备新型水消毒剂ClO2的原料,可以采用如图所示装置制备NCl3。下列说法正确的是
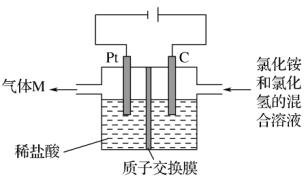
| A.每生成1 mol NCl3,理论上有4 mol H+经质子交换膜由右侧向左侧迁移 |
| B.可用湿润的KI-淀粉试纸检验气体M |
| C.石墨极的电极反应式为NH4++3Cl--6e-===NCl3+4H+ |
| D.电解过程中,电子的流动方向为电源负极→铂棒→石墨棒→电源正极 |
您最近一年使用:0次


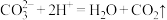
 :
:
 :
: