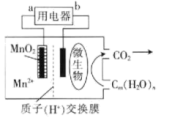
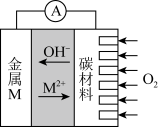
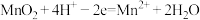将H2S废气资源化的反应原理为2H2S(g)+O2(g)=S2(s)+2H2O(1) △H=-632 kJ·mol-1。如图为H2S燃料电池的示意图,下列说法正确的是
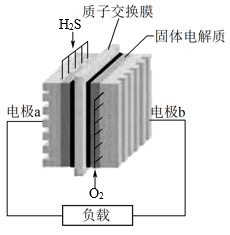

| A.电极a上发生还原反应 |
| B.电极b上发生的电极反应为O2+4H++4e-=2H2O |
| C.电路中每通过2 mol电子,电池内部释放316 kJ热量 |
| D.H+经质子交换膜由a极区移向b极区 |
更新时间:2022-01-13 19:37:13
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】NO2是大气的主要污染物之一,某研究小组设计如图装置对NO2进行回收利用,装置中 a、b 为多孔石墨电极。下列说法正确的是
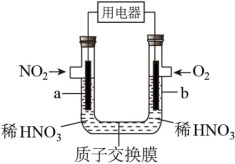

| A.b 为电池的正极,发生氧化反应、 |
| B.a 极的电极反应式为: NO2 2e- 2H+ =NO H2O |
| C.一段时间后,b 极附近HNO3浓度减小 |
| D.电池总反应为4NO2 O2 2H2O=4HNO3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】某金属能和盐酸反应生成H2,该金属与锌组成原电池时,锌为负极,则该金属可能为
| A.铝 | B.铜 | C.锡 | D.铁 |
您最近一年使用:0次
【推荐1】钠离子电池主要依靠钠离子在正极和负极之间移动来工作,具有安全性能高,充电速度快等优点。一种以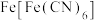 为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是
为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是
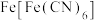 为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是
为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是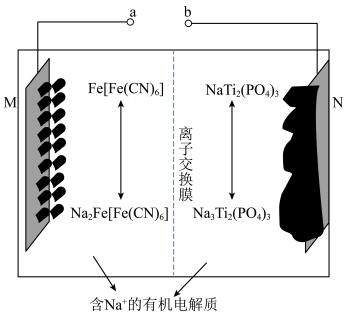
| A.充电时,电极电势:M<N |
B.放电时, 通过离子交换膜从右室移向左室 通过离子交换膜从右室移向左室 |
C.充电时,阳极反应式为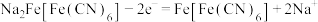 |
D.若初始两电极质量相等,当转移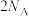 个电子时,两电极质量差为46g 个电子时,两电极质量差为46g |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】某化学小组为了探究铝电极在原电池中的作用,进行了下列实验,实验结果记录如表。下列说法正确的是
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| ① | Mg、Al | 稀盐酸 | 偏向Al |
| ② | Al、Cu | 稀盐酸 | 偏向Cu |
| ③ | Al、石墨 | 稀盐酸 | 偏向____ |
| ④ | Mg、Al | NaOH溶液 | 偏向Mg |
| A.实验①和②中,Al电极的作用不相同 |
| B.实验③中,电流表指针偏向Al |
| C.实验④中,Mg为负极,电极反应式为:Mg-2e-=Mg2+ |
| D.综合以上实验,铝在原电池中的作用,与另一个电极材料和电解质溶液有关 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】钠硫电池作为一种新型化学电源,具有体积小、容量大、寿命长、效率高等重要优点。其结构与工作原理如图所示,下列说法错误的是
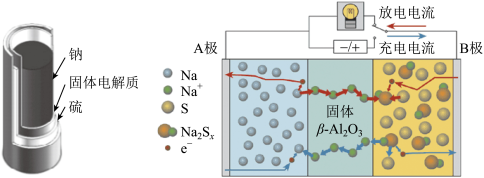

| A.放电过程中,A极为电源正极 |
B.放电过程中,电池总反应为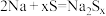 |
C.充电过程中, 由A极移动到B极 由A极移动到B极 |
D.充电过程中,外电路中流过 电子,负极材料增重 电子,负极材料增重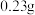 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
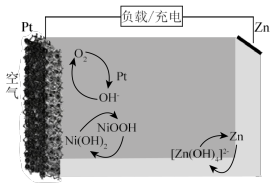
【推荐2】中国科学家试验成功了一种新型的“可呼吸式”镍锌电池( ),充电时产生氧气,放电时吸收氧气,显著提高镍锌电池的能量效率和稳定性,电池工作原理如图。下列说法正确的是
),充电时产生氧气,放电时吸收氧气,显著提高镍锌电池的能量效率和稳定性,电池工作原理如图。下列说法正确的是
 ),充电时产生氧气,放电时吸收氧气,显著提高镍锌电池的能量效率和稳定性,电池工作原理如图。下列说法正确的是
),充电时产生氧气,放电时吸收氧气,显著提高镍锌电池的能量效率和稳定性,电池工作原理如图。下列说法正确的是
| A.该电池为非水系电解质溶液 |
| B.放电时,正极存在两个电极反应 |
C.充电时,阴极反应式: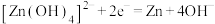 |
| D.放电时,负极质量减少65g,则正极耗氧气11.2L(标准状况) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】氨硼烷(NH3·BH3)电池装置如图所示(起始未加入氨硼烷之前,两极室内液体质量相等),该电池工作时的总反应为NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法错误的是
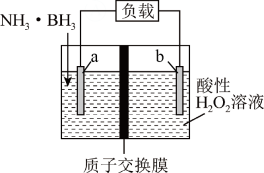

| A.b极为正极 |
| B.电池工作时,H+通过质子交换膜向右移动 |
C.a极反应式为NH3·BH3-6e-+6OH-=NH +BO +BO +4H2O +4H2O |
| D.当加入6.2gNH3·BH3(假设全部消耗)时,左右两极室内液体质量差为5g |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,总反应式为:2C2H6+7O2+8KOH=4K2CO3+10H2O,下列推断正确的是
| A.负极反应为7O2+14 H2O+28e- =28OH- |
| B.每消耗1mol C2H6,则电路上转移的电子为14 mol |
| C.放电一段时间后,负极周围的pH升高 |
| D.放电过程中KOH的物质的量浓度减小 |
您最近一年使用:0次