2019年的诺贝尔化学奖授予锂离子电池研究的三位科学家。下图是一种锂离子电池的工作原理示意图,其负极材料为嵌锂石墨,正极材料为LiCoO2,其总反应可表示为:LixCy+Li1−xCoO2=LiCoO2+Cy。下列说法不正确 的是
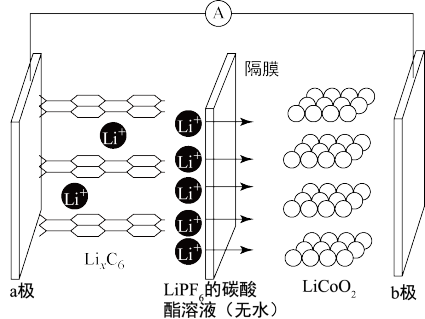

| A.放电时锂离子由a极脱嵌,移向b极 |
| B.充电时b极的反应式为:LiCoO2−xe-=Li1−xCoO2+xLi+ |
| C.充电时,a极接正极,发生还原反应 |
| D.使用LiPF6的碳酸酯溶液作电解液是为了避免使用水溶剂会与金属锂反应 |
21-22高二上·浙江温州·期末 查看更多[5]
更新时间:2022-01-21 21:44:27
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】 电池功率大,可用于海上导航,其结构如图所示(阴离子交换膜仅允许阴离子通过)。下列说法错误的是
电池功率大,可用于海上导航,其结构如图所示(阴离子交换膜仅允许阴离子通过)。下列说法错误的是

 电池功率大,可用于海上导航,其结构如图所示(阴离子交换膜仅允许阴离子通过)。下列说法错误的是
电池功率大,可用于海上导航,其结构如图所示(阴离子交换膜仅允许阴离子通过)。下列说法错误的是
| A.该装置是将化学能转化为电能 |
B.电池工作时, 从碳纤维电极区透过阴离子交换膜移向铝电极区 从碳纤维电极区透过阴离子交换膜移向铝电极区 |
C.Al为负极,负极的电极反应式为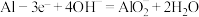 |
D.电子移动方向:铝电极→KOH溶液→离子交换膜→ 溶液→碳纤维电极 溶液→碳纤维电极 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质。下列说法错误的是
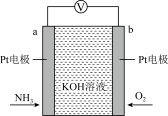

| A.溶液中K+向电极b移动 |
| B.氨气在电极a上发生氧化反应 |
| C.反应消耗的NH3与O2的物质的量之比为4:3 |
| D.正极的电极反应式为:O2+4e-+2H2O=4OH-,故反应一段时间后,电解液的pH升高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】关于如图所示装置的叙述,正确的是
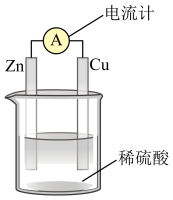

| A.将电能转化为化学能的装置 |
| B.电子由铜片经导线流向锌片 |
| C.锌片为负极,发生氧化反应 |
D.铜片上发生的反应为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,每填充一次燃料,大约可连续24小时输出50W的电力。一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,下列对该燃料电池的说法不正确的是
| A.电路中每流过5mol电子,肯定有5.6 L丙烷被完全氧化 |
| B.该电池的总反应是:C3H8+5O2→3CO2+4H2O |
| C.在熔融电解质中,O2-由正极移向负极 |
| D.通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2-=3CO2+4H2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
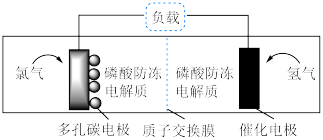
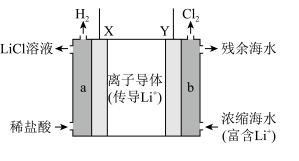
【推荐1】某团队报道了工作温度范围广( )的可充电氢氯电池,模拟装置如图所示。下列叙述正确的是
)的可充电氢氯电池,模拟装置如图所示。下列叙述正确的是
 )的可充电氢氯电池,模拟装置如图所示。下列叙述正确的是
)的可充电氢氯电池,模拟装置如图所示。下列叙述正确的是
| A.放电时,多孔碳电极为负极 |
B.放电时,多孔碳电极附近电解质溶液中 减小 减小 |
C.充电时,多孔碳电极的电极反应式为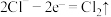 |
D.充电时,若有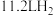 参与反应,则有 参与反应,则有 质子由质子交换膜左侧向右侧迁移 质子由质子交换膜左侧向右侧迁移 |
您最近一年使用:0次
单选题
|
较易
(0.85)
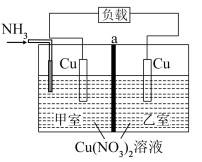
【推荐2】利用电解质溶液的浓度对电极电势的影响,可设计浓差电池。某热再生浓差电池放电时的工作原理如图所示,通入 发生反应
发生反应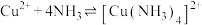 ,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
 发生反应
发生反应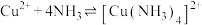 ,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
,电池开始工作,甲室电极质量减少,乙室电极质量增加,中间a为离子交换膜,放电后利用工业废热进行充电。下列说法正确的是
| A.放电时,甲室Cu电极电势高于乙室 |
B.充电时, 经阴离子交换膜a由甲室向乙室迁移 经阴离子交换膜a由甲室向乙室迁移 |
C.放电时,外电路有 电子通过时,乙室溶液质量减少6.4g 电子通过时,乙室溶液质量减少6.4g |
D.电池的总反应为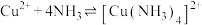 , , |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】锗在航空航天测控、核物理探测、光纤通讯、红外光学、化学催化剂、生物医学等领域有广泛而重要的应用。一种从二氧化锗粗品(主要含GeO2、As2O3)中制备锗的工艺流程如下:
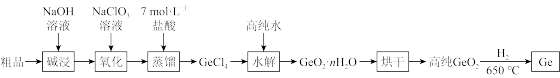
已知:i.GeO2与Al2O3的性质相似;ii.GeCl4易水解,GeCl4的沸点为86.6°C;iii.As2O3+2NaOH=2NaAsO2+H2O,NaAsO2与盐酸反应生成有毒的AsCl3。下列说法不正确的是
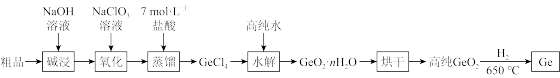
已知:i.GeO2与Al2O3的性质相似;ii.GeCl4易水解,GeCl4的沸点为86.6°C;iii.As2O3+2NaOH=2NaAsO2+H2O,NaAsO2与盐酸反应生成有毒的AsCl3。下列说法不正确的是
| A.已知锗的原子序数为32,可推出其位于元素周期表中第四周期第IVA族 |
| B.工业上对高纯GeO2和SiO2的混合物进行电解制备硅锗合金,则产品在阴极区生成 |
| C.“水解”反应的化学方程式为GeCl4+(n+2)H2O=GeO2·nH2O↓+4HCl |
| D.若“氧化”的目的是将NaAsO2氧化为Na3AsO4,则该反应中氧化剂与还原剂的物质的量之比为3:1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】SO2既是大气主要污染物之一,也是重要的工业原料。工业制硫酸时在接触室中以V2O5为催化剂,发生反应2SO2(g) + O2(g)  2SO3(g) ΔH<0,尾气中的SO2在高温下可被CO、H2还原为硫单质,也可被Na2SO3溶液吸收生成NaHSO3溶液。电解NaHSO3溶液时阴极可生成硫单质。硫单质的熔沸点较低。下列化学反应表示正确的是
2SO3(g) ΔH<0,尾气中的SO2在高温下可被CO、H2还原为硫单质,也可被Na2SO3溶液吸收生成NaHSO3溶液。电解NaHSO3溶液时阴极可生成硫单质。硫单质的熔沸点较低。下列化学反应表示正确的是
 2SO3(g) ΔH<0,尾气中的SO2在高温下可被CO、H2还原为硫单质,也可被Na2SO3溶液吸收生成NaHSO3溶液。电解NaHSO3溶液时阴极可生成硫单质。硫单质的熔沸点较低。下列化学反应表示正确的是
2SO3(g) ΔH<0,尾气中的SO2在高温下可被CO、H2还原为硫单质,也可被Na2SO3溶液吸收生成NaHSO3溶液。电解NaHSO3溶液时阴极可生成硫单质。硫单质的熔沸点较低。下列化学反应表示正确的是A.H2S燃烧生成SO2:H2S + O2  SO2 + H2 SO2 + H2 |
B.高温下CO还原SO2:CO + SO2  S + CO2 S + CO2 |
C.Na2SO3溶液吸收SO2: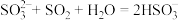 |
D.电解NaHSO3溶液时的阴极反应: −4e-+ 5H+ = S +3H2O −4e-+ 5H+ = S +3H2O |
您最近一年使用:0次



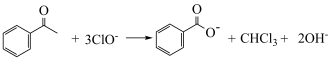
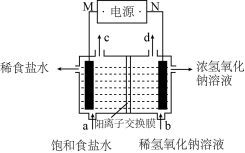
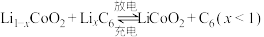 ,以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是
,以该锂离子电池为电源、苯乙酮为原料制备苯甲酸的装置如图所示(苯甲酸盐溶液酸化后可以析出苯甲酸)。下列说法正确的是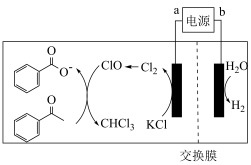
 极质量增加
极质量增加 极发生还原反应
极发生还原反应 为阳离子交换膜
为阳离子交换膜