对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。请利用分类法结合所学知识完成下列各小题:
(1)现有下列9种微粒: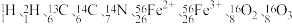 。形成上述9种微粒的核素有
。形成上述9种微粒的核素有___________ 种、元素有___________ 种。以上微粒所含某些元素构成的五核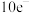 分子的空间构型是
分子的空间构型是___________ ,写出一种由以上两种元素构成含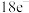 的微粒的电子式
的微粒的电子式___________
(2)现有以下物质:①稀盐酸 ② ③
③ 固体 ④NaOH溶液 ⑤熔融
固体 ④NaOH溶液 ⑤熔融 ⑥
⑥ ⑦铝条 ⑧蔗糖。以上物质中能导电的是
⑦铝条 ⑧蔗糖。以上物质中能导电的是___________ (填标号,下同),属于电解质的是___________ ,属于非电解质的是___________ 。
(3)已知有下列物质:① ②NaCl ③
②NaCl ③ ④
④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦ 这些物质中,只含有离子键的是
这些物质中,只含有离子键的是___________ ,含有非极性共价键的离子化合物是___________ ,属于共价化合物的是___________ 。用电子式表示 的形成过程
的形成过程___________ , 的结构式
的结构式___________
(1)现有下列9种微粒:
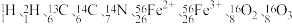 。形成上述9种微粒的核素有
。形成上述9种微粒的核素有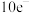 分子的空间构型是
分子的空间构型是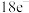 的微粒的电子式
的微粒的电子式(2)现有以下物质:①稀盐酸 ②
 ③
③ 固体 ④NaOH溶液 ⑤熔融
固体 ④NaOH溶液 ⑤熔融 ⑥
⑥ ⑦铝条 ⑧蔗糖。以上物质中能导电的是
⑦铝条 ⑧蔗糖。以上物质中能导电的是(3)已知有下列物质:①
 ②NaCl ③
②NaCl ③ ④
④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦ 这些物质中,只含有离子键的是
这些物质中,只含有离子键的是 的形成过程
的形成过程 的结构式
的结构式
更新时间:2022-01-30 06:54:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据要求回答下列问题。
①CaBr2②H2O③NH4Cl④H2O2⑤Na2O2⑥ ⑦HClO⑧Al
⑦HClO⑧Al
(1)只含有离子键的是___________ (填序号,下同)。
(2)含有共价键的离子化合物是___________ 。
(3)属于共价化合物的是___________ 。
(4)熔融状态下和固态时都能导电的物质是___________ 。
(5)用电子式表示H2O的形成过程___________ 。
①CaBr2②H2O③NH4Cl④H2O2⑤Na2O2⑥
 ⑦HClO⑧Al
⑦HClO⑧Al(1)只含有离子键的是
(2)含有共价键的离子化合物是
(3)属于共价化合物的是
(4)熔融状态下和固态时都能导电的物质是
(5)用电子式表示H2O的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是_____ (填序号,下同);仅发生离子键破坏的是_____ 。
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是_____ ;既存在离子键又存在极性键的是_____ 。
(3)写出下列物质的电子式。
①Na2O2_____ 。
②HClO_____ 。
③NH4Cl_____ 。
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是
(3)写出下列物质的电子式。
①Na2O2
②HClO
③NH4Cl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】图是自然界中氮循环的示意图。

(1) 的电子式是
的电子式是_______ ,氮气在常温下稳定,很难与 反应,说明断开其化学键所吸收的能量
反应,说明断开其化学键所吸收的能量_______ (填“大”或“小”)。
(2)“雷电作用”中氮元素发生了_______ 反应。(填“氧化”或“还原”)
(3)氮循环中,过程①②均会使水中溶解氧的含量_______ (填“增大”或“降低”)。
(4)长期饮用硝酸盐含量超标的水会对健康产生不利影响,某课题组在一定温度下,用铁粉降解水系中的 ,将之转化为
,将之转化为 。
。
①根据Ⅰ、Ⅱ可知, 降解速率的主要影响因素是
降解速率的主要影响因素是_______ 。
②Ⅱ中, 降解的速率为
降解的速率为_______  。(列式即可)
。(列式即可)
③Ⅱ中,铁粉还原 的离子方程式是
的离子方程式是_______ 。

(1)
 的电子式是
的电子式是 反应,说明断开其化学键所吸收的能量
反应,说明断开其化学键所吸收的能量(2)“雷电作用”中氮元素发生了
(3)氮循环中,过程①②均会使水中溶解氧的含量
(4)长期饮用硝酸盐含量超标的水会对健康产生不利影响,某课题组在一定温度下,用铁粉降解水系中的
 ,将之转化为
,将之转化为 。
。| 编号 |  浓度 浓度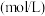 | 反应时间 |  初始浓度 初始浓度 |  终了浓度 终了浓度 |
| Ⅰ | 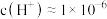 | 24 | 100 | 91 |
| Ⅱ | 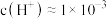 | 24 | 100 | 0 |
 降解速率的主要影响因素是
降解速率的主要影响因素是②Ⅱ中,
 降解的速率为
降解的速率为 。(列式即可)
。(列式即可)③Ⅱ中,铁粉还原
 的离子方程式是
的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有以下10种物质,请回答下列问题:
①干冰②氢氧化钡溶液③铜④稀硫酸⑤Na2SO4溶液⑥熔融碳酸氢钠固体⑦氢氧化钠固体⑧二氧化硫⑨氯化氢⑩NH3⑪Na2CO3
(1)其中能导电的是________ (填写符号,下同);属于电解质的是________ ;属于非电解质的是________ .
(2)写出物质⑪在水中的电离方程式:________________ .
(3)写出物质①和足量⑦在水中发生反应的离子方程式:________________ .
(4)写出②和⑤发生反应的离子方程式:________________ .
(5)写出物质④和⑦反应的离子方程式:________________ .
①干冰②氢氧化钡溶液③铜④稀硫酸⑤Na2SO4溶液⑥熔融碳酸氢钠固体⑦氢氧化钠固体⑧二氧化硫⑨氯化氢⑩NH3⑪Na2CO3
(1)其中能导电的是
(2)写出物质⑪在水中的电离方程式:
(3)写出物质①和足量⑦在水中发生反应的离子方程式:
(4)写出②和⑤发生反应的离子方程式:
(5)写出物质④和⑦反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有如下物质:①石墨② 溶液③稀盐酸④铜⑤
溶液③稀盐酸④铜⑤ 溶液⑥
溶液⑥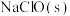 ⑦
⑦ 。请回答下列问题:
。请回答下列问题:
(1)能导电的是_______ (填序号,下同),属于电解质的是_______ 。
(2)NaClO溶液呈碱性,请用离子方程式表示该溶液呈碱性的原因:_______ 。
(3)若向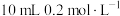 溶液②中逐滴滴加
溶液②中逐滴滴加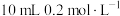 溶液③,实验过程中的现象为
溶液③,实验过程中的现象为_______ ;溶液②中离子浓度由大到小的顺序为_______ 。
(4)已知 ,向
,向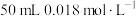 溶液⑤中加入等体积
溶液⑤中加入等体积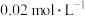 溶液③,混合后溶液中的
溶液③,混合后溶液中的
_______  。(设混合后溶液的体积为原两溶液体积之和)
。(设混合后溶液的体积为原两溶液体积之和)
 溶液③稀盐酸④铜⑤
溶液③稀盐酸④铜⑤ 溶液⑥
溶液⑥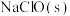 ⑦
⑦ 。请回答下列问题:
。请回答下列问题:(1)能导电的是
(2)NaClO溶液呈碱性,请用离子方程式表示该溶液呈碱性的原因:
(3)若向
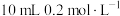 溶液②中逐滴滴加
溶液②中逐滴滴加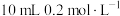 溶液③,实验过程中的现象为
溶液③,实验过程中的现象为(4)已知
 ,向
,向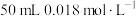 溶液⑤中加入等体积
溶液⑤中加入等体积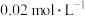 溶液③,混合后溶液中的
溶液③,混合后溶液中的
 。(设混合后溶液的体积为原两溶液体积之和)
。(设混合后溶液的体积为原两溶液体积之和)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)下列物质:①Fe②Br2③Na2O④CO⑤CO2⑥SO3⑦NH3⑧H2S⑨HCl⑩H2SO4⑪Ba(OH)2⑫NaCl⑬蔗糖⑭NaCl溶液。属于电解质的是___ ,属于非电解质的是___ ,能导电的是___ 。
(2)写出下列物质在水中的电离方程式:
NaHSO4:___ 。
H2SO4:___ 。
Ba(OH)2:___ 。
(3)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现___ ,原因:___ ,随后___ ,原因(用离子方程式表示)__ 。
(4)将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图。回答下列问题:

①写出OA段和BC段反应的离子方程式:OA:___ ;BC:___ 。
②原Mg—Al合金的质量是___ 。
③原HCl溶液的物质的量浓度是___ 。
④所加NaOH溶液的物质的量浓度是___ 。
(1)下列物质:①Fe②Br2③Na2O④CO⑤CO2⑥SO3⑦NH3⑧H2S⑨HCl⑩H2SO4⑪Ba(OH)2⑫NaCl⑬蔗糖⑭NaCl溶液。属于电解质的是
(2)写出下列物质在水中的电离方程式:
NaHSO4:
H2SO4:
Ba(OH)2:
(3)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现
(4)将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图。回答下列问题:

①写出OA段和BC段反应的离子方程式:OA:
②原Mg—Al合金的质量是
③原HCl溶液的物质的量浓度是
④所加NaOH溶液的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】【回顾思考】
(1)元素的定义_____________ ,元素种类由__________ 决定。
【观察思考】
(2)请结合教材“观察思考”栏目思考完成以下问题:
①氕、氘、氚的原子结构有何异同?___________________ 。
②氕、氘、氚属于同种元素吗?__________________ 。
(3)①核素:__________________ 。
②同位素:________________ 。
(4)常见的核素种类
①氢元素的三种核素:____________
②碳元素的三种核素:____________
③氧元素的三种核素:____________
④铀元素的三种核素:____________
⑤氯元素的两种核素:____________
(1)元素的定义
【观察思考】
(2)请结合教材“观察思考”栏目思考完成以下问题:
①氕、氘、氚的原子结构有何异同?
②氕、氘、氚属于同种元素吗?
(3)①核素:
②同位素:
(4)常见的核素种类
①氢元素的三种核素:
②碳元素的三种核素:
③氧元素的三种核素:
④铀元素的三种核素:
⑤氯元素的两种核素:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】1.某核素 的氯化物
的氯化物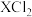 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数A______________ 。
(2)若X的核内中子数为20,求37g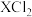 中所含质子的物质的量是
中所含质子的物质的量是______________
2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是______________ ,属于非电解质的是______________
(2)书写硫酸铁电离方程式:_______________________ 书写氯酸钾电离方程式:_______________________
 的氯化物
的氯化物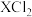 1.11g配成溶液后,需用
1.11g配成溶液后,需用 的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:(1)X的质量数A
(2)若X的核内中子数为20,求37g
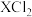 中所含质子的物质的量是
中所含质子的物质的量是2.下列物质中:①酒精 ②氨气 ③硫酸钡 ④铜丝 ⑤二氧化碳 ⑥饱和食盐水 ⑦熔融氯化镁 ⑧醋酸 ⑨氢氧化钠,
(1)属于电解质的是
(2)书写硫酸铁电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)只含离子键的物质有___________ (填序号,下同),只含共价键的物质有___________ 。
(2)属于离子化合物的有___________ ,其中含非极性键的离子化合物有___________ ,含有非极性键的共价化合物有___________ 。
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)只含离子键的物质有
(2)属于离子化合物的有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。请回答以下问题:
(1)F位于第_____ 周期第_____ 族。
(2)G的离子结构示意图为_____ 。
(3)用电子式表示D2的形成过程:______ 。
(4)由A、E、F三种元素形成的化合物的化学式为____ ,含有的化学键有_____ (填化学键类型),属于_____ 化合物。
(5)B的最高价是_____ ,由A、B组成的化合物中,含A量最高的物质的结构式是_____ 。
(1)F位于第
(2)G的离子结构示意图为
(3)用电子式表示D2的形成过程:
(4)由A、E、F三种元素形成的化合物的化学式为
(5)B的最高价是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】针对下面10种元素,完成以下各小题。

(1)金属性最强的元素是________ (填名称);化学性质最不活泼的元素是________ (填元素符号)。
(2)S 原子结构示意图为___________ ;
(3)除Ne以外的其余九种元素的原子中,原子半径最小的是___________ (填元素符号);
(4)元素硅的氧化物常用于制造___________ (填一种高性能的现代通讯材料的名称);
(5)氮元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型为_______________ ;氮元素的氢化物与氯元素的氢化物能生成盐W,W的电子式为____________________ 。
(6)元素最高价氧化物对应的水化物中,碱性最强的是_______ (填化学式),呈两性的是_________ (填化学式);两者反应的化学方程式 __________________________ 。

(1)金属性最强的元素是
(2)S 原子结构示意图为
(3)除Ne以外的其余九种元素的原子中,原子半径最小的是
(4)元素硅的氧化物常用于制造
(5)氮元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型为
(6)元素最高价氧化物对应的水化物中,碱性最强的是
您最近一年使用:0次

 H、
H、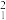 H、
H、 C、
C、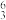 Li、
Li、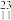 Na、
Na、 N、
N、 Li、
Li、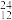 Mg
Mg

