回答下列问题:
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是_____ (填序号,下同);仅发生离子键破坏的是_____ 。
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是_____ ;既存在离子键又存在极性键的是_____ 。
(3)写出下列物质的电子式。
①Na2O2_____ 。
②HClO_____ 。
③NH4Cl_____ 。
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是
(3)写出下列物质的电子式。
①Na2O2
②HClO
③NH4Cl
更新时间:2023-03-26 12:58:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是__ 。
(2)下列关于化学键的说法正确的是____ 。
① 含有金属元素的化合物一定是离子化合物
② 第IA族和第ⅦA族元素原子化合时,一定生成离子键
③ 由非金属元素形成的化合物一定不是离子化合物
④ 活泼金属与非金属化合时,能形成离子键
⑤ 离子键就是阴、阳离子间的相互引力
⑥离子化合物中可能含有非极性共价键
(3)写出下列物质的电子式:Mg(OH)2:____ , N2:_______ ,NH4I:_______ 。
(4)用电子式表示下列化合物的形成过程:Na2S:_______ ;H2O:_______ 。
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)下列关于化学键的说法正确的是
① 含有金属元素的化合物一定是离子化合物
② 第IA族和第ⅦA族元素原子化合时,一定生成离子键
③ 由非金属元素形成的化合物一定不是离子化合物
④ 活泼金属与非金属化合时,能形成离子键
⑤ 离子键就是阴、阳离子间的相互引力
⑥离子化合物中可能含有非极性共价键
(3)写出下列物质的电子式:Mg(OH)2:
(4)用电子式表示下列化合物的形成过程:Na2S:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列9种微粒: 、
、 、
、 、
、 、
、 、
、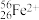 、
、 、
、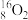 、
、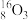 。按要求完成以下各题:
。按要求完成以下各题:
(1)互为同素异形体的微粒是_______ 。
(2)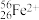 的中子数为
的中子数为_______ ,核外电子数为_______ 。
(3)形成上述9种微粒的核素有_______ 种,元素有_______ 种。
(4)写出下列物质的电子式:NH4Cl_______ ,N2_______ ,HClO_______ 。
(5)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是_______ ;只含有共价键的是_______ ;既含有离子键又含有共价键的是_______ ;含有非极性共价键的化合物是_______ ;不含化学键的是_______ ;属于电解质的是_______ ,属于非电解质的是_______
 、
、 、
、 、
、 、
、 、
、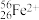 、
、 、
、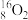 、
、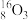 。按要求完成以下各题:
。按要求完成以下各题:(1)互为同素异形体的微粒是
(2)
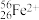 的中子数为
的中子数为(3)形成上述9种微粒的核素有
(4)写出下列物质的电子式:NH4Cl
(5)已知有下列物质:①HNO3②硫单质③NaOH④液氦⑤Na2O2⑥H2O2⑦CCl4⑧NH4Cl⑨KBr⑩O2,分别将正确的序号填入相应的位置。
以上物质中只含有离子键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】NaCN超标的电镀废水可用两段氧化法处理:
①NaCN与NaClO反应,生成NaOCN和NaCl
②NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(K=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)HClO的电子式为___________ 。
(2)第一次氧化时,溶液的pH应调节为____________ (选填“酸性”、“碱性”或“中性”);原因是__________________________________________________ 。
(3)写出第二次氧化时发生反应的离子方程式。_______________________________________
(4)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO______ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
①NaCN与NaClO反应,生成NaOCN和NaCl
②NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(K=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)HClO的电子式为
(2)第一次氧化时,溶液的pH应调节为
(3)写出第二次氧化时发生反应的离子方程式。
(4)处理100 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用可产生NH3。试回答下列问题:
(1)Na3N是_______ 化合物;
(2)Na3N与水的反应属于______ 反应;
(3)Na3N与盐酸反应生成______ 种盐。
(1)Na3N是
(2)Na3N与水的反应属于
(3)Na3N与盐酸反应生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.氢化钠(NaH) 是一种离子化合物,遇水后放出氢气并生成一种碱,主要应用在有机合成和储氢材料方面。根据信息完成下列各空:
(1)氢化钠的电子式为_____________________________ 。
(2)氢化钠与水反应的化学方程式为_____________________ ,反应的氧化剂为___________ 。该反应过程中,被破坏的化学键有_____________ (填序号,下同),形成的化学键有______________ 。
①离子键 ②极性共价键 ③非极性共价键
II.现有短周期元素X 形成的单质A与NaOH溶液反应,有如下转化关系:, (若产物中有水生成则省略未表示出来)。
(若产物中有水生成则省略未表示出来)。
(1)常温常压下,若A 为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为________________________________________________ ;
(2)若A 为金属单质,C 为气体,则A 与NaOH 溶液反应的离子方程式为_____________________________ ;A 最高价氧化物的水化物与NaOH 溶液反应的离子方程式为______________________________ 。
(1)氢化钠的电子式为
(2)氢化钠与水反应的化学方程式为
①离子键 ②极性共价键 ③非极性共价键
II.现有短周期元素X 形成的单质A与NaOH溶液反应,有如下转化关系:,
 (若产物中有水生成则省略未表示出来)。
(若产物中有水生成则省略未表示出来)。(1)常温常压下,若A 为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为
(2)若A 为金属单质,C 为气体,则A 与NaOH 溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】将一块普通的棉布浸在氯化铵的饱和溶液中,片刻后取出晾干就成防火布了。将这块经过处理的布用火柴点,不但点不着,而且还冒出白色的烟雾。氯化铵是很好的防火能手,戏院里的舞台布景、舰艇上的木料等,都经常用氯化铵处理,以求达到防火的目的。
(1)问题一:氯化铵处理棉布作防火布的化学原理是什么___ ?
(2)问题二:氯化铵中含有哪些化学键___ ?属于哪类化合物___ ?
(3)问题三:氯化铵受热分解成NH3和HCl的过程中有什么化学键断裂___ ?形成了什么化学键___ ?
(1)问题一:氯化铵处理棉布作防火布的化学原理是什么
(2)问题二:氯化铵中含有哪些化学键
(3)问题三:氯化铵受热分解成NH3和HCl的过程中有什么化学键断裂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列是中学化学常见的物质
A.金刚石 B.HCl C.NaCl D.Na2SO4 E.Na2S F .He G.N2
请用序号回答(1)-(4)题:
(1)这些物质中只含共价键的是______________
(2)既含离子键又含共价键的是_______________
(3)固态时属于离子晶体的是_______________
(4)熔化时需克服共价键的是______________
(5)试写出E、G的电子式:__________ 、___________
A.金刚石 B.HCl C.NaCl D.Na2SO4 E.Na2S F .He G.N2
请用序号回答(1)-(4)题:
(1)这些物质中只含共价键的是
(2)既含离子键又含共价键的是
(3)固态时属于离子晶体的是
(4)熔化时需克服共价键的是
(5)试写出E、G的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)只含离子键的物质有___________ (填序号,下同),只含共价键的物质有___________ 。
(2)属于离子化合物的有___________ ,其中含非极性键的离子化合物有___________ ,含有非极性键的共价化合物有___________ 。
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ ⑩
⑩
(1)只含离子键的物质有
(2)属于离子化合物的有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列物质:①He;②N2;③H2O2;④CaO;⑤NaHCO3;⑥NH4Cl;⑦Na2O2;⑧SiO2;⑨MgCl2;⑩KOH。请用序号填空:
(1)只含离子键的物质是______________ ;
(2)只含共价键的物质是______________ ;
(3)既含离子键又含共价键的物质是______________ ;
(4)只含极性键的物质是______________ ;
(5)既含离子键又含非极性键的物质是______________ ;
(6)不存在化学键的物质是______________ ;
(7)属于离子化合物的是______________ ;
(8)属于共价化合物的是______________ 。
(1)只含离子键的物质是
(2)只含共价键的物质是
(3)既含离子键又含共价键的物质是
(4)只含极性键的物质是
(5)既含离子键又含非极性键的物质是
(6)不存在化学键的物质是
(7)属于离子化合物的是
(8)属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)写出⑦的原子结构示意图:___________ 。
(2)元素④、⑩、⑪的简单气态氢化物的稳定性最强的是___________ (用化学式表示,下同),元素②、③简单氢化物沸点较高的是___________ 。
(3)元素⑤、⑥最高价氧化物对应的水化物碱性强的是___________ ,元素⑪最高价氧化物对应的水化物的化学式是___________ 。
(4)元素⑤与⑩形成化合物的电子式___________ 。
(5)元素①与⑩形成的最简单化合物中化学键类型为___________ (填“离子键”或“共价键”)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)元素④、⑩、⑪的简单气态氢化物的稳定性最强的是
(3)元素⑤、⑥最高价氧化物对应的水化物碱性强的是
(4)元素⑤与⑩形成化合物的电子式
(5)元素①与⑩形成的最简单化合物中化学键类型为
您最近一年使用:0次



