反应焓变
(1)概念:___________ 的焓与___________ 的焓之差。
(2)表达式:ΔH=___________ ,单位是___________ 。
(3)反应焓变与反应热的关系:对于等压条件下进行的化学反应,如果反应中物质的能量变化只与热能发生转化,则反应热Qp与焓变ΔH的关系是___________ 。
(4)反应焓变与吸热反应和放热反应的关系
(1)概念:
(2)表达式:ΔH=
(3)反应焓变与反应热的关系:对于等压条件下进行的化学反应,如果反应中物质的能量变化只与热能发生转化,则反应热Qp与焓变ΔH的关系是
(4)反应焓变与吸热反应和放热反应的关系
| 图示 |  |  |
| 体系能 量变化 | 反应产物的焓 | 反应产物的焓 |
| 反应类型 |
21-22高二·全国·课前预习 查看更多[2]
更新时间:2022-02-10 11:12:41
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】 或
或 可以催化还原
可以催化还原 以达到消除污染的目的。已知在一定温度下:
以达到消除污染的目的。已知在一定温度下:
 ①
①
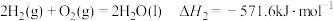 ②
②
 ③
③
(1)在该温度下反应①属于_______ (填“吸热”或“放热”)反应。
(2)在该温度下反应①消耗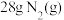 时,
时,
_______ 。
(3)在该温度下反应②生成 时,
时,
_______ 。
(4)在该温度下反应③的
_______ 。
 或
或 可以催化还原
可以催化还原 以达到消除污染的目的。已知在一定温度下:
以达到消除污染的目的。已知在一定温度下: ①
①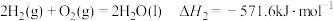 ②
② ③
③(1)在该温度下反应①属于
(2)在该温度下反应①消耗
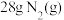 时,
时,
(3)在该温度下反应②生成
 时,
时,
(4)在该温度下反应③的

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】焓
(1)概念:焓是一种“物理量”,用它的变化来描述等压反应的___________ ,符号为___________ 。
(2)单位:___________ 或___________ 。
(3)影响因素:取决于物质的物质的___________ 并受___________ 等因素的影响。
(1)概念:焓是一种“物理量”,用它的变化来描述等压反应的
(2)单位:
(3)影响因素:取决于物质的物质的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】反应热和焓变
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境_______ 的热量。
(2)焓变
①焓(H):焓是与内能有关的物理量。
②焓变( ):生成物的焓与反应物的焓之差。
):生成物的焓与反应物的焓之差。
③焓变与反应热的关系
等压条件下的反应热等于反应的焓变,常用_______ 表示反应热,常用单位:_______ 。
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境
(2)焓变
①焓(H):焓是与内能有关的物理量。
②焓变(
 ):生成物的焓与反应物的焓之差。
):生成物的焓与反应物的焓之差。③焓变与反应热的关系
等压条件下的反应热等于反应的焓变,常用
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)已知1g硫完全燃烧释放的热量为akJ,写出硫的燃烧热的热化学方程式__ ;
(2)真空碳热还原-氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=a kJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=__ kJ·mol-1(用含a、b的代数式表示);
(3)已知 2SO2(g)+O2(g)=2SO3(g) △H反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3放出99kJ的热量,请回答下列问题:
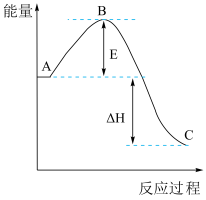
①图中A表示___ ;
②E的大小对该反应的反应热__ (填“有”或“无”)影响;
③该反应通常用V2O5作催化剂,加V2O5会使图中B点__ (填“升高”“降低”)。
(2)真空碳热还原-氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=a kJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=b kJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=
(3)已知 2SO2(g)+O2(g)=2SO3(g) △H反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3放出99kJ的热量,请回答下列问题:

①图中A表示
②E的大小对该反应的反应热
③该反应通常用V2O5作催化剂,加V2O5会使图中B点
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列问题
(1)1 mol C与1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),需要吸收131.5 kJ的热量,该反应的反应热为△H=___________ kJ/mol。
(2)已知反应A(g)+3B(g) 2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为
2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为___________
(3)若各物质的平衡浓度分别为c(A)=2.0 mol/L、c(B)=2.0 mol/L、c(C)=1.0 mol/L,则K=___________ 。
(1)1 mol C与1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),需要吸收131.5 kJ的热量,该反应的反应热为△H=
(2)已知反应A(g)+3B(g)
 2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为
2C(g)在一定温度下达到平衡,该反应的平衡常数表达式为(3)若各物质的平衡浓度分别为c(A)=2.0 mol/L、c(B)=2.0 mol/L、c(C)=1.0 mol/L,则K=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(1)该反应是___________ 反应(填“吸热”或“放热”)。
(2)△H=_______________ 。
(3)反应体系中加入催化剂对反应热是否有影响?___________________ (填“有影响”“无影响”)。
(4)升高温度,该反应的平衡常数K 将_________ (填“增大”“减小”或“不变”)。
 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是
(2)△H=
(3)反应体系中加入催化剂对反应热是否有影响?
(4)升高温度,该反应的平衡常数K 将
您最近一年使用:0次
【推荐3】Ⅰ.如图是1molC(s)和1molH2O(g)反应生成1molCO(g)、1molH2(g)的途径和三个状态的能量。

(1)该反应_____ (填“吸热”或“放热”)反应。
(2)比较E1、E2、E3的大小:_____ 。
Ⅱ.已知2mol氢气燃烧生成液态水时放出572kJ的热量,请回答下列问题:
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量_____ (填“大于”、“小于”或 “等于”)572kJ。
(4)若1mol液态水分解生成氢气和氧气,该反应_____ (填“吸收”或“放出”) _____ kJ的能量。
Ⅲ.已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。
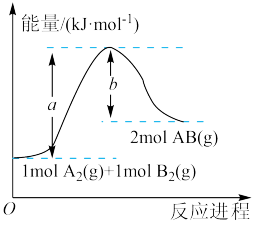
(5)该反应_____ (填“吸收”或“放出”)_____ kJ(用a、b表示)的能量。

(1)该反应
(2)比较E1、E2、E3的大小:
Ⅱ.已知2mol氢气燃烧生成液态水时放出572kJ的热量,请回答下列问题:
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量
(4)若1mol液态水分解生成氢气和氧气,该反应
Ⅲ.已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。

(5)该反应
您最近一年使用:0次

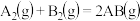 的能量变化如图所示:
的能量变化如图所示:
 、b分别代表的意思是
、b分别代表的意思是


