按要求填空
(1)向CuCl2溶液中滴加NaOH溶液,现象:_______ ,离子方程式:_______
(2)向NaHCO3溶液中滴加稀硫酸,现象:_______ ,离子方程式:_______ ;
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂_______ ,离子方程式:_______ 。
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂_______ ,离子方程式_______ 。
(5)NaHSO4和Ba(OH)2两溶液混合,反应后溶液成中性时的离子方程式为:_______ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀硫酸,现象:
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂
(4)FeSO4 (CuSO4):除杂,括号内为杂质,所加试剂
(5)NaHSO4和Ba(OH)2两溶液混合,反应后溶液成中性时的离子方程式为:
更新时间:2021-12-29 19:55:22
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有四种物质:①铁 ②稀硫酸 ③碳酸氢钠 ④氢氧化钠
(1)属于电解质的是_______ (填序号)。
(2)写出③的电离方程式_______ 。
(3)写出物质②和③反应的离子方程式_______ 。
(4)写出加热固体③发生反应的化学方程式_______ 。
(1)属于电解质的是
(2)写出③的电离方程式
(3)写出物质②和③反应的离子方程式
(4)写出加热固体③发生反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列反应的离子方程式。
(1)铜与硝酸银溶液反应:___ 。
(2)盐酸除铁锈:___ 。
(3)澄清石灰水中加入稀硫酸:___ 。
(4)将硝酸滴到CuO固体上:___ 。
(5)硫酸镁溶液与烧碱溶液混合:___ 。
(6)NaHCO3与KOH两溶液混合:___ 。
(1)铜与硝酸银溶液反应:
(2)盐酸除铁锈:
(3)澄清石灰水中加入稀硫酸:
(4)将硝酸滴到CuO固体上:
(5)硫酸镁溶液与烧碱溶液混合:
(6)NaHCO3与KOH两溶液混合:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)请写出下列反应的化学方程式(①②)或离子方程式(③④),并注明其基本反应类型。
①氢气在氧气中燃烧。________________
②碳酸钙高温分解为二氧化碳和氧化钙。_________
③铝与硫酸反应生成硫酸铝和氢气。__________________
④盐酸和氢氧化钠溶液反应。__________________
(2)根据化学方程式,写出对应的离子方程式:
①AgNO3+KCl=AgCl↓+KNO3______________
②CuO+H2SO4=CuSO4+H2O________________
(3)写出一个能实现下列离子反应的化学方程式:
①Fe+Cu2+=Fe2++Cu___________________
②CO +2H+=CO2↑+H2O
+2H+=CO2↑+H2O ______________
①氢气在氧气中燃烧。
②碳酸钙高温分解为二氧化碳和氧化钙。
③铝与硫酸反应生成硫酸铝和氢气。
④盐酸和氢氧化钠溶液反应。
(2)根据化学方程式,写出对应的离子方程式:
①AgNO3+KCl=AgCl↓+KNO3
②CuO+H2SO4=CuSO4+H2O
(3)写出一个能实现下列离子反应的化学方程式:
①Fe+Cu2+=Fe2++Cu
②CO
 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| HNO3(H2SO4) | ||
| Cu(Fe) | ||
| ZnSO4(CuSO4) | ||
| NaCl(Na2CO3) |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O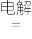 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(1)用单线桥表示出电子转移的方向和数目__ ,题干中反应改写成离子方程式是___ 。
(2)电解食盐水的过程中,被氧化的元素是__ ,被还原的元素是___ ,氧化产物是___ 。
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO 、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。
、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。
①氯化钡、纯碱、烧碱分别除去的离子是___ 、____ 、____ 。
②盐酸与滤液反应的离子方程式:___ 、___ 。
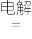 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑(1)用单线桥表示出电子转移的方向和数目
(2)电解食盐水的过程中,被氧化的元素是
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO
 、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。
、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。①氯化钡、纯碱、烧碱分别除去的离子是
②盐酸与滤液反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示:
请回答下列问题。
(1)三次检测结果中第______ 次检测结果肯定不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(不考虑其他酸根离子),进行如下实验:
第一步:向溶液中滴加过量的_____ (填化学式)溶液,其目的是检验CO32-并将其除去;
第二步:加入__________ (填化学式)溶液,其目的是________ ;
第三步:过滤,再向滤液中加入_________ (填化学式)溶液,其目的是____________ 。
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
请回答下列问题。
(1)三次检测结果中第
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(不考虑其他酸根离子),进行如下实验:
第一步:向溶液中滴加过量的
第二步:加入
第三步:过滤,再向滤液中加入
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】选择完成下列实验的装置。

(1)除去粗盐水中的泥沙,用_______ (填序号,下同)。
(2)除去Na2CO3固体中的少量NaHCO3固体,用_______ 。
(3)加热MnO2和浓盐酸的混合物制Cl2,用_______ 。
(4)用饱和碳酸氢钠溶液除去CO2中的HCl,用_______ 。

(1)除去粗盐水中的泥沙,用
(2)除去Na2CO3固体中的少量NaHCO3固体,用
(3)加热MnO2和浓盐酸的混合物制Cl2,用
(4)用饱和碳酸氢钠溶液除去CO2中的HCl,用
您最近一年使用:0次
【推荐2】为除去粗盐中的Ca2+、Mg2+、SO 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
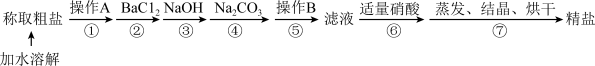
(1)第①步中,操作A是_______ ,第⑤步中,操作B是_______ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)_______ 。
(3)第②步和第③步操作是否可以调换?_______ 理由是_______ 。
(4)第②步与第④步操作是否可以调换?_______ 原因是_______ 。
(5)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因:_______ 。
(6)如何判断SO 已经除尽?
已经除尽?_______ 。
 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)第①步中,操作A是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)
(3)第②步和第③步操作是否可以调换?
(4)第②步与第④步操作是否可以调换?
(5)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因:
(6)如何判断SO
 已经除尽?
已经除尽?
您最近一年使用:0次



