科学家最近发明了一种Al-PbO2电池,电解质为K2SO4、H2SO4、KOH,通过x和y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域(a>b),结构示意图如图所示。下列说法正确的是
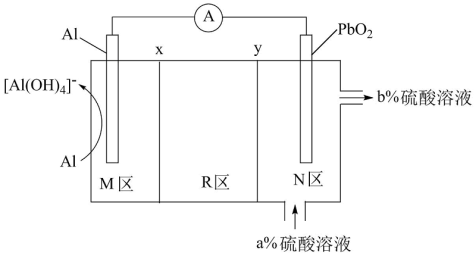

| A.K+通过x膜移向M区 |
| B.R区域的电解质浓度逐渐减小 |
| C.放电时,Al电极反应为:Al-3e-+4OH-=[Al(OH)4]- |
| D.消耗1.8g Al时N区域电解质溶液减少18.0 g |
2022·天津·模拟预测 查看更多[1]
(已下线)一轮巩固卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)
更新时间:2022-03-13 19:32:34
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】高铁电池是一种新型高能高容量电池,某高铁电池的工作原理如图所示。
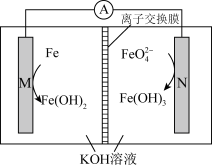
下列说法正确的是

下列说法正确的是
| A.M极电势高于N极电势 |
| B.电池工作时,电子移动方向:M→A→N→M |
C.N极的电极反应式为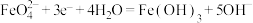 |
| D.电池工作一段时间后,正极区中OH-的物质的量减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示原电池的总反应为Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s),下列叙述正确的是
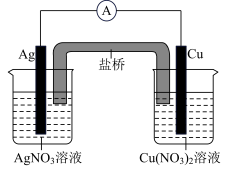

| A.电子从银电极经导线流向铜电极 |
| B.盐桥中的阳离子向硝酸银溶液中迁移 |
| C.电池工作时,铜电极发生还原反应 |
| D.将AgNO3溶液更换为Fe(NO3)3溶液,电流表指针反向偏转 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:相同金属在其不同浓度盐溶液中可形成浓差电池。热再生氨电池工作原理如图所示,通入NH3发生反应Cu2++4NH3 [Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是
[Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是
 [Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是
[Cu(NH3)4]2+,电池开始工作,左边电极质量减少,右边电极质量增加,放电后利用废热进行充电。下列说法正确的是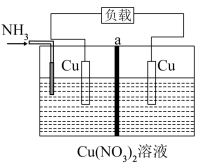
| A.放电、充电过程中,能量主要是在电能与化学能之间转变 |
B.Cu2++4NH3 [Cu(NH3)4]2+正反应为吸热反应 [Cu(NH3)4]2+正反应为吸热反应 |
| C.Cu2+通过中间离子交换膜移向右侧极区 |
| D.放电时,外电路有0.2mol电子通过时,右池溶液质量减少18.8g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以NaBH4(B元素的化合价为+3)和H2O2为原料的电池, 可以作为通讯卫星的高能电池。其电极负极材料为Pt/C,正极材料为MnO2,工作原理如图所示。下列说法不正确的是
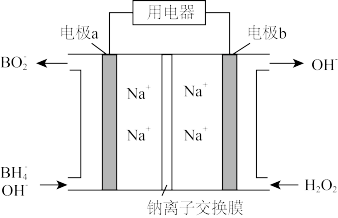

| A.该电池工作时Na+由a极区移向b极区 |
| B.电极b是原电池的正极 |
C.该电池的负极反应为:BH +8OH--8e-=BO +8OH--8e-=BO +6H2O +6H2O |
| D.电路中通过6.02×1022个电子时,理论上消耗H2O2 0.1mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】锂离子电池具有能量密度大、工作寿命长的特点,其原理如图所示。下列说法正确的是
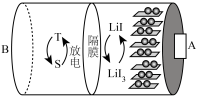
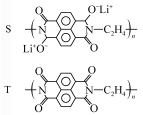


| A.充电时B极与电源正极相连 |
B.放电时A极发生反应 |
| C.充放电过程中,O元素化合价不变 |
D.每生成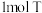 时,转移 时,转移 |
您最近一年使用:0次



