我国规定饮用水质量标准必须符合下列要求:
以下是源水处理成自来水的工艺流程示意图:

(1)源水中含Ca2+ 、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式 。
(2)凝聚剂除去悬浮固体颗粒的过程 (填写编号,多选倒扣分)
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4.7H2O是常用的凝聚剂,它在水中最终生成 沉淀。
(3)通入二氧化碳的目的是 和 。
(4)气体A的作用是 。这种作用是基于气体A和水反应的产物具有 性
(5)下列物质中, 可以作为气体A的代用品。(填写编号,多选倒扣分)
①Ca(ClO)2 ②NH3 (液) ③K2FeO4 ④SO2
| pH | 6.5~6.8 |
| Ca2+、Mg2+总浓度 | <0.0045mol/L |
| 细菌总数 | <100个/L |
以下是源水处理成自来水的工艺流程示意图:

(1)源水中含Ca2+ 、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式 。
(2)凝聚剂除去悬浮固体颗粒的过程 (填写编号,多选倒扣分)
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4.7H2O是常用的凝聚剂,它在水中最终生成 沉淀。
(3)通入二氧化碳的目的是 和 。
(4)气体A的作用是 。这种作用是基于气体A和水反应的产物具有 性
(5)下列物质中, 可以作为气体A的代用品。(填写编号,多选倒扣分)
①Ca(ClO)2 ②NH3 (液) ③K2FeO4 ④SO2
12-13高一上·广东深圳·期末 查看更多[2]
更新时间:2013-03-29 11:55:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列有关钠的问题:
(1)下列各项中属于保存金属钠的正确方法是_______ 。
A.放在细沙中 B.放在水中 C.放在煤油中
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,请写出发生反应的化学方程式:_______
(3)钠和水反应的离子方程式:_______
(4)过氧化钠常用于呼吸面具的来源,其原理为:_______ 。(用化学反应方程式表示),其中每生成1molO2,转移电子_______ mol
(5)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为_______ (填化学式)。
(6)将一定量的CO2通入NaOH溶液中,再向所得溶液中逐滴滴加盐酸,所得气体的体积与加入盐酸的体积关系如图所示:
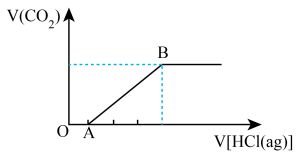
①其中OA段发生的离子反应方程式为_______ 。
②达到B点时所消耗盐酸为50g,已知所用盐酸的质量分数为36.5%,则原溶液中所含溶质NaOH的质量为_______ 。
(1)下列各项中属于保存金属钠的正确方法是
A.放在细沙中 B.放在水中 C.放在煤油中
(2)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,请写出发生反应的化学方程式:
(3)钠和水反应的离子方程式:
(4)过氧化钠常用于呼吸面具的来源,其原理为:
(5)将Na、Na2O、Na2O2、NaOH久置于空气中,最终都是变为
(6)将一定量的CO2通入NaOH溶液中,再向所得溶液中逐滴滴加盐酸,所得气体的体积与加入盐酸的体积关系如图所示:

①其中OA段发生的离子反应方程式为
②达到B点时所消耗盐酸为50g,已知所用盐酸的质量分数为36.5%,则原溶液中所含溶质NaOH的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠、铝、铁是三种重要的金属。请回答:
(1)将一小块金属钠投入水中,发生反应的离子方程式为_____________________ ;可观察到的实验现象是________ (填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.溶液变为红色
(2)Fe跟Cl2在一定条件下反应,所得产物的化学式是__________ 。将该产物溶于水配成溶液,分装在三支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成________ 色。
b.向另一支试管中滴加NaOH溶液,现象为_________________________ ,
c.向第三支试管中加入铁粉,反生的离子方程式是__________________ ,
d.Fe跟H2O在一定条件下反应的化学方程式_______________________ ,
(3)Al既能与盐酸反应又能与氢氧化钠反应,请写出与NaOH溶液反应的化学方程式__________________________________________________ 若反应过程中有1.2mol电子转移,那么消耗NaOH______________ mol .
(1)将一小块金属钠投入水中,发生反应的离子方程式为
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.溶液变为红色
(2)Fe跟Cl2在一定条件下反应,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
c.向第三支试管中加入铁粉,反生的离子方程式是
d.Fe跟H2O在一定条件下反应的化学方程式
(3)Al既能与盐酸反应又能与氢氧化钠反应,请写出与NaOH溶液反应的化学方程式
您最近一年使用:0次
【推荐3】A、B、C、D 4种可溶性盐,它们的阳离子可能分别是 、
、 、
、 、
、 中的某一种,阴离子可能分别是
中的某一种,阴离子可能分别是 、
、 、
、 、
、 中的某一种。
中的某一种。
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为_______ 、_______
(2)写出A与D反应的离子方程式:_______ ;
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是_______ 和_______
 、
、 、
、 、
、 中的某一种,阴离子可能分别是
中的某一种,阴离子可能分别是 、
、 、
、 、
、 中的某一种。
中的某一种。①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为
(2)写出A与D反应的离子方程式:
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学与生产、生活息息相关。回答下列问题:
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:___________ 。
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为___________ 。
(3)补铁剂中的铁元素化合价为___________ ,常和维生素 C 一起服用,说明维 C 具有 ___________ 性。
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为 。该反应中被还原的元素是
。该反应中被还原的元素是___________ (填元素符号)。
(5)安全气囊弹出时发生反应: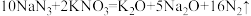 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为___________ 。标准状况下生成 44.8LN2时转移电子个数为 ___________ NA ( NA为阿伏加德罗常数的值)。
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(3)补铁剂中的铁元素化合价为
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为
 。该反应中被还原的元素是
。该反应中被还原的元素是(5)安全气囊弹出时发生反应:
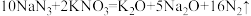 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.无机化合物可根据其组成和性质进行分类。

(1)如图所示的物质分类方法名称是_______ 。
(2)在 Ca、H、O、N 四种元素中任意选择三种元素组成合适的物质,将其化学式分别填在①、②后面的横线上①_______ ,②________ 。
(3)写出向澄清石灰水中通入少量④反应的离子方程式:_______ 。
(4)在盛有 FeCl3溶液的烧杯中,加入氢氧化钠溶液反应后,得到的分散系类别是_______ ;向 Fe(OH)3胶体中逐滴滴入过量的稀硫酸,可观察到的现象是_______ ;
II.选择合适的实验方法完成下列操作(填字母):
A.蒸馏 B.分液 C.升华 D.过滤 E.蒸发结晶 F.溶解、过滤 (洗涤、干燥)、蒸发结晶 G.溶解、蒸发浓缩、冷却结晶、过滤(洗涤、干燥)
(5)分离KCl和MnO2的混合物_______ 。
(6)除去KNO3固体中少量的KCl_______ 。
(7)从碘和氯化钠的混合物中提取碘_______ 。
(8)从NaCl水溶液中提取NaCl固体_______ 。
(9)从海水中得到淡水_______ 。
(10)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)_______ 。

(1)如图所示的物质分类方法名称是
(2)在 Ca、H、O、N 四种元素中任意选择三种元素组成合适的物质,将其化学式分别填在①、②后面的横线上①
(3)写出向澄清石灰水中通入少量④反应的离子方程式:
(4)在盛有 FeCl3溶液的烧杯中,加入氢氧化钠溶液反应后,得到的分散系类别是
II.选择合适的实验方法完成下列操作(填字母):
A.蒸馏 B.分液 C.升华 D.过滤 E.蒸发结晶 F.溶解、过滤 (洗涤、干燥)、蒸发结晶 G.溶解、蒸发浓缩、冷却结晶、过滤(洗涤、干燥)
(5)分离KCl和MnO2的混合物
(6)除去KNO3固体中少量的KCl
(7)从碘和氯化钠的混合物中提取碘
(8)从NaCl水溶液中提取NaCl固体
(9)从海水中得到淡水
(10)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.SO2在工农业生产中有着重要的应用,请回答下列问题:
(1)工业上用软锰矿(主要成分为MnO2)制备Mn(H2PO4)2•2H2O。常用稀硫酸酸浸软锰矿,同时通入SO2,此时发生反应的离子方程式为_____ ,SO2作_____ (填“氧化剂”或“还原剂”)。
Ⅱ.一定温度下,向容积为2L的恒容密闭容器中通入2molSO2和1molO2,在一定条件下发生反应2SO2(g)+O2(g) 2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:
2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:
(2)下列说法能够判断上述反应达到化学平衡状态的是_____ (填标号)。
(3)上述反应体系的正反应速率和逆反应速率相等的时间段是_____ (填“0~4”、“4~8”、“8~12”“12~18”或“18~25”)min。
(4)0~8min内,用SO3表示该反应的平均速率为_____ mol•L-1•min-1,12min时,SO2的转化率为_____ 。
(5)若起始时容器内压强为p0MPa,则平衡时,容器内压强约为_____ (用含p0的代数式表示,保留2位有效数字)MPa。
(1)工业上用软锰矿(主要成分为MnO2)制备Mn(H2PO4)2•2H2O。常用稀硫酸酸浸软锰矿,同时通入SO2,此时发生反应的离子方程式为
Ⅱ.一定温度下,向容积为2L的恒容密闭容器中通入2molSO2和1molO2,在一定条件下发生反应2SO2(g)+O2(g)
 2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:
2SO3(g)。O2的物质的量随时间变化的实验数据如表所示:| 时间/min | 4 | 8 | 12 | 18 | 25 |
| n(O2)/mol | 0.70 | 0.50 | 0.40 | 0.32 | 0.32 |
| A.v(SO2)=2v(O2) | B.容器内气体的平均摩尔质量不再发生变化 |
| C.SO2和O2的浓度之比为2:1 | D.SO3的百分含量不再发生变化 |
(4)0~8min内,用SO3表示该反应的平均速率为
(5)若起始时容器内压强为p0MPa,则平衡时,容器内压强约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】判断下列离子方程式的书写是否正确,并说明理由。
(1)在 溶液中通入足量氯气:
溶液中通入足量氯气:
_____
(2)用石墨电极材料电解 饱和溶液:
饱和溶液: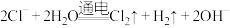
_____
(3)向 溶液中通入二氧化碳气体:
溶液中通入二氧化碳气体: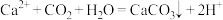
_____
(4)向 溶液中加入稀硫酸:
溶液中加入稀硫酸:
_____
(5)醋酸与锌粒反应: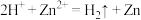
_____
(1)在
 溶液中通入足量氯气:
溶液中通入足量氯气:
(2)用石墨电极材料电解
 饱和溶液:
饱和溶液: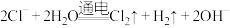
(3)向
 溶液中通入二氧化碳气体:
溶液中通入二氧化碳气体: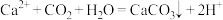
(4)向
 溶液中加入稀硫酸:
溶液中加入稀硫酸:
(5)醋酸与锌粒反应:
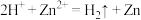
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Zn和浓硫酸反应:Zn+2H+=H2↑+Zn2+。( )
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度下,部分酸的电离平衡常数如下表:
(1)在温度相同时,各酸的Ka值与酸性的相对强弱的关系为_______ 。
(2)室温下①0.1 mol·L-1 HCOONa、②0.1 mol·L-1 NaClO、③0.1 mol·L-1 Na2CO3、④0.1 mol·L-1 NaHCO3溶液中pH由大到小的顺序为_______ 。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为_______ 。
(4)下列离子方程式正确的是_______ (填字母)。
a.2ClO-+H2O+CO2=2HClO+CO
b.2HCOOH+CO =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+SO
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为_______ 。
| 酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 | Ka=1.77×10-4 | Ka=4.0×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)在温度相同时,各酸的Ka值与酸性的相对强弱的关系为
(2)室温下①0.1 mol·L-1 HCOONa、②0.1 mol·L-1 NaClO、③0.1 mol·L-1 Na2CO3、④0.1 mol·L-1 NaHCO3溶液中pH由大到小的顺序为
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO
 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为(4)下列离子方程式正确的是
a.2ClO-+H2O+CO2=2HClO+CO

b.2HCOOH+CO
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑c.H2SO3+2HCOO-=2HCOOH+SO

(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为
您最近一年使用:0次



