某同学在实验室利用橄榄油与甲醇制备生物柴油(高级脂肪酸甲酯),其原理及实验步骤:
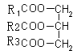 (油脂)+3CH3OH(甲醇)
(油脂)+3CH3OH(甲醇)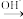
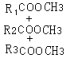 (高级脂肪酸甲酯)+
(高级脂肪酸甲酯)+ 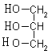 (甘油)
(甘油)
①称取9.2g CH3OH和0.56g KOH依次放入锥形瓶中,充分振荡得KOH的甲醇溶液;
②将40g橄榄油( 平均分子量279~286)、40g 正己烷( 作溶剂)、配好的KOH的甲醇溶液一次加入到三颈烧瓶中;
③连接好装置(如图),保持反应温度在60~64℃左右,搅拌速度350r/min,回流1.5h~2h;
④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:
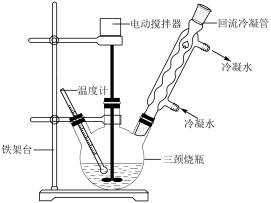
(1)反应中搅拌器的作用是___________ , 保持反应温度在60~64℃左右最好采用哪种加热方式?___________ 。
(2)实验中甲醇过量的主要目的是___________ ; KOH 的用量不宜过多,其原因是___________ 。
(3)步骤④的液体分为两层,上层为生物柴油 、正己烷和甲醇。分离出的上层液体需用温水洗涤,能说明已洗涤干净的依据是___________ 。
(4)油脂的不饱和度可通过油脂与碘的加成反应来测定,通常称为油脂的碘值,碘值越大,油脂的不饱和度越大,碘值是指100g油脂中所能吸收碘的克数;现称取x g实验油脂,加入含y mol I2的溶液(韦氏液,碘值测定时使用的特殊试剂,含CH3COOH),充分振荡;过量的I2用c mol·L-1Na2S2O3溶液滴定(淀粉作指示剂),用去V ml Na2S2O3溶液。(已知: 2Na2S2O3+I2 =Na2S4O6+2NaI)
①该油脂的碘值为___________ 。 (用相关字母表示)
②韦氏液中CH3COOH也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值___________ (填“偏高”“偏低”或“不影响”)。
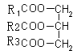 (油脂)+3CH3OH(甲醇)
(油脂)+3CH3OH(甲醇)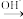
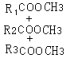 (高级脂肪酸甲酯)+
(高级脂肪酸甲酯)+  (甘油)
(甘油)①称取9.2g CH3OH和0.56g KOH依次放入锥形瓶中,充分振荡得KOH的甲醇溶液;
②将40g橄榄油( 平均分子量279~286)、40g 正己烷( 作溶剂)、配好的KOH的甲醇溶液一次加入到三颈烧瓶中;
③连接好装置(如图),保持反应温度在60~64℃左右,搅拌速度350r/min,回流1.5h~2h;
④冷却、分液、水洗、回收溶剂并得到生物柴油。
回答下列问题:

(1)反应中搅拌器的作用是
(2)实验中甲醇过量的主要目的是
(3)步骤④的液体分为两层,上层为生物柴油 、正己烷和甲醇。分离出的上层液体需用温水洗涤,能说明已洗涤干净的依据是
(4)油脂的不饱和度可通过油脂与碘的加成反应来测定,通常称为油脂的碘值,碘值越大,油脂的不饱和度越大,碘值是指100g油脂中所能吸收碘的克数;现称取x g实验油脂,加入含y mol I2的溶液(韦氏液,碘值测定时使用的特殊试剂,含CH3COOH),充分振荡;过量的I2用c mol·L-1Na2S2O3溶液滴定(淀粉作指示剂),用去V ml Na2S2O3溶液。(已知: 2Na2S2O3+I2 =Na2S4O6+2NaI)
①该油脂的碘值为
②韦氏液中CH3COOH也会消耗Na2S2O3,所以还要做相关实验进行校正,否则会引起测得的碘值
更新时间:2022-02-20 19:22:25
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】研究电解质在水溶液中的离子反应和平衡有重要的意义.
(1)实验人员运用 传感器测定
传感器测定 盐酸滴定
盐酸滴定 未知浓度氨水的
未知浓度氨水的 随盐酸体积的变化情况如图所示。
随盐酸体积的变化情况如图所示。
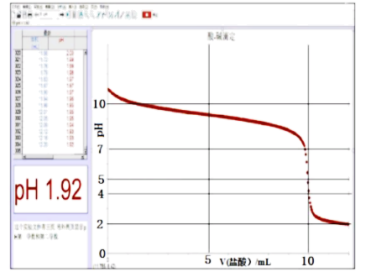
请结合该图回答下列问题:
①盐酸滴定氨水应选择的指示剂为______________ (选填“酚酞”或“甲基橙”).
②滴定终点时,溶液中各离子浓度从大到小的顺序为_____________ .
③滴定曲线上有以下四点: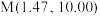 、
、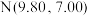 、
、 和
和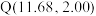 ,所对应的溶液中水的电离程度最大的点是
,所对应的溶液中水的电离程度最大的点是___________ .
(2) 时,三种酸的电离平衡常数(单位略)如表:
时,三种酸的电离平衡常数(单位略)如表:
请回答下列问题:
①相同浓度的 溶液和
溶液和 溶液,前者的
溶液,前者的
_________ (填“>”“<”或“=”下同)后者的 。
。
② 相同且体积相同的盐酸和醋酸溶液中分别滴加相同物质的量浓度的
相同且体积相同的盐酸和醋酸溶液中分别滴加相同物质的量浓度的 溶液至反应完全,消耗
溶液至反应完全,消耗 溶液的体积:V(前者)
溶液的体积:V(前者)_________ V(后者)。
③已知:①氯气与水反应的离子方程式为: ;②“84消毒液”的主要成分为
;②“84消毒液”的主要成分为 .下列叙述正确的是
.下列叙述正确的是_____________ (填序号)。
a.将少量 固体加入醋酸溶液中不会产生气泡
固体加入醋酸溶液中不会产生气泡
b.在新制氯水中加入 固体,可增强该溶液的漂白性
固体,可增强该溶液的漂白性
c.在“84消毒液”中滴入少量白醋,可增强其杀菌消毒能力
④用蒸馏水稀释 的醋酸溶液,下列各式表示的数值随加水量的增加而逐渐减小的
的醋酸溶液,下列各式表示的数值随加水量的增加而逐渐减小的________ 是(填序号)。
a. b.
b.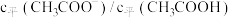
c. d.
d.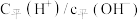
⑤ 时,
时, 的次氯酸溶液中
的次氯酸溶液中 为
为__________  。
。
(1)实验人员运用
 传感器测定
传感器测定 盐酸滴定
盐酸滴定 未知浓度氨水的
未知浓度氨水的 随盐酸体积的变化情况如图所示。
随盐酸体积的变化情况如图所示。
请结合该图回答下列问题:
①盐酸滴定氨水应选择的指示剂为
②滴定终点时,溶液中各离子浓度从大到小的顺序为
③滴定曲线上有以下四点:
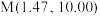 、
、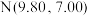 、
、 和
和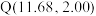 ,所对应的溶液中水的电离程度最大的点是
,所对应的溶液中水的电离程度最大的点是(2)
 时,三种酸的电离平衡常数(单位略)如表:
时,三种酸的电离平衡常数(单位略)如表:| 化学式 |  |  |  |
电离平衡常数 |  | 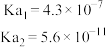 |  |
请回答下列问题:
①相同浓度的
 溶液和
溶液和 溶液,前者的
溶液,前者的
 。
。②
 相同且体积相同的盐酸和醋酸溶液中分别滴加相同物质的量浓度的
相同且体积相同的盐酸和醋酸溶液中分别滴加相同物质的量浓度的 溶液至反应完全,消耗
溶液至反应完全,消耗 溶液的体积:V(前者)
溶液的体积:V(前者)③已知:①氯气与水反应的离子方程式为:
 ;②“84消毒液”的主要成分为
;②“84消毒液”的主要成分为 .下列叙述正确的是
.下列叙述正确的是a.将少量
 固体加入醋酸溶液中不会产生气泡
固体加入醋酸溶液中不会产生气泡b.在新制氯水中加入
 固体,可增强该溶液的漂白性
固体,可增强该溶液的漂白性c.在“84消毒液”中滴入少量白醋,可增强其杀菌消毒能力
④用蒸馏水稀释
 的醋酸溶液,下列各式表示的数值随加水量的增加而逐渐减小的
的醋酸溶液,下列各式表示的数值随加水量的增加而逐渐减小的a.
 b.
b.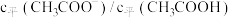
c.
 d.
d.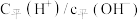
⑤
 时,
时, 的次氯酸溶液中
的次氯酸溶液中 为
为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸四氨合铜晶体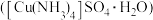 在工业上用途广泛。常温下该物质易溶于水,难溶于乙醇,受热时易发生分解。某化学兴趣小组拟合成硫酸四氨合铜晶体并测定其纯度。
在工业上用途广泛。常温下该物质易溶于水,难溶于乙醇,受热时易发生分解。某化学兴趣小组拟合成硫酸四氨合铜晶体并测定其纯度。
I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)A仪器的名称为______ 。
II.晶体的制备。将上述制备的CuSO4溶液按如图所示进行操作
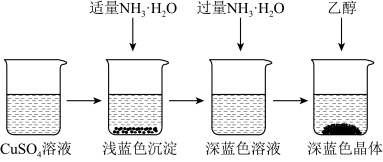
(2)已知浅蓝色沉淀的成分为Cu2OH2SO4,试写出生成此沉淀的离子反应方程式______ 。
(3)析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是______ 。
III.氨含量的测定。精确称取mg晶体,加适量水溶解,然后逐滴加入VmL10%NaOH溶液,加热,将样品液中的氨全部蒸出,用V1mLC1mol/L的盐酸标准溶液完全吸收。然后用C2mol/L的NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
(4)样品中氨的质量分数的表达式______ 。
(5)下列实验操作可能使氨含量测定结果偏高的原因是______ 。
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.滴定达到终点时立刻读数
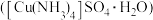 在工业上用途广泛。常温下该物质易溶于水,难溶于乙醇,受热时易发生分解。某化学兴趣小组拟合成硫酸四氨合铜晶体并测定其纯度。
在工业上用途广泛。常温下该物质易溶于水,难溶于乙醇,受热时易发生分解。某化学兴趣小组拟合成硫酸四氨合铜晶体并测定其纯度。I.CuSO4溶液的制备
①称取4g铜粉,在A仪器中灼烧10分钟并不断搅拌,放置冷却。
②在蒸发皿中加入30mL3mol/L的硫酸,将A中固体慢慢放入其中,加热并不断搅拌。
③趁热过滤得蓝色溶液。
(1)A仪器的名称为
II.晶体的制备。将上述制备的CuSO4溶液按如图所示进行操作

(2)已知浅蓝色沉淀的成分为Cu2OH2SO4,试写出生成此沉淀的离子反应方程式
(3)析出晶体时采用加入乙醇的方法,而不是浓缩结晶的原因是
III.氨含量的测定。精确称取mg晶体,加适量水溶解,然后逐滴加入VmL10%NaOH溶液,加热,将样品液中的氨全部蒸出,用V1mLC1mol/L的盐酸标准溶液完全吸收。然后用C2mol/L的NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
(4)样品中氨的质量分数的表达式
(5)下列实验操作可能使氨含量测定结果偏高的原因是
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.滴定达到终点时立刻读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH+6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数_______ (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_______ (填“偏大”、“偏小”或“无影响”)。
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品中氮的质量分数为_______ 。
步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
(2)滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】Ⅰ.充分燃烧1.4 g某有机物A生成4.4 gCO2和1.8 g H2O,该有机物蒸气的密度是相同条件下H2密度的28倍。
(1)该有机物的分子式为________ 。
(2)A的链状同分异构体共________ 种。
(3)A的链状同分异构体中含有支链的同分异构体的结构简式为________ ,其系统命名为________ 。
(4)B是A的某种同分异构体,B的磁共振氢谱中只有4个信号峰(即只有4种氢原子),B通入Br2的CCl4溶液褪色,生成化合物C。则由B生成C的化学方程式为________ 。
Ⅱ.油脂是高级脂肪酸甘油酯,在工业上用途广泛。
(5)以硬脂酸甘油酯为例写出油脂的皂化反应方程式为_____________________ 。
(6)从皂化反应后的溶液中提取肥皂和甘油的过程如下:

加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是_____________________ 。
(1)该有机物的分子式为
(2)A的链状同分异构体共
(3)A的链状同分异构体中含有支链的同分异构体的结构简式为
(4)B是A的某种同分异构体,B的磁共振氢谱中只有4个信号峰(即只有4种氢原子),B通入Br2的CCl4溶液褪色,生成化合物C。则由B生成C的化学方程式为
Ⅱ.油脂是高级脂肪酸甘油酯,在工业上用途广泛。
(5)以硬脂酸甘油酯为例写出油脂的皂化反应方程式为
(6)从皂化反应后的溶液中提取肥皂和甘油的过程如下:

加入食盐颗粒后,液体表面析出白色固体,则食盐的作用是
您最近一年使用:0次
【推荐2】某实验小组设计的糖厂甘蔗渣利用方案如图所示:
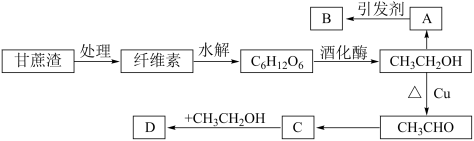
其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
(1)“C6H12O6”所示物质的名称是____ ;C的结构简式为_____ 。
(2)写出A转化为B的化学方程式____ ,反应类型为____ 。
(3)下列说法中正确的是____ 。

其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质。请回答以下问题:
(1)“C6H12O6”所示物质的名称是
(2)写出A转化为B的化学方程式
(3)下列说法中正确的是
| A.物质C和D均可以发生取代反应 |
| B.糖类物质在一定条件下均能发生水解反应 |
| C.动物的脂肪在酸性条件下水解可以得到肥皂的主要成分 |
| D.塑料、合成橡胶、合成纤维、淀粉都是高分子化合物 |
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】下表是A、B、X、D、E五种有机物的有关信息。
(1)B与溴的四氧化碳溶液反应的生成物的名称是_______________ 。
(2)写出在浓硫酸作用下,X与浓硝酸反应的化学方程式______________________________ 。
(3)A与足量NaOH溶液共热发生皂化反应的化学方程式是____________________________ 。
(4)若以B为主要原料合成乙酸,其合成路线如图所示:
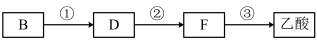
①F的结构简式为____________ 。
②反应②的反应类型为____________ 。
③工业上以B为原料可以合成一种有机高分子。写出反应的化学方程式________________ 。
(5)写出D与E反应的化学方程式____________________________________ 。
| A | A的结构简式 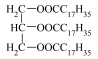 |
| B | ①能使溴的四氯化碳溶液褪色;②比例模型为  ;③能与水在一定条件下反应生成D ;③能与水在一定条件下反应生成D |
| X | ①由C、H两种元素组成;②球棍模型为 |
| D | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应 |
| E | ①由C、H、O三种元素组成;②球棍模型为 |
(2)写出在浓硫酸作用下,X与浓硝酸反应的化学方程式
(3)A与足量NaOH溶液共热发生皂化反应的化学方程式是
(4)若以B为主要原料合成乙酸,其合成路线如图所示:

①F的结构简式为
②反应②的反应类型为
③工业上以B为原料可以合成一种有机高分子。写出反应的化学方程式
(5)写出D与E反应的化学方程式
您最近一年使用:0次



