能量转化是化学变化的主要特征之一,按要求回答下列问题。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主,页岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_______(填序号)。
(2)有关的电池装置如下:
①上述四种电池中,属于二次电池的是_______ (填序号,下同),属于干电池的是_______ 。
②a装置中,外电路中电子的流向是_______ (填“从Zn流向Cu”或“从Cu流向Zn”)。
③c装置中,若电解质改为碱性介质,则负极的电极反应式为_______ 。
(3)氧化还原反应一般可以设计成原电池。若将反应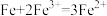 设计成原电池,则:
设计成原电池,则:
①该电池的电解质溶液可以是_______ 。
②当外电路中转移1mol e-时,电解质溶液增加的质量是_______ g。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主,页岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_______(填序号)。
| A.页岩气属于新能源 |
| B.页岩气和氧气的反应是放热反应 |
| C.甲烷中每个原子的最外层电子排布都达到8电子稳定结构 |
| D.页岩气可以作燃料电池的负极燃料 |
| 电池装置 | 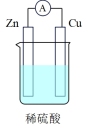 | 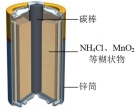 | 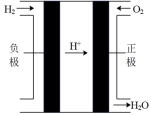 | 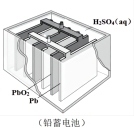 |
| 编号 | a | b | c | d |
①上述四种电池中,属于二次电池的是
②a装置中,外电路中电子的流向是
③c装置中,若电解质改为碱性介质,则负极的电极反应式为
(3)氧化还原反应一般可以设计成原电池。若将反应
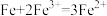 设计成原电池,则:
设计成原电池,则:①该电池的电解质溶液可以是
②当外电路中转移1mol e-时,电解质溶液增加的质量是
更新时间:2022-04-18 22:26:08
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】据图回答下列问题:
(1)若烧杯中溶液为氢氧化钠溶液,则负极为________ (填Mg或Al),总反应方程式为______ 。
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应式为:___________________________ 。
(3)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为:____________ 。
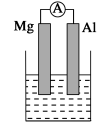
(1)若烧杯中溶液为氢氧化钠溶液,则负极为
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应式为:
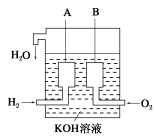
(3)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,则该电池的负极反应式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据上表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同?___________ 。
(2)实验3中铝为___________ 极,电极反应式为 ;
;
(3)实验4中的铝为___________ 极,写出铝电极的电极反应式:___________ 。
(4)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响?___________ 。
Ⅱ.某种燃料电池的工作原理示意如图所示(a、b均为石墨电极)。
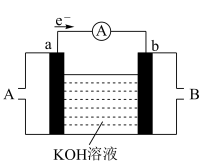
(5)假设使用的“燃料”是氢气( ),则b极的电极反应式为
),则b极的电极反应式为___________ 。
(6)假设使用的“燃料”是甲烷( ),则通入甲烷气体的电极反应式为:
),则通入甲烷气体的电极反应式为:___________ 电池工作一段时间后,电解液的碱性将___________ (填“增强”、“减弱”或“不变”)。
(7)若消耗标准状况下的甲烷4.48L,假设化学能完全转化为电能,则转移电子的数目为___________ (用 表示)。
表示)。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)实验1、2中Al电极的作用是否相同?
(2)实验3中铝为
 ;
;(3)实验4中的铝为
(4)根据以上实验结果,在原电池中相对活泼的金属作正极还是作负极受到哪些因素的影响?
Ⅱ.某种燃料电池的工作原理示意如图所示(a、b均为石墨电极)。

(5)假设使用的“燃料”是氢气(
 ),则b极的电极反应式为
),则b极的电极反应式为(6)假设使用的“燃料”是甲烷(
 ),则通入甲烷气体的电极反应式为:
),则通入甲烷气体的电极反应式为:(7)若消耗标准状况下的甲烷4.48L,假设化学能完全转化为电能,则转移电子的数目为
 表示)。
表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)体积相同,c(H+)相同的盐酸和醋酸溶液分别与足量的颗粒大小相同的锌粒反应,开始时产生氢气的速率________________________________________________ ,充分反应后产生氢气的量_____________ (相同、醋酸的多、盐酸的多),原因是_____________________________________________________________ 。
(2)在一定量的盐酸溶液中加入足量的锌粒,要使产生氢气的量保持不变,但反应速率加快,可加入___________ 晶体,理由是___________________________________________ ;要使产生氢气的量不变,但反应速率减慢,可加入___________________________________ 晶体,理由是_______________________________ 。可供选择的晶体有:
A.纯碱B.烧碱C.胆矾D.醋酸钠E.KHSO4
(2)在一定量的盐酸溶液中加入足量的锌粒,要使产生氢气的量保持不变,但反应速率加快,可加入
A.纯碱B.烧碱C.胆矾D.醋酸钠E.KHSO4
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池.请利用反应“Cu+2Ag+ =2 Ag +Cu2+”,设制一个化学电池(正极材料用碳棒),回答下列问题:
①该电池的负极材料是_______ ,电解质溶液是_____________ ;
②正极的反应式为_____________________ .
③若导线上转移电子1mol,则生成银___________ 克.
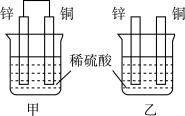
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
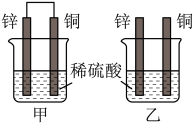
①在相同时间内,两烧杯中产生气泡的速度:甲____________ 乙(填“>”、“<“或“=” ).
②请写出图中构成原电池的负极电极反应式_______________ . 电池工作时,溶液中SO42-向______ 极(填正、负)移动,电池工作完成后,溶液中SO42-浓度_________ (填增大或减小或不变).
(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池.请利用反应“Cu+2Ag+ =2 Ag +Cu2+”,设制一个化学电池(正极材料用碳棒),回答下列问题:
①该电池的负极材料是
②正极的反应式为
③若导线上转移电子1mol,则生成银
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①在相同时间内,两烧杯中产生气泡的速度:甲
②请写出图中构成原电池的负极电极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】生活中,形式多样化的电池,满足不同的市场需求。图中是几种不同类型的原电池装置。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。
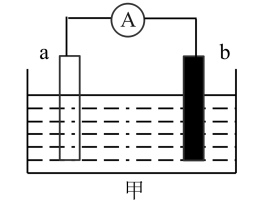
①若容器中盛有 溶液,a极为
溶液,a极为_______ (填“正极”或“负极”);b极附近观察到的现象是_______ 。
②若容器中盛有浓硫酸,b极的电极反应式是_______ ,导线中电子的流动方向是_______ (填“a→b”或“b→a”)。
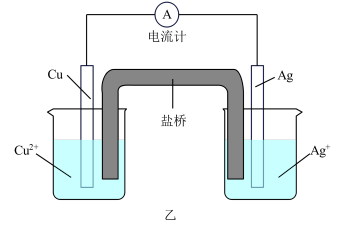
(2)铜-银原电池装置如图乙所示,下列有关叙述正确的是_______(填标号)。
(3)乙烯是水果的催熟剂,又可用作燃料,由 和
和 组成的燃料电池的结构如图丙所示。
组成的燃料电池的结构如图丙所示。
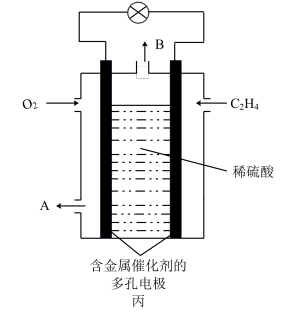
①乙烯燃料电池的正极反应式是_______ 。
②当消耗2.8g乙烯时,生成物质B的体积为_______ L(标准状况下)。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。

①若容器中盛有
 溶液,a极为
溶液,a极为②若容器中盛有浓硫酸,b极的电极反应式是
(2)铜-银原电池装置如图乙所示,下列有关叙述正确的是_______(填标号)。

| A.银电极上发生还原反应 |
| B.电池工作一段时间后,铜极的质量增加 |
| C.取出盐桥后,电流计依旧发生偏转 |
| D.电池工作时,每转移0.1mol电子,两电极的质量差会增加14g |
 和
和 组成的燃料电池的结构如图丙所示。
组成的燃料电池的结构如图丙所示。
①乙烯燃料电池的正极反应式是
②当消耗2.8g乙烯时,生成物质B的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
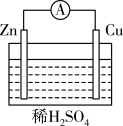
【推荐1】由铜、锌和硫酸溶液组成的原电池中,作正极的是____ (填化学式),正极的电极反应式为____ ;作负极的是____ (填化学式),电子由____ (填“正”或“负”,下同)极经导线移向_____ 极。

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】由Zn—Cu—H2SO4组成的原电池,工作一段时间后,锌片的质量减少了6.5g。求:
(1)原电池的_______ 极生成氢气_______ L(标准状况)。
(2)已知:1mol氢气完全燃烧放出285.8kJ的热量。将(1)中获得的氢气燃烧,可以得到_________ kJ的热量。
(3)若将电解质溶液改为硫酸铜溶液,当电池输出相同的电量时,电池两极的质量差为_____________ 。
(1)原电池的
(2)已知:1mol氢气完全燃烧放出285.8kJ的热量。将(1)中获得的氢气燃烧,可以得到
(3)若将电解质溶液改为硫酸铜溶液,当电池输出相同的电量时,电池两极的质量差为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】该小组同学设想用电解硫酸钠溶液装置来制取氧气、氧气、硫酸和氧氧化钠。请结合实验小组探究活动设想图,回答下列问题:
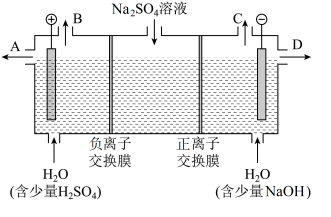
(1)B出口导出的气体是________ 。
(2)制得的氢氧化钠溶液从出口________ (填“A”、“B”、“C”或“D”)导出。
(3)通过负离子交换膜的离子数________ (填“>”、“<”或“=”)通过正离子交换膜的离子数。
(4)氢气、氧气和氢氧化钠溶液又可制成燃料电池,该电池的负极反应式为________________ 。

(1)B出口导出的气体是
(2)制得的氢氧化钠溶液从出口
(3)通过负离子交换膜的离子数
(4)氢气、氧气和氢氧化钠溶液又可制成燃料电池,该电池的负极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某学生利用下面实验装置探究盐桥式原电池的工作原理。按照实验步骤依次回答下列问题:
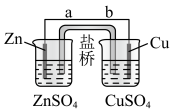
(1)锌电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ 。
(2)导线中电子流向为___________ (用 、
、 表示)。
表示)。
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子数目为___________ ;
(4)装置中盐桥中除添加琼脂外,还要添加 的饱和溶液,电池工作时,对盐桥中的
的饱和溶液,电池工作时,对盐桥中的 ,
, 的移动方向描述正确的是___________。
的移动方向描述正确的是___________。
(5)若 溶液中含有杂质
溶液中含有杂质 ,会加速
,会加速 电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去
电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去 ,最好选用下列试剂中的___________(填代号)。
,最好选用下列试剂中的___________(填代号)。

(1)锌电极为电池的
(2)导线中电子流向为
 、
、 表示)。
表示)。(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子数目为
(4)装置中盐桥中除添加琼脂外,还要添加
 的饱和溶液,电池工作时,对盐桥中的
的饱和溶液,电池工作时,对盐桥中的 ,
, 的移动方向描述正确的是___________。
的移动方向描述正确的是___________。A.盐桥中的 向左侧烧杯移动、 向左侧烧杯移动、 向右侧烧杯移动 向右侧烧杯移动 |
B.盐桥中的 向右侧烧杯移动、 向右侧烧杯移动、 向左侧烧杯移动 向左侧烧杯移动 |
C.盐桥中的 、 、 都向右侧烧杯移动 都向右侧烧杯移动 |
D.盐桥中的 、 、 几乎都不移动 几乎都不移动 |
(5)若
 溶液中含有杂质
溶液中含有杂质 ,会加速
,会加速 电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去
电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去 ,最好选用下列试剂中的___________(填代号)。
,最好选用下列试剂中的___________(填代号)。A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】I.如图所示的三个烧杯中,烧杯中都盛有稀硫酸。请回答以下问题:
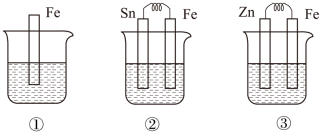
(1)①中反应的离子方程式为___ 。
(2)②所示原电池中,Fe电极为电池的___ 极,发生的电极方程式为:___ ,Sn极发生___ (填“氧化”或“还原”)反应,随着反应的进行,Sn极附近溶液的pH逐渐___ (填增大、减小或不变)。
(3)③中被腐蚀的金属是___ ,电解质溶液中的H+向___ 极移动,随着反应的进行,溶液中SO 的浓度逐渐
的浓度逐渐___ (填“增大”、“减小”或“不变”)。
(4)比较①、②、③中铁被腐蚀的速率由快到慢的顺序是___ 。
II.利用下列反应:Fe+2Fe3+=3Fe2+设计一个原电池,请选择适当的材料和试剂。
(1)请写出你选用的正极材料、负极材料、电解质溶液)写化学式):正极为___ ,负极为___ ,电解质溶液:___ 。
(2)负极反应式:__ 。

(1)①中反应的离子方程式为
(2)②所示原电池中,Fe电极为电池的
(3)③中被腐蚀的金属是
 的浓度逐渐
的浓度逐渐(4)比较①、②、③中铁被腐蚀的速率由快到慢的顺序是
II.利用下列反应:Fe+2Fe3+=3Fe2+设计一个原电池,请选择适当的材料和试剂。
(1)请写出你选用的正极材料、负极材料、电解质溶液)写化学式):正极为
(2)负极反应式:
您最近一年使用:0次

 均
均


