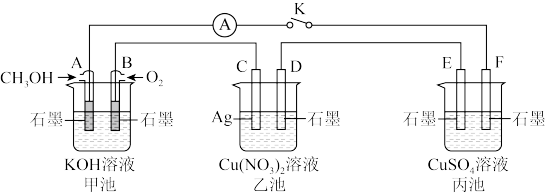
某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键 K 时,观察到电流计的指针发生了偏转。
请回答下列问题:
(1)甲池为_______ (选填“原电池”、“电解池”),A电极的电极反应式为 _______ 。
(2)丙池中F电极为_______ (选填“正极”、“负极”、“阴极”或“阳极”),该池的总反应的化学方程式为 _______ 。
(3)当池中C极质量减少10.8 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况下),一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是_______ (填字母)。
A.Cu B.CuO C.Cu(OH)2 D.CuCO3
(4)常温下,已知丙池中的溶液为 400 mL,合上开关 K,一段时间后,丙池中,阳极共收集到气体 224 mL(标准状况下)气体,则此时溶液的pH为_______ 。

请回答下列问题:
(1)甲池为
(2)丙池中F电极为
(3)当池中C极质量减少10.8 g时,甲池中B电极理论上消耗O2的体积为
A.Cu B.CuO C.Cu(OH)2 D.CuCO3
(4)常温下,已知丙池中的溶液为 400 mL,合上开关 K,一段时间后,丙池中,阳极共收集到气体 224 mL(标准状况下)气体,则此时溶液的pH为
更新时间:2022-04-14 15:33:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】生物电池具有工作时不发热、不损坏电极等优点,不但可以节约大量金属,而且寿命比化学电源长的多,因此越来越受到人们的青睐。某生物电池以葡萄糖(C6H12O6)作原料,在酶的作用下被氧化为葡萄糖酸(C6H12O7),其工作原理如图所示。
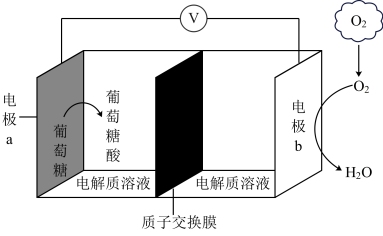
(1)电极b为___________ (填“正极”或“负极”),电极a的电极反应式为___________ 。
(2)该生物电池中发生反应的化学方程式为___________ ,当有2molH+通过质子交换膜时,理论上需要标准状况下氧气的体积为___________ L。
(3)该电池___________ (填“能”或“不能”)在高温条件下使用,原因是___________ 。

(1)电极b为
(2)该生物电池中发生反应的化学方程式为
(3)该电池
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,组成一种原电池。试回答下列问题(灯泡功率合适):
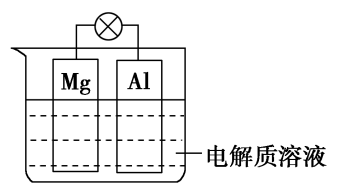
(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为____________ ;Al电极上发生的反应为________ 。溶液中 向
向________ 移动(填“Mg电极”或“Al电极”)
(2)电解质溶液为NaOH溶液时,灯泡________ (填“亮”或“不亮”,填“亮”做a题,填“不亮”做b题)。_______________
a.若灯泡亮,Al电极为_______________(填“正极”或“负极”)。
b.若灯泡不亮,其理由为__________________。

(1)电解质溶液为稀硫酸时,灯泡亮,Mg电极上发生的反应为
 向
向(2)电解质溶液为NaOH溶液时,灯泡
a.若灯泡亮,Al电极为_______________(填“正极”或“负极”)。
b.若灯泡不亮,其理由为__________________。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学原理在能量转换、金属冶炼等方面应用广泛。
(1)图①是碱性锌锰电池,在负极发生反应的物质是___________ (填“Zn”或“ ”),正极发生
”),正极发生___________ 反应(填“氧化”或“还原”)。

(2)图②是碱性电解质的氢氧燃料电池,B极通入的气体为___________ ,B极发生的电极反应式___________ 。

(3)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为: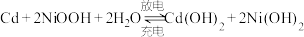 ,充电时,阳极的电极反应式为
,充电时,阳极的电极反应式为___________ ;当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性___________ (填“增强”“减弱”或“不变”)。紧急状况下,应急电池会自动启动,工作原理为 ,其负极的电极反应式为
,其负极的电极反应式为___________ 。
(4)利用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: 。则
。则 在
在___________ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为___________ 。

(1)图①是碱性锌锰电池,在负极发生反应的物质是
 ”),正极发生
”),正极发生
(2)图②是碱性电解质的氢氧燃料电池,B极通入的气体为

(3)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。其工作原理为:
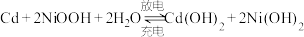 ,充电时,阳极的电极反应式为
,充电时,阳极的电极反应式为 ,其负极的电极反应式为
,其负极的电极反应式为(4)利用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: 。则
。则 在
在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列电解池均以石墨为电极,溶液体积为100mL,浓度均为2mol/L,通电一段时间后,甲池的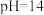 ,请回答以下问题:
,请回答以下问题:

(1)电解化学方程式为:甲___________ 乙___________
(2)四个电解池生成气体的总体积为___________ (标况)
(3)四个电解池在相同时间内生成气体的物质的量在理论上由多到少的顺序是___________
(4)电解一段时间后,要恢复原溶液,向四个电解池中分别加入甲___________ 乙___________ 丙___________ 丁___________
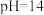 ,请回答以下问题:
,请回答以下问题:
(1)电解化学方程式为:甲
(2)四个电解池生成气体的总体积为
(3)四个电解池在相同时间内生成气体的物质的量在理论上由多到少的顺序是
(4)电解一段时间后,要恢复原溶液,向四个电解池中分别加入甲
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)丙池中E电极为_______ (填“正极”、“负极”、“阴极”或“阳极”)
(2)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为_______ mL(标况)。
(3)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______ (填选项字母)。
(4)爱迪生蓄电池的反应式为:Fe+NiO2+2H2O=Fe(OH)2+Ni(OH)2;高铁酸钠(Na2FeO4)易溶于水,是一种新型净水剂。用如图装置可以制取少量高铁酸钠。

①此装置中爱迪生蓄电池的正极是_______ (填“a“或"b"),该电池工作一段时间后必须充电,充电时阴极的电极反应式为_______ 。
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为_______ 。

(1)丙池中E电极为
(2)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为
(3)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是_______ (填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |

①此装置中爱迪生蓄电池的正极是
②写出在用电解法制取高铁酸钠时,阳极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图是一个电化学过程的示意图,回答下列问题:
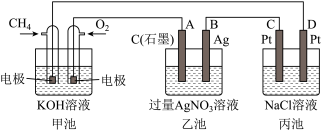
(1)甲池将__________ 能转化为__________ 能,乙装置中电极A是__________ 极。
(2)甲装置中通入CH4一极的电极反应式为__________
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=__________ (已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入__________ (写化学式)。

(1)甲池将
(2)甲装置中通入CH4一极的电极反应式为
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25℃时的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用如图所示装置电解硝酸银溶液和硫酸钠溶液(甲中盛有AgNO3溶液,乙中盛有Na2SO4溶液)。
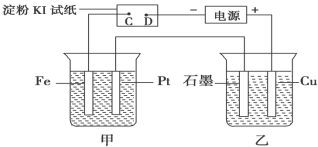
(1)通电一段时间,观察到湿润的淀粉KI试纸的___________ (填“C”或“D”)端先变蓝。
(2)装置甲中阳极为___________ ,阴极的电极反应式为___________ 。
(3)装置乙中观察到的现象是___________ 。
(4)电解一段时间后,装置甲、乙中共收集到气体0.168 L(标准状况下),测得装置甲中溶液的体积为1 L,则装置甲中溶液的pH为___________ 。

(1)通电一段时间,观察到湿润的淀粉KI试纸的
(2)装置甲中阳极为
(3)装置乙中观察到的现象是
(4)电解一段时间后,装置甲、乙中共收集到气体0.168 L(标准状况下),测得装置甲中溶液的体积为1 L,则装置甲中溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将两支惰性电极插入500mLAgNO3溶液中,通电电解,当电解液的pH由6.0变为3.0时(设电解时阴极没有氢析出,且电解液在电解前后体积变化可以忽略)。
(1)写出电极反应式阳极:___________________________ ,
阴极:_________________________________________ 。
(2)电极上应析出银的质量是_________________________ 。
(3)欲使该溶液复原应加入___________________________ 。
(1)写出电极反应式阳极:
阴极:
(2)电极上应析出银的质量是
(3)欲使该溶液复原应加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如图所示:

①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极应连接电源的_______ (填“正极”或“负极”),对应的电极反应式为_______ 。
②a极区pH_______ (填“增大”“减小”或“不变”)。
③图中应使用_______ (填“阴”或“阳”)离子交换膜。
(2)电解硝酸工业的尾气NO可制备NH4NO3(NH4NO3溶液显酸性),其工作原理如图所示:
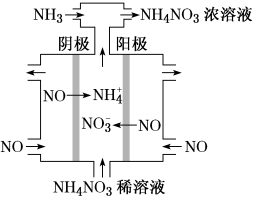
①阴极的电极反应式为_______ 。
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为_______ 。
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如图所示:

①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极应连接电源的
②a极区pH
③图中应使用
(2)电解硝酸工业的尾气NO可制备NH4NO3(NH4NO3溶液显酸性),其工作原理如图所示:

①阴极的电极反应式为
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)在含有AlO2—溶液中通入足量CO2,写出反应的离子方程式____________
(2)Al2O3在碳的还原作用下生成铝的气态低价氧化物X (X中Al与O的质量比为6.75∶2)则X的化学式为_________ 。
(3)三氟化氮(NF3)是一种无色、无臭的气体。三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,反应产物中生成酸M、酸N和一种无色气体(遇空气变成红棕色),其中酸M是一种弱酸,酸N为常见的含氧强酸。
① 写出该反应的化学方程式_________ 。
② 酸M是弱酸(难电离)的原因是____________
③一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO3、NaF等盐外,还可以生成的盐是____________ (填化学式)。
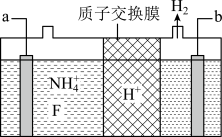
④在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。写出a电极的电极反应式________ 。
(2)Al2O3在碳的还原作用下生成铝的气态低价氧化物X (X中Al与O的质量比为6.75∶2)则X的化学式为
(3)三氟化氮(NF3)是一种无色、无臭的气体。三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,反应产物中生成酸M、酸N和一种无色气体(遇空气变成红棕色),其中酸M是一种弱酸,酸N为常见的含氧强酸。
① 写出该反应的化学方程式
② 酸M是弱酸(难电离)的原因是
③一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO3、NaF等盐外,还可以生成的盐是
④在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。写出a电极的电极反应式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在如图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16g。试回答:

(1)电源中Y电极为直流电源的__________ 极。
(2)pH变化:A:________ B:________ (填“增大”、“减小”或“不变”)。
(3) 若A中KCl溶液的体积是200 mL,电解后,溶液的pH为__________ (设电解前后溶液体积无变化)。
(4)B中电解CuSO4溶液的电极总反应:_______________________________________

(1)电源中Y电极为直流电源的
(2)pH变化:A:
(3) 若A中KCl溶液的体积是200 mL,电解后,溶液的pH为
(4)B中电解CuSO4溶液的电极总反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】利用电化学装置可消除氮氧化物(如 NO、NO 、NO
、NO 尿素等)污染,变废为宝。
尿素等)污染,变废为宝。
(1)下图为电解 NO制备NH4NO3 的装置。该装置中阴极的电极反应式为___________ ;“反应室”中发生反应的离子方程式为___________ 。

(2)化学家正在研究尿素[CO(NH2)2]动力燃料电池直接去除城市废水中的尿素,既能产生净化的水, 又能发电,尿素燃料电池结构如图所示:
甲电极的电极反应式为___________ ;乙电极的电极反应式为___________ 。理论上每净化 1mol尿素, 消耗O2的体积约为___________ L(标准状况)。
(3)工业上用电解法治理亚硝酸盐 NO
NO 具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:
具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:___________ 。 随后, 铁电极附近有无色气体产生,可能原因是___________ 。

(4)某乙烯熔融碳酸盐燃料电池工作原理如图所示,若要维持电池持续稳定工作,则从理论上讲,进入石墨Ⅱ电极上的CO2与石墨I电极上生成的CO2的物质的量之比是___________ 。

 、NO
、NO 尿素等)污染,变废为宝。
尿素等)污染,变废为宝。(1)下图为电解 NO制备NH4NO3 的装置。该装置中阴极的电极反应式为

(2)化学家正在研究尿素[CO(NH2)2]动力燃料电池直接去除城市废水中的尿素,既能产生净化的水, 又能发电,尿素燃料电池结构如图所示:
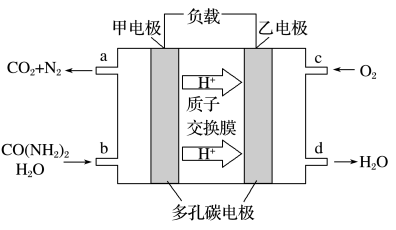
甲电极的电极反应式为
(3)工业上用电解法治理亚硝酸盐
 NO
NO 具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:
具有强氧化性)对水体的污染,模拟工艺如下图所示,写出电解时铁电极的电极反应式:
(4)某乙烯熔融碳酸盐燃料电池工作原理如图所示,若要维持电池持续稳定工作,则从理论上讲,进入石墨Ⅱ电极上的CO2与石墨I电极上生成的CO2的物质的量之比是

您最近一年使用:0次



