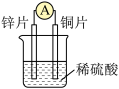
回答下列问题
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O + Zn + H2O = 2Ag + Zn(OH)2
①工作时电子从___________ 极流向___________ 极(填“Ag2O”或“Zn”)。
②工作时电池正极区的pH___________ (填“增大”、“减小”或“不变”)。
③请写出负极的电极反应式:___________ 。
(2)家用液化气中主要成分之一是丁烷。 当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50 kJ。试写出丁烷燃烧的热化学方程式:___________ 。
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O + Zn + H2O = 2Ag + Zn(OH)2
①工作时电子从
②工作时电池正极区的pH
③请写出负极的电极反应式:
(2)家用液化气中主要成分之一是丁烷。 当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50 kJ。试写出丁烷燃烧的热化学方程式:
更新时间:2022-05-22 16:22:05
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)家用液化气的主要成分之一是丁烷,当58g丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为2900kJ,试写出表示丁烷燃烧热的热化学方程式:__________________ ;
(2)稀盐酸和NaOH稀溶液反应生成1mol水放热57.3KJ, 该反应的热化学方程式为_______________________________________________ 。
(2)稀盐酸和NaOH稀溶液反应生成1mol水放热57.3KJ, 该反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗) SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)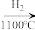 Si(纯)
Si(纯)
写出SiCl4的电子式:________ ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___________________________ 。
(2)CuCl(s)和O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗1molCuCl(s),放热44.4kJ,该反应的热化学方程式是____________________ 。
(3)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
由上述方程式可知:CH3OH的燃烧热________ (填“大于”“等于”或“小于”)192.9kJ/mol。已知水的气化热为44kJ/mol。则表示氢气燃烧热的热化学方程式为__________________ 。
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101kPa下:
①H2(g)+ O2(g)=H2O(g) ΔH1=-242 kJ/mol
O2(g)=H2O(g) ΔH1=-242 kJ/mol
②CH3OH(g)+ O2(g)=CO2(g)+2H2O(g) ΔH2=-676 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2=-676 kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____________________ 。
(5)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=+64 kJ/mol
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196 kJ/mol
③H2(g)+ O2(g)=H2O(l) ΔH3=-285 kJ/mol
O2(g)=H2O(l) ΔH3=-285 kJ/mol
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为__________________ 。
Si(粗)
 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)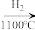 Si(纯)
Si(纯)写出SiCl4的电子式:
(2)CuCl(s)和O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗1molCuCl(s),放热44.4kJ,该反应的热化学方程式是
(3)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol由上述方程式可知:CH3OH的燃烧热
(4)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃、101kPa下:
①H2(g)+
 O2(g)=H2O(g) ΔH1=-242 kJ/mol
O2(g)=H2O(g) ΔH1=-242 kJ/mol②CH3OH(g)+
 O2(g)=CO2(g)+2H2O(g) ΔH2=-676 kJ/mol
O2(g)=CO2(g)+2H2O(g) ΔH2=-676 kJ/mol写出CO2和H2生成气态甲醇等产物的热化学方程式
(5)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=+64 kJ/mol
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196 kJ/mol
③H2(g)+
 O2(g)=H2O(l) ΔH3=-285 kJ/mol
O2(g)=H2O(l) ΔH3=-285 kJ/mol在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是 和
和 反应生成
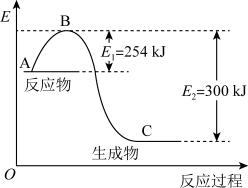
反应生成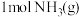 过程中能量的变化示意图,该化学反应属于
过程中能量的变化示意图,该化学反应属于___________ (放热或吸热)反应,正反应的活化能为___________ ,写出该反应的热化学方程式:___________ 。
(2)上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为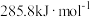 ,请写出氢气燃烧热的热化学方程式:
,请写出氢气燃烧热的热化学方程式:________ 。已知 转化成
转化成 吸收
吸收 的热量,
的热量,________ 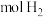 完全燃烧生成气态水可以放出
完全燃烧生成气态水可以放出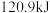 的热量(不可虑热量损失)。
的热量(不可虑热量损失)。

(1)如图是
 和
和 反应生成
反应生成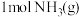 过程中能量的变化示意图,该化学反应属于
过程中能量的变化示意图,该化学反应属于(2)上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为
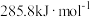 ,请写出氢气燃烧热的热化学方程式:
,请写出氢气燃烧热的热化学方程式: 转化成
转化成 吸收
吸收 的热量,
的热量,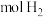 完全燃烧生成气态水可以放出
完全燃烧生成气态水可以放出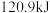 的热量(不可虑热量损失)。
的热量(不可虑热量损失)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】开发新能源是解决大气污染的有效途径之一、直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如下图所示,通入a气体的电极是原电池的___________ 极(填“正”或“负”),其电极反应式为___________ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是___ ;电解质溶液Y是__ 。
(2)银电极为电池的___ 极,发生的电极反应为____ 。X电极上发生的电极反应为__ 。外电路中的电子是从___ 极流向___ 极。
(3)此盐桥内为含琼胶的饱和KCl溶液,盐桥是通过__ 移动来导电的。在工作时,K+移向__ (填“正极区”或“负极区”,下同),Cl-移向__ ,盐桥的作用是_____ 。

请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)此盐桥内为含琼胶的饱和KCl溶液,盐桥是通过
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】请回答下列问题。
(1)在原电池中,通常较活泼的金属做_____ 极,发生_______ 反应;
电解池中,与电源正极相连的极是_______ 极,发生________ 反应。
(2)下图所示水槽中试管内有一枚铁钉,放置数天后观察:
①若试管内液面上升,发生_____ 腐蚀,正极反应式为________________ 。
②若试管内液面下降,发生_______ 腐蚀,正极反应式为_______________ 。
(1)在原电池中,通常较活泼的金属做
电解池中,与电源正极相连的极是
(2)下图所示水槽中试管内有一枚铁钉,放置数天后观察:

①若试管内液面上升,发生
②若试管内液面下降,发生
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应式为_______ 。 一种可超快充电的新型铝电池,充放电时AlC 和Al2C
和Al2C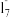 两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为
两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为_______ 。
 和Al2C
和Al2C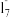 两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为
两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)在下图的8个装置中,属于原电池的是____________ 。

(2)铅蓄电池的正极材料是_________ 。
(3)航天飞机常采用燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。如图是甲烷燃料电池原理示意图,回答下列问题:
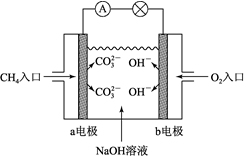
①电池的负极是___ (填“a”或“b”),该极的电极反应是_________ 。
②消耗标准状况下5.6L O2时,有____ mol电子发生转移。
③开始放电时,正极附近溶液的pH__________ (填“增大”“减小”或“不变”)

(2)铅蓄电池的正极材料是
(3)航天飞机常采用燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是
②消耗标准状况下5.6L O2时,有
③开始放电时,正极附近溶液的pH
您最近一年使用:0次