硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产,其中一步反应原理为 ,该反应为放热反应,下列有关说法正确的是
,该反应为放热反应,下列有关说法正确的是
 ,该反应为放热反应,下列有关说法正确的是
,该反应为放热反应,下列有关说法正确的是A.只要选择适宜的条件, 和 和 就能全部转化为 就能全部转化为 |
| B.升高温度会使正逆反应速率都加快 |
C.由反应可知, 的能量大于 的能量大于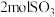 的能量 的能量 |
D.在达到平衡的体系中,充入由 原子组成的 原子组成的 后, 后, 仅存在于 仅存在于 和 和 中 中 |
更新时间:2022-05-14 09:29:28
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】对于反应Zn + H2SO4 = ZnSO4+ H2↑,下列叙述正确的是


| A.反应过程中的能量关系可用如图表示 |
| B.1mol Zn的能量大于1 molH2的能量 |
| C.若将其设计为原电池,则锌作正极 |
| D.若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】对于化学反应中的能量变化,表述正确的是
| A.需要加热的化学反应都是吸热反应 |
| B.中和反应都是放热反应 |
| C.浓硫酸溶于水为放热反应 |
| D.反应中旧键断裂放出的能量大于新键形成吸收的能量时,反应为放热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列四种酸与锌片反应,起始时生成H2反应速率最大的是
| A.10 ℃ 20 mL 3 mol/L的盐酸 | B.10 ℃ 40 mL 2 mol/L的醋酸 |
| C.20 ℃ 20 mL 2 mol/L的硫酸 | D.20 ℃ 10 mL 4 mol/L的硝酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关化学反应速率的说法中,正确的是
| A.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |
| B.用铁片和稀硫酸反应制取H2时,改用铁片和浓硫酸可以加快产生H2的速率 |
| C.二氧化硫的催化氧化反应是一个放热反应,所以升高温度,反应速率减慢 |
| D.100mL2mol·L-1的盐酸与锌反应时,加入适量的NaCl溶液,生成H2的速率不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是
| A.反应混合物的浓度 | B.反应物的转化率 |
| C.正、逆反应的速率 | D.反应体系的压强 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关化学反应限度的说法正确的是
| A.可逆反应达到平衡状态时,各反应物、生成物的浓度相等 |
| B.在一定条件下,一个可逆反应达到的平衡状态就是该反应所能达到的最大限度 |
| C.化学反应在一定条件下建立平衡状态时,化学反应将会停止 |
D.1mol 和 和 在一定条件下可完全生成 在一定条件下可完全生成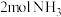 |
您最近一年使用:0次



 ,在一定条件下达到平衡,下列有关叙述正确的是
,在一定条件下达到平衡,下列有关叙述正确的是 的浓度不变
的浓度不变 的浓度,v(正)增大,v(逆)减小,平衡正向移动
的浓度,v(正)增大,v(逆)减小,平衡正向移动

