为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试回答下列问题:
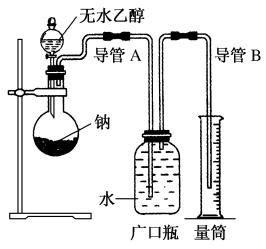
(1)指出实验装置中的错误:_______ 。
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将_______ (填“偏大”“偏小”或“不变”)。
(3)请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤):_______

(1)指出实验装置中的错误:
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将
(3)请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤):
2022高一·上海·专题练习 查看更多[1]
(已下线)7.3.1 乙醇-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
更新时间:2022-05-12 16:40:20
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】为了测定乙醇的结构式,利用乙醇和钠的反应,设计如图1装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。
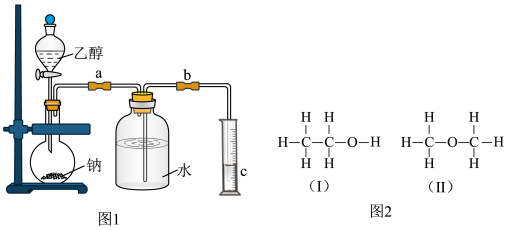
(1)实验前检验该装置的气密性的实验操作是__ 。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为__ (填“正确”或“不正确”)。
(3)若实验中所用乙醇含有少量水则实验结果将_ (填“偏大”或“偏小”),若实验开始前b导管内未充满水则实验结果将__ (填“偏大”或“偏小”)。
(4)若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确__ 。

(1)实验前检验该装置的气密性的实验操作是
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为
(3)若实验中所用乙醇含有少量水则实验结果将
(4)若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确
您最近一年使用:0次
【推荐1】A是化学实验室中最常见的有机物乙醇,俗名酒精,它易溶于水并有特殊香味,能进行如图所示的多种反应。

(1)写出D的分子式_____________________ 。
(2)发生反应①时钠在____________________ 。(填“液面上”或“液体底部”)。
(3)写出反应③的反应类型___________ 。
(4)下列关于化合物B的化学性质,说法正确的是__________ (填字母)。
A.化合物B可以与Cl2发生取代反应
B.化合物B可以与Cl2发生加成反应
C.化合物B可以使溴的四氯化碳溶液褪色
D.化合物B不可以使酸性高锰酸钾溶液褪色

(1)写出D的分子式
(2)发生反应①时钠在
(3)写出反应③的反应类型
(4)下列关于化合物B的化学性质,说法正确的是
A.化合物B可以与Cl2发生取代反应
B.化合物B可以与Cl2发生加成反应
C.化合物B可以使溴的四氯化碳溶液褪色
D.化合物B不可以使酸性高锰酸钾溶液褪色
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
【推荐2】A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。
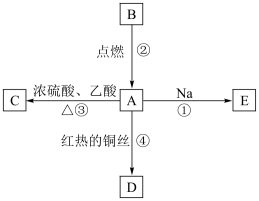
(1)写出A的化学式___________ 。
(2)写出下列反应的化学方程式:反应①___________ ;反应②___________ ;反应③___________ 反应④___________ 。

(1)写出A的化学式
(2)写出下列反应的化学方程式:反应①
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学活动小组欲利用乙醇与金属钠的反应测定乙醇中的活性氢原子个数,并验证乙醇的部分化学性质,设计了如下实验。回答下列问题:
Ⅰ.用如图1装置来推测乙醇分子中活性氢原子的个数;___________ ;
(2)若使用的圆底烧瓶未进行干燥,含有少量水(钠过量),则收集到氢气的体积___________ (填“偏大”、“偏小”或“无影响”);
(3)已知无水乙醇的密度为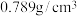 ,移取
,移取 乙醇,反应完全后(钠过量),当收集到标准状况下约
乙醇,反应完全后(钠过量),当收集到标准状况下约___________ (填整数) 的气体时,可证明一个乙醇分子中活性氢原子的个数为1。
的气体时,可证明一个乙醇分子中活性氢原子的个数为1。
Ⅱ.利用图2装置进行乙醇的催化氧化实验.已知:乙醛可进一步被氧化为乙酸____________________ ;
(5)装入实验药品后,打开活塞a、b、c,在铜丝的中间部分加热,通过控制活塞a和b,间歇性地通入氧气,即可在M处观察到受热部分的铜丝______________ (填实验现象);写出乙醇催化氧化的化学反应方程式______________ 。
Ⅰ.用如图1装置来推测乙醇分子中活性氢原子的个数;
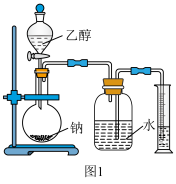
(2)若使用的圆底烧瓶未进行干燥,含有少量水(钠过量),则收集到氢气的体积
(3)已知无水乙醇的密度为
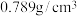 ,移取
,移取 乙醇,反应完全后(钠过量),当收集到标准状况下约
乙醇,反应完全后(钠过量),当收集到标准状况下约 的气体时,可证明一个乙醇分子中活性氢原子的个数为1。
的气体时,可证明一个乙醇分子中活性氢原子的个数为1。Ⅱ.利用图2装置进行乙醇的催化氧化实验.已知:乙醛可进一步被氧化为乙酸

(5)装入实验药品后,打开活塞a、b、c,在铜丝的中间部分加热,通过控制活塞a和b,间歇性地通入氧气,即可在M处观察到受热部分的铜丝
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
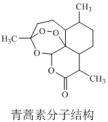
【推荐1】我国科学家屠呦呦因成功从黄花蒿中提取青蒿素而获得2015年诺贝尔奖。青蒿素是治疗疟疾的有效药物,属于酯类化合物,其分子结构如图所示。
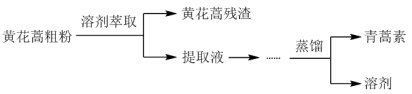
(1)从黄花蒿中提取青蒿素的流程如下:
研究团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
①分离黄花蒿残渣与提取液的实验操作是_______ 。
②提取青蒿素使用的溶剂最好选择_______ 。
③研究发现,青蒿素分子中的某个基团受热不稳定,据此分析用乙醇作溶剂,提取效率偏低,不能达到理想效果的原因是_______ 。
④蒸馏操作中用到的玻璃仪器有:酒精灯、蒸馏烧瓶、_______ 、冷凝管、尾接管、锥形瓶。
(2)研究还发现,将青蒿素通过下面反应转化为双氢青蒿素,治疗疟疾的效果更好。
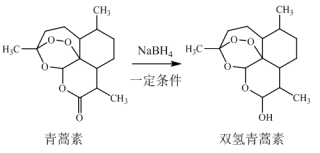
①该反应的反应类型是_______ 。
②从分子结构与物理性质的关系角度推测双氢青蒿素疗效更好的原因_______ 。
(3)提取并转化青蒿素治疗疟疾的过程中,应考虑物质的_______ 、_______ 等性质。

(1)从黄花蒿中提取青蒿素的流程如下:

研究团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
| 溶剂 | 水 | 乙醇 | 乙醚 |
| 沸点/℃ | 100 | 78 | 35 |
| 提取效率 | 几乎为0 | 35% | 95% |
②提取青蒿素使用的溶剂最好选择
③研究发现,青蒿素分子中的某个基团受热不稳定,据此分析用乙醇作溶剂,提取效率偏低,不能达到理想效果的原因是
④蒸馏操作中用到的玻璃仪器有:酒精灯、蒸馏烧瓶、
(2)研究还发现,将青蒿素通过下面反应转化为双氢青蒿素,治疗疟疾的效果更好。

①该反应的反应类型是
②从分子结构与物理性质的关系角度推测双氢青蒿素疗效更好的原因
(3)提取并转化青蒿素治疗疟疾的过程中,应考虑物质的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和_______ ,原因是_______ ,对应的离子方程式_______ 。
(2)除去蒸馏水中溶解的O2常采用_______ 的方法。
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为_______
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是_______ 。
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是_______ 。

(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和
(2)除去蒸馏水中溶解的O2常采用
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
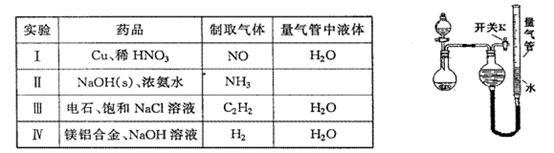
(1)如何检验如图所示装置的气密性:____________________________ 。
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?________ (填“可行”或“不可行”),原因是______________________ 。
(3)实验Ⅲ烧瓶中发生反应的化学方程式是___________________________________ ,打开开关K,产生的气体经验纯后点燃,现象是__________________________ 。
(4)实验Ⅱ中量气管中的液体最好是____ (填字母编号,下同)
a.浓NaOH溶液b.氨水c.煤油d.饱和氯化铵溶液
该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有_____________
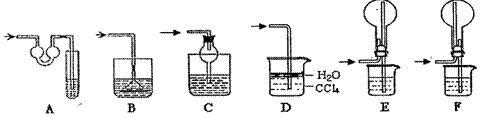
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②_____ ,③视线与凹液面最低处相平。
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
根据上述数据,可计算出镁铝合金中铝的质量分数为______________ 。

(1)如何检验如图所示装置的气密性:
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?
(3)实验Ⅲ烧瓶中发生反应的化学方程式是
(4)实验Ⅱ中量气管中的液体最好是
a.浓NaOH溶液b.氨水c.煤油d.饱和氯化铵溶液
该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有

(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②
(6)实验Ⅳ获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
您最近一年使用:0次

 有刺激性气味的产物
有刺激性气味的产物

