为了测定乙醇的结构式,利用乙醇和钠的反应,设计如图1装置进行实验,在烧瓶中放入足量的钠,从分液漏斗中缓缓滴入一定量的乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积。__ 。
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为__ (填“正确”或“不正确”)。
(3)若实验中所用乙醇含有少量水则实验结果将_ (填“偏大”或“偏小”),若实验开始前b导管内未充满水则实验结果将__ (填“偏大”或“偏小”)。
(4)若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确__ 。
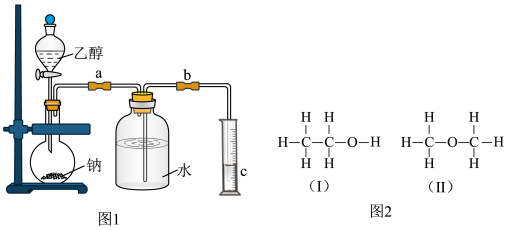
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为
(3)若实验中所用乙醇含有少量水则实验结果将
(4)若测得有1.15gC2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280mL,试结合计算和讨论,判断图2中(Ⅰ)和(Ⅱ)两式中,哪个正确
更新时间:2020/01/30 14:36:18
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试回答下列问题:
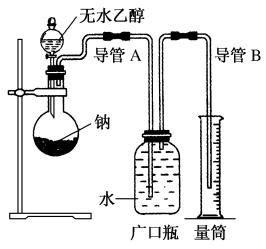
(1)指出实验装置中的错误:_______ 。
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将_______ (填“偏大”“偏小”或“不变”)。
(3)请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤):_______

(1)指出实验装置中的错误:
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将
(3)请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤):
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
解题方法
【推荐1】乙醇是生活中常见的有机物,能进行如下图所示的多种反应,A、C都是有机物。
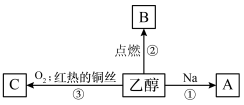
写出下列反应的化学方程式:
①______________________ ;
②_________________________ ;
③___________________________ 。

写出下列反应的化学方程式:
①
②
③
您最近一年使用:0次
【推荐2】A是化学实验室中最常见的有机物乙醇,俗名酒精,它易溶于水并有特殊香味,能进行如图所示的多种反应。

(1)写出D的分子式_____________________ 。
(2)发生反应①时钠在____________________ 。(填“液面上”或“液体底部”)。
(3)写出反应③的反应类型___________ 。
(4)下列关于化合物B的化学性质,说法正确的是__________ (填字母)。
A.化合物B可以与Cl2发生取代反应
B.化合物B可以与Cl2发生加成反应
C.化合物B可以使溴的四氯化碳溶液褪色
D.化合物B不可以使酸性高锰酸钾溶液褪色

(1)写出D的分子式
(2)发生反应①时钠在
(3)写出反应③的反应类型
(4)下列关于化合物B的化学性质,说法正确的是
A.化合物B可以与Cl2发生取代反应
B.化合物B可以与Cl2发生加成反应
C.化合物B可以使溴的四氯化碳溶液褪色
D.化合物B不可以使酸性高锰酸钾溶液褪色
您最近一年使用:0次
【推荐3】下表是有机物 A、B、C、D 的有关信息:
根据表中信息回答下列问题:
(1)写出B 的结构式_____ ;D 的官能团名称是_____ 。
(2)B 能使溴的四氯化碳溶液褪色,反应后生成物的名称_____ 。
(3)B→D 的化学反应类型为_____ 。
(4)D 催化氧化生成E 的化学方程式为_____ 。
(5)C 的分子式是_____ ,写出在浓硫酸作用下,C 在 50 ~60℃与浓硝酸发生反应的化学方程式:_____ 。
(6)与A 互为同系物的物质均符合通式 CnH2n+2,当 n=5 时,该有机物有_____ 种同分异构体, 其中碳链最短的同分异构体的结构简式是_____ 。
A | ①无色无味、难溶于水; ②最简单的有机化合物 | B | ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与水在一定条件下反应生成 D |
| C | ①由 C、H 两种元素组成; ②球棍模型为:  。 。 | D | ①能与钠反应,但不能与 NaOH 溶液反应; ②在催化剂条件下能被空气中的氧气氧化为 E |
(1)写出B 的结构式
(2)B 能使溴的四氯化碳溶液褪色,反应后生成物的名称
(3)B→D 的化学反应类型为
(4)D 催化氧化生成E 的化学方程式为
(5)C 的分子式是
(6)与A 互为同系物的物质均符合通式 CnH2n+2,当 n=5 时,该有机物有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学兴趣小组模拟工业生产无水FeCl3.利用如图所示装置向500-600℃的铁屑中通入Cl2生产无水FeCl3。
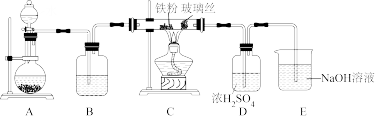
已知:FeCl3固体呈黑棕色、易潮解、易升华。回答下列问题:
(1)写出用KMnO4和浓盐酸在装置A中制备Cl2的离子方程式:_____ 。
(2)装置B中加入的试剂是_____ ,装置C中玻璃丝的作用是____ ,E中为碱液,其作用是_____ 。
(3)有同学认为气体通入装置C前应先除去其中含有的HCl,否则会影响所得FeCl3的纯度,对此你的观点是_____ 。
(4)已知FeCl3·6H2O晶体在水中的溶解度如下:
则从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是:加入少量盐酸、_____ 、_____ 、过滤、洗涤、干燥。
(5)FeCl3的质量分数通常可用碘量法测定:称取2.300g无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶中,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用0.1000mol·L-1Na2S2O3溶液滴定,消耗12.50mL标准液。已知:I2+2 =2I-+
=2I-+
①写出加入稍过量的KI溶液发生反应的离子方程式:______ 。
②样品中氯化铁的质量分数为_______ (保留一位小数)。

已知:FeCl3固体呈黑棕色、易潮解、易升华。回答下列问题:
(1)写出用KMnO4和浓盐酸在装置A中制备Cl2的离子方程式:
(2)装置B中加入的试剂是
(3)有同学认为气体通入装置C前应先除去其中含有的HCl,否则会影响所得FeCl3的纯度,对此你的观点是
(4)已知FeCl3·6H2O晶体在水中的溶解度如下:
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
(5)FeCl3的质量分数通常可用碘量法测定:称取2.300g无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶中,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用0.1000mol·L-1Na2S2O3溶液滴定,消耗12.50mL标准液。已知:I2+2
 =2I-+
=2I-+
①写出加入稍过量的KI溶液发生反应的离子方程式:
②样品中氯化铁的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】对羟基苯甲酸乙酯广泛用于食品、化妆品、医药等领域。某化学兴趣小组通过查阅文献制备对羟基苯甲酸乙酯。回答下列问题:
Ⅰ.对羟基苯甲酸乙酯的合成
实验原理: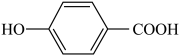 +CH3CH2OH
+CH3CH2OH
 +H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;
+H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;
实验步骤:取 乙醇和催化剂置于干燥的仪器A中,
乙醇和催化剂置于干燥的仪器A中, 对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
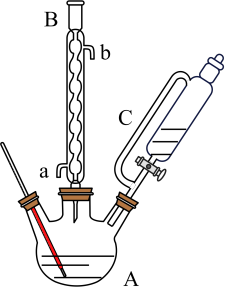
(1)仪器C的名称是____________________ ,仪器B的名称是____________________ 。
(2)某同学对实验装置做出了改进,在仪器A和B之间加一个脱水装置(如图),并在油水分离器(分水器)中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。
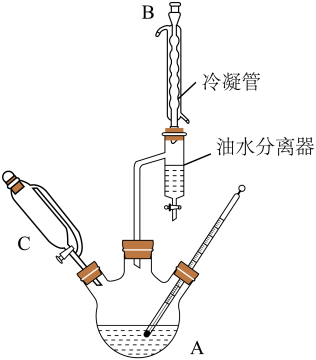
反应中利用分水器将水分去,该操作的目的是:____________________ 。
Ⅱ.对羟基苯甲酸乙酯的精制
实验方法:①反应完毕后趁热滤出催化剂,滤液倒入冷水中,析出固体,过滤。
②固体先后用5%的 溶液和水洗涤,干燥后得到粗产品。
溶液和水洗涤,干燥后得到粗产品。
③在装有冷凝管的圆底烧瓶中,按照一定比例加入粗品酯、乙醇、水和活性炭,加热回流0.5小时,趁热抽滤,滤液冷却,析出白色晶体,于80℃烘干。
(1)在②中用5%的 溶液洗涤的目的是
溶液洗涤的目的是_______ ,能不能用NaOH溶液替代?__________ (填“能”或“不能”)。
(2)在③趁热抽滤主要除去的杂质为___________ ,‘‘趁热”的目的是_________ 。
Ⅲ.该小组同学按0.1mol对羟基苯甲酸、0.4mol乙醇和催化剂2g进行投料,最后得到对羟基苯甲酸乙酯13.9g,则该实验的产率为____________________ 。
Ⅰ.对羟基苯甲酸乙酯的合成
实验原理:
 +CH3CH2OH
+CH3CH2OH
 +H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;
+H2O;对羟基苯甲酸摩尔质量为138g/mol,对羟基苯甲酸乙酯的摩尔质量为166g/mol;实验步骤:取
 乙醇和催化剂置于干燥的仪器A中,
乙醇和催化剂置于干燥的仪器A中, 对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
对羟基苯甲酸置于恒压滴液漏斗C中,实验装置如图所示(加热和夹持装置省略)。加热回流,充分反应。
(1)仪器C的名称是
(2)某同学对实验装置做出了改进,在仪器A和B之间加一个脱水装置(如图),并在油水分离器(分水器)中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。

反应中利用分水器将水分去,该操作的目的是:
Ⅱ.对羟基苯甲酸乙酯的精制
实验方法:①反应完毕后趁热滤出催化剂,滤液倒入冷水中,析出固体,过滤。
②固体先后用5%的
 溶液和水洗涤,干燥后得到粗产品。
溶液和水洗涤,干燥后得到粗产品。③在装有冷凝管的圆底烧瓶中,按照一定比例加入粗品酯、乙醇、水和活性炭,加热回流0.5小时,趁热抽滤,滤液冷却,析出白色晶体,于80℃烘干。
(1)在②中用5%的
 溶液洗涤的目的是
溶液洗涤的目的是(2)在③趁热抽滤主要除去的杂质为
Ⅲ.该小组同学按0.1mol对羟基苯甲酸、0.4mol乙醇和催化剂2g进行投料,最后得到对羟基苯甲酸乙酯13.9g,则该实验的产率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】有两位同学同时进行蔗糖的性质实验,并检验水解产物中是否含有葡萄糖。请回答下列问题:
(1)甲的操作如下:取少量蔗糖加适量水配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟,冷却;在冷却后的溶液中加入银氨溶液,水浴加热。实验结果是没有银镜产生,其原因是___ (填字母)。
A.蔗糖尚未水解
B.加热时间不够
C.煮沸后的溶液中没有加碱中和作催化剂的酸
D.蔗糖水解的产物中没有葡萄糖
(2)乙的操作:将蔗糖溶液与稀 共沸后,向溶液中加入新制
共沸后,向溶液中加入新制 悬浊液,加热至沸腾,一直未见砖红色沉淀产生,其原因是
悬浊液,加热至沸腾,一直未见砖红色沉淀产生,其原因是_______ 。
(3)检验蔗糖无还原性但水解产物有还原性,应选用的物质是_______ (填字母)。
A.新制的氢氧化铜悬浊液、稀硫酸 B.银氨溶液、稀硫酸、氢氧化钠溶液
C.银氨溶液、氢氧化钠溶液 D.新制的氢氧化铜悬浊液、氢氧化钠溶液
(4)两个同学都没有将实验做成功,原因是多方面的。你认为甲同学应该如何操作才能获得成功?______________
(1)甲的操作如下:取少量蔗糖加适量水配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟,冷却;在冷却后的溶液中加入银氨溶液,水浴加热。实验结果是没有银镜产生,其原因是
A.蔗糖尚未水解
B.加热时间不够
C.煮沸后的溶液中没有加碱中和作催化剂的酸
D.蔗糖水解的产物中没有葡萄糖
(2)乙的操作:将蔗糖溶液与稀
 共沸后,向溶液中加入新制
共沸后,向溶液中加入新制 悬浊液,加热至沸腾,一直未见砖红色沉淀产生,其原因是
悬浊液,加热至沸腾,一直未见砖红色沉淀产生,其原因是(3)检验蔗糖无还原性但水解产物有还原性,应选用的物质是
A.新制的氢氧化铜悬浊液、稀硫酸 B.银氨溶液、稀硫酸、氢氧化钠溶液
C.银氨溶液、氢氧化钠溶液 D.新制的氢氧化铜悬浊液、氢氧化钠溶液
(4)两个同学都没有将实验做成功,原因是多方面的。你认为甲同学应该如何操作才能获得成功?
您最近一年使用:0次

 有刺激性气味的产物
有刺激性气味的产物

