某化学小组为了探究原电池的基本原理,设计装置如图。下列相关分析错误的是
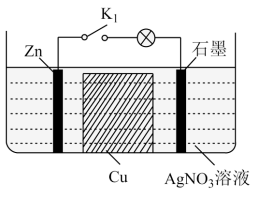

| A.电池工作时,石墨电极发生反应:Ag++e-=Ag |
| B.电池中Cu块取出前后灯泡亮度会发生变化 |
| C.一段时间后铜块无明显变化 |
| D.Zn为该电池的负极,发生氧化反应 |
更新时间:2022-05-17 21:23:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一种新型AC/LiMn2O4体系,在快速启动、电动车等领域具有广阔应用前景。其采用尖晶石结构的LiMn2O4作正极(可由Li2CO3和MnO2按物质的量比1:2反应合成),高比表面积活性炭AC(石墨颗粒组成)作负极,Li2SO4作电解液,充电、放电的过程如图所示:

| A.合成LiMn2O4的过程中可能有O2产生 |
| B.放电时正极的电极反应式为:LiMn2O4+xe- = Li(1-x)Mn2O4+xLi+ |
| C.充电时AC极应与电源正极相连 |
| D.可以用Na2SO4代替Li2SO4作电解液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】被称为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。总反应的化学方程式为:Zn+2MnO2+H2O=Zn(OH)2+Mn2O3,下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.电池正极的电极反应式为:2MnO2+H2O+2e-= Mn2O3+2OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
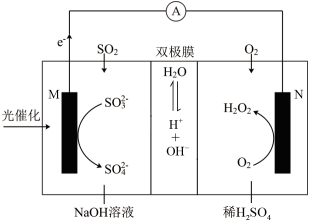
【推荐1】我国科研人员将单独脱除 反应与制备
反应与制备 反应相结合,实现协同转化(装置如图)。
反应相结合,实现协同转化(装置如图)。
已知:①单独脱除 反应
反应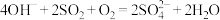 能自发进行;②单独制备
能自发进行;②单独制备 反应
反应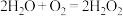 不能自发进行;③双极膜复合层间
不能自发进行;③双极膜复合层间 能解离为
能解离为 和
和 ,且能实现
,且能实现 和
和 向两极迁移。下列说法错误的是
向两极迁移。下列说法错误的是
 反应与制备
反应与制备 反应相结合,实现协同转化(装置如图)。
反应相结合,实现协同转化(装置如图)。已知:①单独脱除
 反应
反应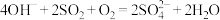 能自发进行;②单独制备
能自发进行;②单独制备 反应
反应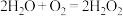 不能自发进行;③双极膜复合层间
不能自发进行;③双极膜复合层间 能解离为
能解离为 和
和 ,且能实现
,且能实现 和
和 向两极迁移。下列说法错误的是
向两极迁移。下列说法错误的是
| A.反应①释放的能量可以用于反应② |
B. 移向N极区域,反应过程中无需补加 移向N极区域,反应过程中无需补加 |
C.M为负极,该区域存在反应 |
D.每生成 ,M极区域溶液的质量增加 ,M极区域溶液的质量增加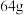 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
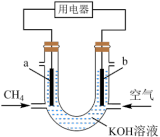
【推荐2】用一种新型H2O2液态燃料电池(乙池)电解催化氮气制备铵盐和硝酸盐(甲池)的工作原理示意图如下(c、d均为石墨电极)。下列说法正确的是
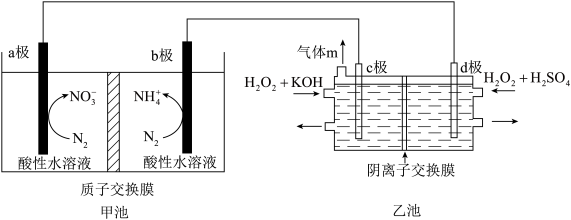

| A.乙池中若生成15molm气体,则甲池a、b两极共消耗8molN2 |
| B.甲池中H+从b极区通过质子交换膜转移至a极区 |
| C.一段时间后,乙池中c电极区的pH增大 |
D.甲池a极反应式为:N2+12OH--10e-=2 +6H2O +6H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】碱性锌锰干电池是生活中应用最广泛的电池,下列说法中不正确的是
| A.该电池正极反应式为:MnO2+H2O+e-=MnOOH+OH- |
| B.电池工作时负极pH降低 |
| C.用该电池作电源精炼铜,纯铜与锌连接 |
| D.用该电池作电源电解硫酸铜溶液,负极溶解6.5 g锌,阴极析出0.2 g H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学合成具有反应条件温和、反应试剂纯净和生产效率高等优点,利用下图所示装置可合成己二腈[NC(CH2)4CN]。充电时生成己二腈,放电时生成O2,其中a、b是互为反置的双极膜,双极膜中的H2O会解离出H+和OH-向两极移动。下列说法正确的是。
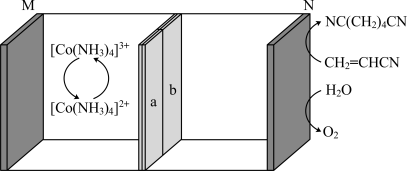

| A.放电时,M极作正极,电极反应式为[Co(NH3)4]3++e-=[Co(NH3)4]2+ |
| B.放电时,双极膜中H+向N极移动 |
| C.充电时,阳极的电极反应式为2CH2=CHCN+2e-+2H+=NC(CH2)4CN |
| D.若充电时制得1molNC(CH2)4CN,则放电时需生成1molO2,才能使左室溶液恢复至初始状态 |
您最近一年使用:0次

 +5H2O
+5H2O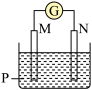
 的有机离子液体(有机离子不参与反应),放电时泡沫石墨电极中释放
的有机离子液体(有机离子不参与反应),放电时泡沫石墨电极中释放



