如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
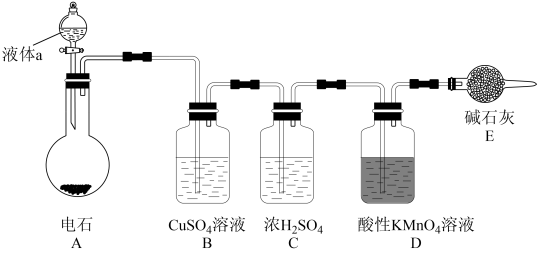
(1)写出实验室制取乙炔的化学方程式_______ 。
(2)实验室制取乙炔时,分液漏斗中的液体a通常是_______ 。
(3)装置D中的现象是_______ 。
(4)若D装置中药品为溴水,其生成四溴代物的反应方程式为:_______ 。

(1)写出实验室制取乙炔的化学方程式
(2)实验室制取乙炔时,分液漏斗中的液体a通常是
(3)装置D中的现象是
(4)若D装置中药品为溴水,其生成四溴代物的反应方程式为:
更新时间:2022-05-19 22:08:44
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
【推荐1】C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:

(1)写出A的电子式_______________ ;
(2)写出碳化钙与水反应制取A的化学方程式________________ ;B→C的化学方程式________________ ,其反应类型为_______________ 。
(3)D还可以用石蜡油制取,石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。
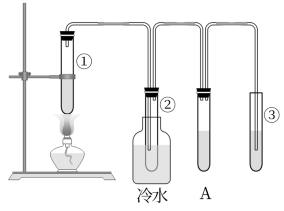
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(4)装置A的作用是__________________
(5)试管①中发生的主要反应有:C17H36 C8H18+C9H18;C8H18
C8H18+C9H18;C8H18 C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为
C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为_____________ 和____________ ,这两种有机物混合后在一定条件下其可能结构为____________ 。
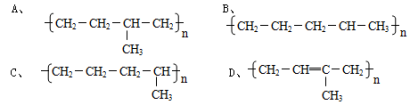
(6)写出试管③中反应的一个化学方程式_______________________ 。

(1)写出A的电子式
(2)写出碳化钙与水反应制取A的化学方程式
(3)D还可以用石蜡油制取,石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。

实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(4)装置A的作用是
(5)试管①中发生的主要反应有:C17H36
 C8H18+C9H18;C8H18
C8H18+C9H18;C8H18 C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为
C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为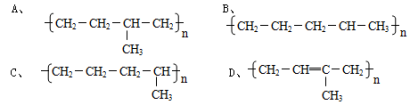
(6)写出试管③中反应的一个化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】近年来,由于石油价格上涨,以煤为原料制备一些化工产品的前景又被看好。如图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。
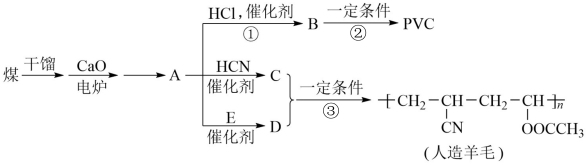
请回答下列问题:
(1)A的结构中含有三键,则A的结构式为_____ ,B的结构简式为____ 。
(2)写出反应类型:反应①____ ,反应③____ 。
(3)PVC的链节为____ ,写出B生成PVC的化学方程式:____ 。
(4)已知D的结构简式为CH2=CHOOCCH3,则E的结构简式为____ 。
(5)反应③中C、D两种单体按…CDCDCD…方式加聚,则C和D生成人造羊毛的化学方程式为____ 。

请回答下列问题:
(1)A的结构中含有三键,则A的结构式为
(2)写出反应类型:反应①
(3)PVC的链节为
(4)已知D的结构简式为CH2=CHOOCCH3,则E的结构简式为
(5)反应③中C、D两种单体按…CDCDCD…方式加聚,则C和D生成人造羊毛的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】用天然气、石油等可得到多种有机产品。
(1)从天然气获得的甲烷,甲烷用途广泛,工业上可用甲烷经下列变化制得CHFCl2 (氟利昂的一种主要成分):
CH4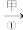 乙
乙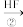 CHFCl2
CHFCl2
甲的分子式为_______ ;反应①、②都是取代反应,写出反应②的化学方程式_______ 。
(2)从石油炼制中获得的乙烯可以合成白色乳胶成分聚乙酸乙烯酯,合成路线如图:
乙烯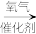 A(C2H4O)
A(C2H4O)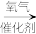 B(C2H4O2)
B(C2H4O2) C(C4H6O2)
C(C4H6O2)
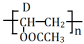
已知X分子为含碳量最大的气态烃,B是生活中常用的调味品。
请写出与A互为同系物且相对分子质量最小的有机物的结构简式_______ ;写出B转化为C的化学方程式_______ 。
(1)从天然气获得的甲烷,甲烷用途广泛,工业上可用甲烷经下列变化制得CHFCl2 (氟利昂的一种主要成分):
CH4
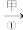 乙
乙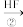 CHFCl2
CHFCl2甲的分子式为
(2)从石油炼制中获得的乙烯可以合成白色乳胶成分聚乙酸乙烯酯,合成路线如图:
乙烯
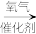 A(C2H4O)
A(C2H4O)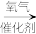 B(C2H4O2)
B(C2H4O2) C(C4H6O2)
C(C4H6O2)
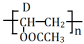
已知X分子为含碳量最大的气态烃,B是生活中常用的调味品。
请写出与A互为同系物且相对分子质量最小的有机物的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】在实验室利用如图装置,可制备某些气体并验证其化学性质。

(1)完成表格:
(2)实验①中,D装置中氢氧化钠溶液的作用是______ ,装置E中的现象是____ 。
(3)写出乙炔与溴水反应生成四溴代物的反应方程式______ 。

(1)完成表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| ① | 乙烯 | B→D→E | |
| ② | 乙炔 |
(3)写出乙炔与溴水反应生成四溴代物的反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
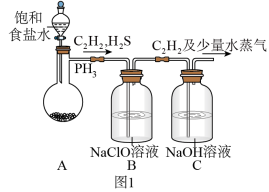
①装置A中用饱和食盐水代替水的目的是_____________ 。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为______ 。该过程中,可能产生新的杂质气体Cl2,其原因是:______ (用离子方程式回答)。
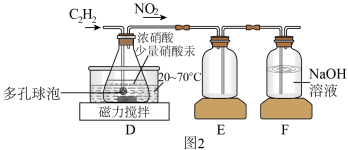
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是__________ 。
②装置D中生成H2C2O4的化学方程式为____________ 。
③从装置D中得到产品,还需经过___________ (填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是_____________ 。
②滴定过程中发现褪色速率开始很慢后逐渐加快,分析可能的原因是____________ 。
③产品中H2C2O4·2H2O的质量分数为_________ (列出含 m、c、V 的表达式)。
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。


①装置A中用饱和食盐水代替水的目的是
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是
②装置D中生成H2C2O4的化学方程式为
③从装置D中得到产品,还需经过
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是
②滴定过程中发现褪色速率开始很慢后逐渐加快,分析可能的原因是
③产品中H2C2O4·2H2O的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】乙炔(C2H2)是易燃气体,难溶于水。在实验室以电石(主要成分是CaC2)为原料制备乙炔,反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑,其装置如图所示:

已知:电石与水反应非常剧烈,饱和食盐水可以较大程度地降低反应速率。回答下列问题:
(1)仪器B的名称是_______ (填“圆底烧瓶”或“锥形瓶”)。
(2)要使B中反应速率降低,仪器A中应盛放的试剂是_______ (填“水”或“饱和食盐水”)。
(3)本实验收集乙炔所用的方法是_______ 。
(4)为除去乙炔中混有的少量H2S杂质,可将气体通过_______ (填字母)。
A.稀盐酸 B.NaOH溶液
(5)欲制得标准状况下2.24L C2H2,至少消耗H2O的质量为_______ g。

已知:电石与水反应非常剧烈,饱和食盐水可以较大程度地降低反应速率。回答下列问题:
(1)仪器B的名称是
(2)要使B中反应速率降低,仪器A中应盛放的试剂是
(3)本实验收集乙炔所用的方法是
(4)为除去乙炔中混有的少量H2S杂质,可将气体通过
A.稀盐酸 B.NaOH溶液
(5)欲制得标准状况下2.24L C2H2,至少消耗H2O的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】电石中的碳化钙和水能完全反应:CaC2+2H2O=C2H2↑+Ca(OH)2使反应产生的气体排水,测量排出水的体积,可计算出标准状况下乙炔的体积,从而可测定电石中碳化钙的含量。
(1)若用下列仪器和导管组装实验装置

如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:____ 接____ 接____ 接____ 接____ 接____ 。
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不产生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是__________________ 。
(3)若实验产生的气体有难闻气味,且测定结果偏大,这是因为电石中含有___________ 杂质。
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是_________ %。
(1)若用下列仪器和导管组装实验装置

如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞。
②检查装置的气密性。
③在仪器6和5中注入适量水。
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)。
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不产生气体时,关闭活塞。
正确的操作顺序(用操作编号填写)是
(3)若实验产生的气体有难闻气味,且测定结果偏大,这是因为电石中含有
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】如图装置可以用来制取某些气体.
(1)该装置可以制备乙炔气体,圆底烧瓶中盛放的物质是__________ (填电子式)分液漏斗中盛放的是______ ,目的是______________________________________ .
(2)实验室中制备乙炔的反应原理是______________________________________ .
(3)用此方法制取的乙炔气体通常混有H2S气体,如何除去?____ (填化学试剂)
(4)还能用该装置制备和收集的气体有(答出任意一种即可)______________ .
(5)若用来制备乙烯气体,需要对装置进行改进,将分液漏斗改成温度计,温度计的水银球放置的位置是_________ ,改进时还需要的玻璃仪器是_____________ .
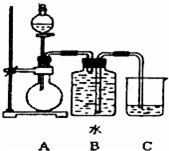
(1)该装置可以制备乙炔气体,圆底烧瓶中盛放的物质是
(2)实验室中制备乙炔的反应原理是
(3)用此方法制取的乙炔气体通常混有H2S气体,如何除去?
(4)还能用该装置制备和收集的气体有(答出任意一种即可)
(5)若用来制备乙烯气体,需要对装置进行改进,将分液漏斗改成温度计,温度计的水银球放置的位置是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】丙烯腈( )是合成纤维、合成橡胶和合成树脂的重要单体,可以由乙炔与HCN反应制得。原理如下
)是合成纤维、合成橡胶和合成树脂的重要单体,可以由乙炔与HCN反应制得。原理如下
I.制备催化剂
(1)通过查阅资料有两种方案可以制备
方案1:铜屑与 在浓盐酸中反应
在浓盐酸中反应
方案2:铜丝在氯气中燃烧
方案1的实验原理如图所示

①仪器a的名称___________ 。
②请写出方案1的反应原理___________ (用离子方程式表示)
(2)用恒压滴液漏斗分批多次滴加 ,且
,且 过量,原因是
过量,原因是___________ 。
(3)方案2燃烧后的固体溶于水,过滤后发现一些白色因体X,为检测X的成分,某同学将其溶于稀硫酸,白色固体变为红色,且溶液呈蓝色,推测X为___________ 。
II.合成丙烯腈
已知:①电石的主要成分是 ,还含有少量硫化钙
,还含有少量硫化钙
②HCN易挥发,有毒,具有较强的还原性
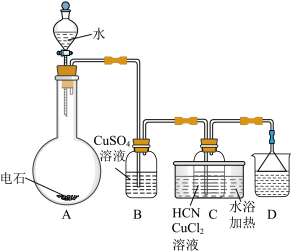
(4)HCN的电子式___________ 。
(5)纯净的乙炔是无色、无臭的气体。但用电石制取的乙炔时常伴有臭鸡蛋气味,这种物质是________ 。
(6)从下列选择装置D中可盛放的溶液___________
 )是合成纤维、合成橡胶和合成树脂的重要单体,可以由乙炔与HCN反应制得。原理如下
)是合成纤维、合成橡胶和合成树脂的重要单体,可以由乙炔与HCN反应制得。原理如下
I.制备催化剂

(1)通过查阅资料有两种方案可以制备
方案1:铜屑与
 在浓盐酸中反应
在浓盐酸中反应方案2:铜丝在氯气中燃烧
方案1的实验原理如图所示

①仪器a的名称
②请写出方案1的反应原理
(2)用恒压滴液漏斗分批多次滴加
 ,且
,且 过量,原因是
过量,原因是(3)方案2燃烧后的固体溶于水,过滤后发现一些白色因体X,为检测X的成分,某同学将其溶于稀硫酸,白色固体变为红色,且溶液呈蓝色,推测X为
II.合成丙烯腈
已知:①电石的主要成分是
 ,还含有少量硫化钙
,还含有少量硫化钙②HCN易挥发,有毒,具有较强的还原性

(4)HCN的电子式
(5)纯净的乙炔是无色、无臭的气体。但用电石制取的乙炔时常伴有臭鸡蛋气味,这种物质是
(6)从下列选择装置D中可盛放的溶液___________
| A.高锰酸钾溶液 | B.NaOH溶液 | C.饱和食盐水 | D.盐酸溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】电石,主要成分为CaC2,杂质主要有CaO、CaS等,是工业和实验室制乙炔的常用原料,某研究性学习小组拟用下列两种方法测定市售电石中的CaC2质量分数:
方法一:用电石与水反应,测定生成乙炔的体积。
(1)用化学方程式表示此法测定原理:___________ 。
(2)现提供下列仪器、装置:按气流由左向右顺序填写选用装置的顺序号:___________ 。

(3)对获得准确气体体积不必要的操作是:___________ ;
①检查装置气密性
②在恢复到室温后,再上下移动量气装置,使左右液面持平
③在气体发生装置胶塞上连接导管,通入N2,将生成乙炔气体全部送入量气装置
④读数时,视线与量气管内液面最低点持平
方法二:将电石在O2或空气中灼烧,使之发生反应: ,测定生成CO2质量。
,测定生成CO2质量。
称量1.40g样品于如图所示的石英管中(夹持及加热装置省略),从a处缓缓通入空气,高温灼烧石英管使样品完全反应,测得丙装置质量比反应前增重1.80g。
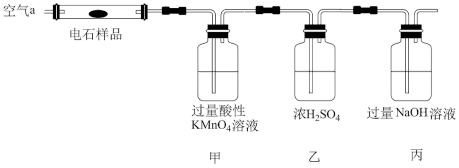
(4)甲瓶中酸性KMnO4(aq)作用:___________ ;
(5)测得电石中CaC2质量分数为___________ 。
(6)实验后发现石英管严重腐蚀,其原因是(用化学方程式解释):___________ ;
(7)你认为该实验设计的缺陷___________ ,改进方式___________ 。
方法一:用电石与水反应,测定生成乙炔的体积。
(1)用化学方程式表示此法测定原理:
(2)现提供下列仪器、装置:按气流由左向右顺序填写选用装置的顺序号:

(3)对获得准确气体体积不必要的操作是:
①检查装置气密性
②在恢复到室温后,再上下移动量气装置,使左右液面持平
③在气体发生装置胶塞上连接导管,通入N2,将生成乙炔气体全部送入量气装置
④读数时,视线与量气管内液面最低点持平
方法二:将电石在O2或空气中灼烧,使之发生反应:
 ,测定生成CO2质量。
,测定生成CO2质量。称量1.40g样品于如图所示的石英管中(夹持及加热装置省略),从a处缓缓通入空气,高温灼烧石英管使样品完全反应,测得丙装置质量比反应前增重1.80g。

(4)甲瓶中酸性KMnO4(aq)作用:
(5)测得电石中CaC2质量分数为
(6)实验后发现石英管严重腐蚀,其原因是(用化学方程式解释):
(7)你认为该实验设计的缺陷
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室制得的乙炔中常混有H2S、PH3等杂质气体。如图是两学生设计的实验装置,用来测定电石样品中CaC2的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ所示。
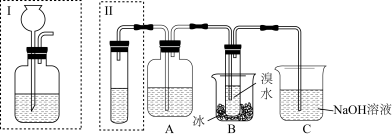
(1)A瓶中的液体可以从酸性KMnO4溶液和CuSO4溶液中选择,应该选择_______ ,它的作用是_______ 。
(2)写出实验室制取乙炔的化学方程式_______ 。
(3)装置C中NaOH作用是_______ ;
(4)装置B中的现象是_______ , B装置中发生的反应方程式_______ 。

(1)A瓶中的液体可以从酸性KMnO4溶液和CuSO4溶液中选择,应该选择
(2)写出实验室制取乙炔的化学方程式
(3)装置C中NaOH作用是
(4)装置B中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:乙炔是无色无味的气体,实验室制的乙炔因电石中含有  、
、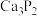 等,与水反应产生
等,与水反应产生 、
、 等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
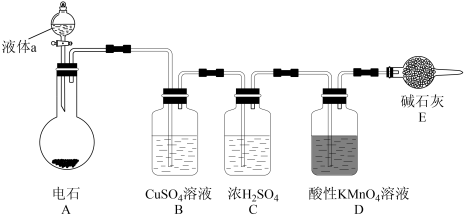
(1)写出实验室制取乙炔的化学方程式:___________
(2)实验室制取乙炔时,分液漏斗中的液体a通常是(填名称):___________
(3)CuSO4溶液的作用是:___________
(4)装置D中的现象是:___________
(5)若将乙炔气体通入足量的溴水溶液中,溴水褪色,其反应的化学反应方程式为:___________
(6)装置E的作用是___________ 。
 、
、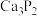 等,与水反应产生
等,与水反应产生 、
、 等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
等气体,所以所制乙炔气体会有难闻的臭味。如图是某课外小组制取乙炔并测定乙炔的某些性质的实验。
(1)写出实验室制取乙炔的化学方程式:
(2)实验室制取乙炔时,分液漏斗中的液体a通常是(填名称):
(3)CuSO4溶液的作用是:
(4)装置D中的现象是:
(5)若将乙炔气体通入足量的溴水溶液中,溴水褪色,其反应的化学反应方程式为:
(6)装置E的作用是
您最近一年使用:0次



