研究硫酸铜的量对锌与稀硫酸反应生成氢气速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。下列说法不正确的是
| 实验混合溶液 | A | B | C | D | E | F |
| 4 mol/LH2SO4溶液(mL) | 30 |  |  |  |  | 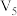 |
| 饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | 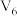 | 20 |
| H2O(mL) | 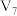 | 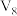 | 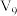 | 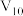 | 10 | 0 |
| 时间(s) | 60 | 50 | 40 | 30 | 20 | 45 |
| A.B组相较于A组反应速率加快,是因为形成了Zn-Cu-稀硫酸原电池 |
| B.加入MgSO4与Ag2SO4可以起与硫酸铜相同的加速作用 |
C. , ,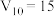 |
| D.F组时间比E组长,可能是置换出的铜太多,覆盖在锌粒表面,阻碍了反应的进行 |
更新时间:2022-05-20 09:27:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】对于某可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是| A.该反应为放热反应,则该反应只有在低温下才能自发进行 |
| B.保持容器内气体压强不变,向其中加入He,化学反应速率不变 |
| C.保持容器容积不变,向其中加入He,化学反应速率增大 |
| D.达到化学平衡时,4v正(O2)=5v逆(NO) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图是可逆反应:C(s)+H2O(g)⇌CO(g)+H2(g) ∆H<0的速率一时间图像,t1时刻改变的条件可能是


| A.恒容通入CO(g) | B.缩小容器体积 | C.升高温度 | D.恒容通入H2O(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】少量铁片与100mL0.01mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变 的产量,可以使用如下方法中的
的产量,可以使用如下方法中的
①加 ②加
②加 溶液③滴入几滴浓盐酸④加少量铁粉⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用100mL0.1mol/L盐酸。
溶液③滴入几滴浓盐酸④加少量铁粉⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用100mL0.1mol/L盐酸。
 的产量,可以使用如下方法中的
的产量,可以使用如下方法中的①加
 ②加
②加 溶液③滴入几滴浓盐酸④加少量铁粉⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用100mL0.1mol/L盐酸。
溶液③滴入几滴浓盐酸④加少量铁粉⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用100mL0.1mol/L盐酸。| A.①⑥⑦ | B.③⑤⑧ | C.③⑦⑧ | D.③④⑥⑦⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关说法中不正确的是
| A.将SO2通入BaCl2溶液中至饱和,无沉淀产生,再通入过量NH3,产生沉淀 |
| B.二氧化硫可广泛用于食品的增白 |
| C.用AlCl3溶液制取Al(OH)3,沉淀剂选用氨水比选用NaOH溶液好 |
| D.纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,反应速率加快 |
您最近一年使用:0次



