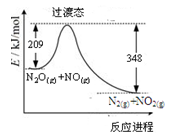
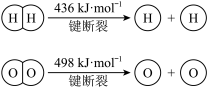
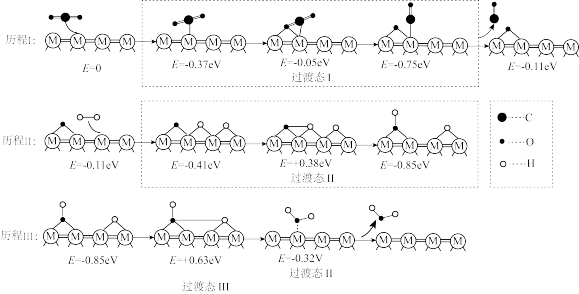
在合适的金属催化剂作用下,可以实现逆水煤气变换反应: CO2(g) + H2(g)⇌CO(g) +2H2O(g)。 反应的微观过程和相对能量(E)如下图所示,“*”代表在催化剂表面被吸附。
下列说法错误的是

下列说法错误的是
| A.历程I反应的方程式可表示为CO2(g)→CO(g) + O* |
| B.历程II涉及H- H的断裂和O- H的形成 |
| C.历程III决定了总反应的反应速率 |
| D.金属催化剂使整个反应的ΔH减小 |
更新时间:2022/06/11 11:26:43
|
相似题推荐
【推荐1】属于氧化还原反应且反应过程中能量变化符合如图所示的是
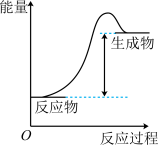

A.CaCO3 CaO+CO2↑ CaO+CO2↑ | B.CH4+2O2 CO2+2H2O CO2+2H2O |
C.C+CO2 2CO 2CO | D.2KOH+H2SO4=K2SO4+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:2H2O(l)===2H2(g)+O2(g)ΔH=+571.6 kJ•mol-1,2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ•mol-1。当1 g液态水变为气态水时,对其热量变化的下列描述:①放出;②吸收;③2.44 kJ;④4.88 kJ;⑤88 kJ。其中正确的是
| A.②和⑤ | B.①和③ |
| C.②和④ | D.②和③ |
您最近一年使用:0次
【推荐1】丙烯( )与氯化氢反应生成1-氯丙烷(
)与氯化氢反应生成1-氯丙烷( )的能量随反应进程的变化如图所示,下列叙述正确的是
)的能量随反应进程的变化如图所示,下列叙述正确的是

 )与氯化氢反应生成1-氯丙烷(
)与氯化氢反应生成1-氯丙烷( )的能量随反应进程的变化如图所示,下列叙述正确的是
)的能量随反应进程的变化如图所示,下列叙述正确的是
| A.第Ⅰ和Ⅱ两步反应均为放热反应 |
| B.1molCH3CH=CH2(g)和1molHCl(g)的总键能大于1molCH3CH2CH2Cl(l)总键能 |
| C.与起始总反应物比,产物CH3CH2CH2Cl(l)更稳定 |
D.使用适当的催化剂能够改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
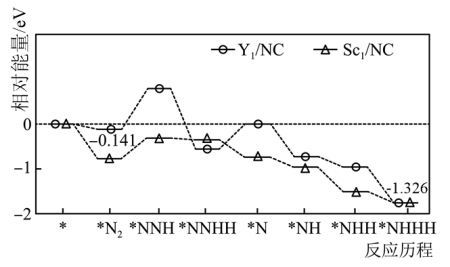
【推荐2】我国科学家合成了Y、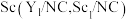 单原子催化剂,用于电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是
单原子催化剂,用于电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是
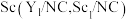 单原子催化剂,用于电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是
单原子催化剂,用于电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是
A.相同条件下,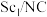 比 比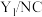 催化剂更利于吸附氮气 催化剂更利于吸附氮气 |
| B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氨气的平衡转化率 |
C.使用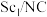 单原子催化剂,反应的快慢由生成 单原子催化剂,反应的快慢由生成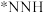 的速率决定 的速率决定 |
| D.工业合成氨与电化学催化还原氮气均涉及到共价键的断裂与形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在一定条件下,已知下列物质燃烧的化学方程式为:
C(s) +O2(g) =CO2(g) △H= -393.5 kJ·mol-1
2H2(g) +O2(g) =2H2O(l) △H= -572 kJ·mol-1
CH4(g) +2O2(g) =CO2(g) +2H2O(l) △H= -890 kJ·mol-1
在此条件下,下列叙述正确的是
C(s) +O2(g) =CO2(g) △H= -393.5 kJ·mol-1
2H2(g) +O2(g) =2H2O(l) △H= -572 kJ·mol-1
CH4(g) +2O2(g) =CO2(g) +2H2O(l) △H= -890 kJ·mol-1
在此条件下,下列叙述正确的是
| A.C(s) +2H2(g) =CH4(g) △H= +75.5 kJ·mol-1 |
| B.CH4(g) +O2(g) =C(s) +2H2O(g) △H= - 1283.5 kJ·mol-1 |
| C.1 mol H2(g)和3 mol CH4(g)燃烧共放热2956 kJ·mol-1 |
| D.l6g CH4充分燃烧放出的热量约等于4 g H2燃烧放出的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列表述中正确的是
| A.在恒压下,凡是自发的过程一定是放热的 |
| B.因为焓是状态函数,而恒压反应的焓变等于恒压反应热,所以热也是状态函数 |
C.单质的 和 和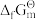 都为零 都为零 |
| D.在恒温恒压条件下,封闭体系自由能减少的过程是自发过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知热化学方程式:一定条件下, 在密闭容器中进行合成氨反应:N2(g)+3H2(g)=2NH3(g),△H=-92.4kJ·mol-1。下列说法中正确的是
| A.将1molN2(g)和3molH2(g)置于个密闭容器中充分反应后,放出热量为-92.4kJ |
| B.反应达到平衡时,NH3的生成速率为零 |
| C.恒温恒压下,在上述已达到平衡的体系中加入高效催化剂,NH3的转化率一定增大 |
| D.相同条件下,1molN2(g)和3molH2(g)的键能之和小于2molNH3(g)的键能 |
您最近一年使用:0次