对知识的归纳和总结是学好化学的重要方法。在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图所示),即氢氧化钙与图中四类物质能够发生化学反应。
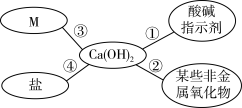
(1)图中M所属的物质类别是_______ 。
(2)氢氧化钙可由生石灰与水反应制得,该反应能_______ (填“吸收”或“放出”)热量。
(3)利用图中氢氧化钙能与_______ 反应的性质,可以解释“用石灰浆粉刷墙壁,干燥后墙面就变硬了”的现象。
(4)利用图中④氢氧化钙与盐反应的性质中,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该反应的化学方程式_______ 。

(1)图中M所属的物质类别是
(2)氢氧化钙可由生石灰与水反应制得,该反应能
(3)利用图中氢氧化钙能与
(4)利用图中④氢氧化钙与盐反应的性质中,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该反应的化学方程式
2022高一·上海·专题练习 查看更多[2]
(已下线)第01讲 常见的化学物质-【暑假自学课】2022年新高一化学暑假精品课(沪科版2020必修第一册)(已下线)第01讲 物质的分类及转化(练)-2023年高考化学一轮复习讲练测(新教材新高考)
更新时间:2022-06-17 12:19:52
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】从海水中提取金属镁的生产步骤有:①浓缩结晶,②加熟石灰,③加盐酸,④过滤,⑤熔融电解,正确的生产步骤是_________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】工业上用氨气和氢气直接合成氨,并通过下列转化过程制备硝酸:
N2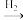 NH3
NH3 NO
NO  NO2
NO2 HNO3
HNO3
(1)上述物质中为红棕色气体的是_______ (填化学式);
(2)写出氮气与氢气的反应方程式_______ ;
(3)配平NO2→HNO3的化学方程式:3NO2+H2O=_______ HNO3+NO;
N2
 NH3
NH3 NO
NO  NO2
NO2 HNO3
HNO3(1)上述物质中为红棕色气体的是
(2)写出氮气与氢气的反应方程式
(3)配平NO2→HNO3的化学方程式:3NO2+H2O=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】乙烯(C2H4)是一种重要的工业原料,在化学工业上有着重要的用途。乙烯完全燃烧时,每一个乙烯分子能和两个B分子反应生成两个C分子和两个D分子,如图所示。
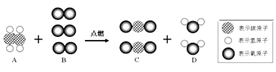
请根据示意图回答下列问题:
(1)上述反应中,___________ (填“分子”、“原子”之一)是化学变化中的最小微粒。
(2)上述反应一定___________ 质量守恒定律(填“遵守”、“不遵守”之一)。
(3)上述反应的化学方程式为___________
(4)上述反应属于___________ 反应(填“分解”、“化合”、“置换”、“复分解”、“氧化”之一)

请根据示意图回答下列问题:
(1)上述反应中,
(2)上述反应一定
(3)上述反应的化学方程式为
(4)上述反应属于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)现有下列10种物质:①H2O、②空气、③Mg、④CaO、⑤KOH、⑥NH3·H2O、⑦CuSO4·5H2O、⑧碘酒、⑨C2H5OH和⑩NaHCO3。
其中,属于混合物的是______________ (填序号,下同);属于碱的是______________ ;属于盐的是______________ 。
(2)标准状况下,①4 g氢气、②33.6 L CH4、③6.02×1023个水分子中,含分子数最多的是________ ,含原子数最多的是__________ 。
其中,属于混合物的是
(2)标准状况下,①4 g氢气、②33.6 L CH4、③6.02×1023个水分子中,含分子数最多的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有下列物质:①CuSO4 ②Ca(OH)2 ③碘酒 ④CH3COOH ⑤单晶硅
其中属于混合物的是___________ (填序号,下同);属于单质的是___________ ;属于酸的是_______ ;属于碱的是__________ ;属于盐的是___________
其中属于混合物的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】为了打赢“蓝天保卫战”,太原市从2020年10月19日至2021年3月31日开始实施机动车限行。回答下列问题:
(1)已知空气中的污染物主要有 、
、 、
、 等,其中属于氧化物的是
等,其中属于氧化物的是_______ ; 和
和 属于氧的
属于氧的_______ (填“同素异形体”或“同位素”)。
(2)若测得太原市某日 空气中含有1.5微克
空气中含有1.5微克 ,则
,则 的物质的量为
的物质的量为_______  (结果保留两位有效数字)。
(结果保留两位有效数字)。
(3)目前我国城市新装修的房间内挥发性有机物的浓度普遍超过国家标准,请列举其中的两种污染物:_______ 。
(1)已知空气中的污染物主要有
 、
、 、
、 等,其中属于氧化物的是
等,其中属于氧化物的是 和
和 属于氧的
属于氧的(2)若测得太原市某日
 空气中含有1.5微克
空气中含有1.5微克 ,则
,则 的物质的量为
的物质的量为 (结果保留两位有效数字)。
(结果保留两位有效数字)。(3)目前我国城市新装修的房间内挥发性有机物的浓度普遍超过国家标准,请列举其中的两种污染物:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】能源是现代社会物质文明的原动力,与我们每个人息息相关。
I.人们常利用化学反应中的能量变化为人类服务。
(1)化石燃料是人类利用最多的常规能源,为促进社会的可持续发展,人类不断地寻找更多新能源,例如:______ 、______ (任意书写两种新能源)。
(2)下列反应属于吸热反应的是______ (填序号)
①CH4燃烧 ②C与CO2反应 ③煅烧石灰石(主要成分是CaCO3)制生石灰
④氯化铵晶体和 混合搅拌
混合搅拌
Ⅱ.已知31g白磷变为31g红磷释放能量。
(3)上述变化属于______ (填“物理”或“化学”)变化。
(4)常温常压下,白磷与红磷更稳定的是______ 。
Ⅲ.如图是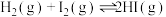 反应过程中的能量变化图。
反应过程中的能量变化图。______ (填“放热反应”或“吸热反应”)。
(6)已知1molH2与1mol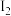 完全反应生成2molHI会放出11kJ的能量,则1gH2与足量
完全反应生成2molHI会放出11kJ的能量,则1gH2与足量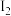 完全反应,放出
完全反应,放出______ kJ能量。断开1molH—H键、1molH—I键分别需要吸收的能量为436KJ、299kJ,则断开1molI—I键需要吸收的能量为______ kJ。
I.人们常利用化学反应中的能量变化为人类服务。
(1)化石燃料是人类利用最多的常规能源,为促进社会的可持续发展,人类不断地寻找更多新能源,例如:
(2)下列反应属于吸热反应的是
①CH4燃烧 ②C与CO2反应 ③煅烧石灰石(主要成分是CaCO3)制生石灰
④氯化铵晶体和
 混合搅拌
混合搅拌Ⅱ.已知31g白磷变为31g红磷释放能量。
(3)上述变化属于
(4)常温常压下,白磷与红磷更稳定的是
Ⅲ.如图是
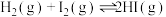 反应过程中的能量变化图。
反应过程中的能量变化图。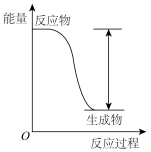
(6)已知1molH2与1mol
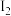 完全反应生成2molHI会放出11kJ的能量,则1gH2与足量
完全反应生成2molHI会放出11kJ的能量,则1gH2与足量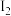 完全反应,放出
完全反应,放出
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1。
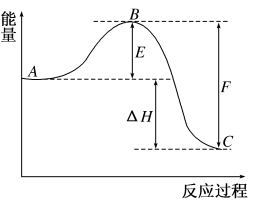
请回答下列问题:
(1)该反应属于_______ 反应(填“放热”或“吸热”)。
(2)图中C表示_______ 。
(3)从化学键的角度分析,F代表什么意义?_______ 。
(4)图中ΔH=_______ kJ·mol-1。
(5)若已知1 mol SO2(g)氧化为1 mol SO3(l)的ΔH2=-Q kJ·mol-1,则ΔH1_______ ΔH2(填“>”“<”或“=”)。

请回答下列问题:
(1)该反应属于
(2)图中C表示
(3)从化学键的角度分析,F代表什么意义?
(4)图中ΔH=
(5)若已知1 mol SO2(g)氧化为1 mol SO3(l)的ΔH2=-Q kJ·mol-1,则ΔH1
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氢能是理想的能源之一。冬奥会的氢能客车搭载了“氢腾”燃料电池系统,实现了绿色出行。回答下列问题:
(1)利用太阳能催化光解水是制备H2的方法之一。太阳能催化光解水制备H2的原理如图所示,光解水中能量的转化形式为_______ 。

(2)在高温时,水蒸气与灼热的炭反应也能制得H2。该反应的能量变化如图所示。

①该反应为_______ 反应(填“吸热”或“放热”),下列有关该反应的说法正确的是_______ (填序号)。
a.反应物的总能量高于产物的总能量
b.该反应过程中化学能全部转化为热能
c.该反应属于氧化还原反应
d.反应过程中,化学键的断裂与形成是化学反应中能量变化的主要原因
②H2、CO、C都是常用的燃料。1 mol H2.1 mol CO、1 mol C完全燃烧生成H2O(l)或CO2(g)时,放出的热量分别为285.8 kJ、283. 0 kJ、393. 5 kJ。相同质量的这三种燃料完全燃烧时放出的热量由大到小的顺序为_______ (用化学式表示)。
(3)如图是以铂(Pt)为电极的氢氧燃料电池示意图,稀H2SO4为电解质溶液,a电极发生的电极反应式是H2-2e-=2H+。
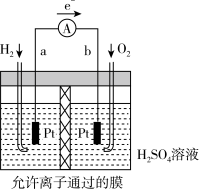
①电池的正极是_______ (填“a”或“b”)极,电池工作时,溶液中SO 移向
移向_______ (填“a”或“b”)极。
②若有4g H2参加反应,O2在b极获得电子的物质的量为_______ 。
(1)利用太阳能催化光解水是制备H2的方法之一。太阳能催化光解水制备H2的原理如图所示,光解水中能量的转化形式为

(2)在高温时,水蒸气与灼热的炭反应也能制得H2。该反应的能量变化如图所示。

①该反应为
a.反应物的总能量高于产物的总能量
b.该反应过程中化学能全部转化为热能
c.该反应属于氧化还原反应
d.反应过程中,化学键的断裂与形成是化学反应中能量变化的主要原因
②H2、CO、C都是常用的燃料。1 mol H2.1 mol CO、1 mol C完全燃烧生成H2O(l)或CO2(g)时,放出的热量分别为285.8 kJ、283. 0 kJ、393. 5 kJ。相同质量的这三种燃料完全燃烧时放出的热量由大到小的顺序为
(3)如图是以铂(Pt)为电极的氢氧燃料电池示意图,稀H2SO4为电解质溶液,a电极发生的电极反应式是H2-2e-=2H+。

①电池的正极是
 移向
移向②若有4g H2参加反应,O2在b极获得电子的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】常见气体的除杂方法及装置选择。除去气体中的杂质通常有如下3套装置:


气体(括号内为杂质) | 除杂试剂 | 装置 |
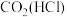 | ||
 | ||
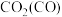 | ||
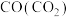 | ||
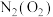 | ||
 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| HNO3(H2SO4) | ||
| Cu(Fe) | ||
| ZnSO4(CuSO4) | ||
| NaCl(Na2CO3) |
您最近一年使用:0次



