题型:
难度:0.4
引用次数:990
题号:16154031
为从粗食盐水中除去 等离子,以制得精盐水。某同学设计如下方案:
等离子,以制得精盐水。某同学设计如下方案:

下列说法正确的是
 等离子,以制得精盐水。某同学设计如下方案:
等离子,以制得精盐水。某同学设计如下方案:
下列说法正确的是
A.A中主要有 和 和 ,也可能有一些 ,也可能有一些 |
B.②中加入过量 溶液的主要目的是为了除去 溶液的主要目的是为了除去 |
C.D中只有 这三种离子 这三种离子 |
D.③中发生的反应只有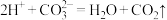 |
更新时间:2022-06-30 15:34:25
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从废水中回收硫酸亚铁和金属铜。请根据流程图回答下列问题,完成回收的简单实验方案。
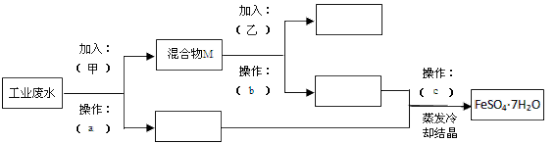
(1)操作a的名称为__________ 。
(2)加入的甲、乙物质分别为________ 、_________ 。
A.浓H2SO4B.稀H2SO4C.Fe粉 D.稀HCl
(3)操作c过程中用到的仪器是_______________ 。
A.坩埚 B.蒸发皿 C.玻璃棒 D.酒精灯
(4)Fe2+具有较强的还原性,易变质,检验产品FeSO4∙7H2O变质的方法是_____________________ 。
(5)为方便处理废液,检测人员取废水样10mL,做相应如图流程处理。加入加入甲物质质量为4.2g,最终得到FeSO4∙7H2O27.8g(不考虑处理过程中的损失),则原试样中c(Fe2+)=__________ 。

(1)操作a的名称为
(2)加入的甲、乙物质分别为
A.浓H2SO4B.稀H2SO4C.Fe粉 D.稀HCl
(3)操作c过程中用到的仪器是
A.坩埚 B.蒸发皿 C.玻璃棒 D.酒精灯
(4)Fe2+具有较强的还原性,易变质,检验产品FeSO4∙7H2O变质的方法是
(5)为方便处理废液,检测人员取废水样10mL,做相应如图流程处理。加入加入甲物质质量为4.2g,最终得到FeSO4∙7H2O27.8g(不考虑处理过程中的损失),则原试样中c(Fe2+)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】高氯酸铵(NH4ClO4)可用作火箭推进剂等。制备 NH4ClO4的工艺流程如下:
(1) 电解 NaClO3溶液时,ClO3-在__ 极发生反应, 其电极反应式为____________ 。
(2)“ 除杂” 有两种方案。
方案 1:加入盐酸和 H2O2溶液,NaClO3转化为ClO2,化学方程式为_____________ 。
方案 2:加入氨水和 FeCl2·4H2O,NaClO3转化为 Cl-,离子方程式为_____________ , 如果FeCl2· 4H2O过量会出现黑色磁性沉淀,该沉淀可能是___________ 。(填化学式)
(3)“反应” 时用 NaClO4 和 NH4Cl在90℃制备NH4ClO4。 如果用浓盐酸和液氨代替NH4Cl,则无需加热,原因是______________________________________ 。
(4)该流程中可循环利用的物质是______________ 。(填化学式)

(1) 电解 NaClO3溶液时,ClO3-在
(2)“ 除杂” 有两种方案。
方案 1:加入盐酸和 H2O2溶液,NaClO3转化为ClO2,化学方程式为
方案 2:加入氨水和 FeCl2·4H2O,NaClO3转化为 Cl-,离子方程式为
(3)“反应” 时用 NaClO4 和 NH4Cl在90℃制备NH4ClO4。 如果用浓盐酸和液氨代替NH4Cl,则无需加热,原因是
(4)该流程中可循环利用的物质是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】I.盐X由四种元素构成,其相对分子质量不超过300。 某学习小组进行如下实验:

已知溶液甲中只含有一种金属阳离子。
(1)化合物X的组成元素________ (填元素符号) 化合物X的化学式为________ 。
(2)黄色溶液甲与SO2反应的化学方程式________________ 。
(3)已知碱性条件下氨气可以与X溶液发生反应,生成一种气体单质,写出反应的离子方程式________________________ 。
II. 某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3 +2H2O=2
+2H2O=2 + MnO2↓+4OH-
+ MnO2↓+4OH-
回答下列问题:
(1)装置A中a的作用是______ ;A 中制备Cl2的化学方程式为____________________ 。
(2)上述装置存在一处缺陷, 会导致KMnO4产本降低,改进的方法是______________ 。

已知溶液甲中只含有一种金属阳离子。
(1)化合物X的组成元素
(2)黄色溶液甲与SO2反应的化学方程式
(3)已知碱性条件下氨气可以与X溶液发生反应,生成一种气体单质,写出反应的离子方程式
II. 某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3
 +2H2O=2
+2H2O=2 + MnO2↓+4OH-
+ MnO2↓+4OH-回答下列问题:
(1)装置A中a的作用是
(2)上述装置存在一处缺陷, 会导致KMnO4产本降低,改进的方法是
您最近一年使用:0次
【推荐1】过硼酸钠是一种用途广泛的无机过氧化物,可用作织物的漂白、染色,医药上可作为消毒剂和杀菌剂。一种由硼镁矿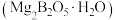 制取过硼酸钠
制取过硼酸钠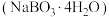 的工艺流程图如下所示。
的工艺流程图如下所示。

已知:
①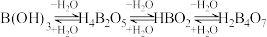 ,若
,若 时,以
时,以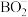 形式存在;若
形式存在;若 时,以
时,以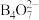 形式存在。
形式存在。
②过硼酸钠为白色晶体,微溶于水,其水溶液不稳定,存在于冷的溶液中,难溶于乙醇。
③硼砂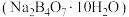 为白色晶体,溶于水吸热,在水中溶解度如图1所示。
为白色晶体,溶于水吸热,在水中溶解度如图1所示。

回答下列问题:
(1)步骤Ⅰ中为加快硼镁矿浸出,除粉碎矿石、升高温度外,还可采取的措施___________ 。(填一项操作即可)
(2)写出步骤Ⅰ中的化学方程式___________ 。
(3)下列说法不正确的是___________。
(4)步骤Ⅲ的回流反应过程需要控制恒温水浴(0℃左右)的理由是_____ 。
请选出正确的操作排序完成装置A中的回流反应:按图2组装好装置→(___________)→(___________)→打开磁力搅拌器→打开冷凝水→(___________)→(___________)→(___________)_____ 。
①用纸槽向c处加入硼砂;②用漏斗向c处加入硼砂;③打开a处旋塞加入双氧水
④调高恒温水浴温度;⑤调低恒温水浴温度;⑥c处加入氢氧化钠溶液。
(5)硼砂水溶液具有缓冲溶液(指酸和盐的混合体系,如醋酸和醋酸钠)的作用,请用离子方程式表示该缓冲溶液的形成过程___________ 。
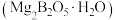 制取过硼酸钠
制取过硼酸钠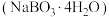 的工艺流程图如下所示。
的工艺流程图如下所示。
已知:
①
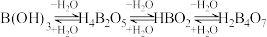 ,若
,若 时,以
时,以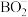 形式存在;若
形式存在;若 时,以
时,以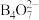 形式存在。
形式存在。②过硼酸钠为白色晶体,微溶于水,其水溶液不稳定,存在于冷的溶液中,难溶于乙醇。
③硼砂
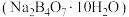 为白色晶体,溶于水吸热,在水中溶解度如图1所示。
为白色晶体,溶于水吸热,在水中溶解度如图1所示。
回答下列问题:
(1)步骤Ⅰ中为加快硼镁矿浸出,除粉碎矿石、升高温度外,还可采取的措施
(2)写出步骤Ⅰ中的化学方程式
(3)下列说法不正确的是___________。
A.步骤Ⅱ中通入的 目的是降低溶液pH值使 目的是降低溶液pH值使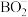 转为 转为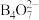 |
| B.步骤Ⅰ、Ⅱ中操作①为过滤,操作②为蒸发浓缩、冷却结晶、抽滤 |
C.步骤Ⅲ发生化学反应生成过硼酸钠(其阴离子结构如图所示),其中硼元素的化合价未发生变化 |
| D.步骤Ⅳ中宜选用的洗涤剂和干燥方式分别为蒸馏水和减压干燥 |
请选出正确的操作排序完成装置A中的回流反应:按图2组装好装置→(___________)→(___________)→打开磁力搅拌器→打开冷凝水→(___________)→(___________)→(___________)
①用纸槽向c处加入硼砂;②用漏斗向c处加入硼砂;③打开a处旋塞加入双氧水
④调高恒温水浴温度;⑤调低恒温水浴温度;⑥c处加入氢氧化钠溶液。
(5)硼砂水溶液具有缓冲溶液(指酸和盐的混合体系,如醋酸和醋酸钠)的作用,请用离子方程式表示该缓冲溶液的形成过程
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
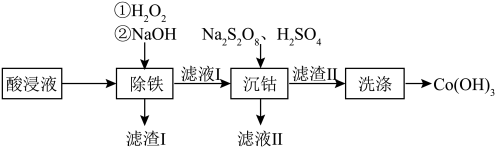
【推荐2】某工厂采用如下工艺处理含钴废料的硫酸浸取液(含 、
、 和
和 )
) 时:以下说法正确的是
时:以下说法正确的是
 、
、 和
和 )
)
 时:以下说法正确的是
时:以下说法正确的是| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 1.9 | 7.5 | 7.7 | 0.1 | 6.5 |
| 沉淀完全的pH | 3.2 | 9.0 | 9.2 | 1.1 | 8.0 |
A.滤液Ⅱ中主要存在的离子有 、 、 、 、 、 、 |
B.根据流程可知: 的还原性大于 的还原性大于 |
C.检验 是否洗涤干净可以用稀盐酸和 是否洗涤干净可以用稀盐酸和 溶液 溶液 |
D.沉钻过程中发生的主要反应的离子方程式为 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】甲酸(HCOOH)是还原性弱酸,常用于橡胶、医药等工业生产,也可用于制备重要的化工原料[Cu(HCOO)2·4H2O]。
I.碱式碳酸铜的制备
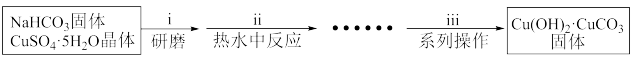
(1)“操作i”中研磨的目的是__ 。
(2)“操作ii”发生的反应是:2CuSO4+4NaHCO3═Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O。原料中NaHCO3必须过量的原因是__ 。反应温度低于80℃的原因是__ 。
(3)“操作iii”中系列操作包括过滤、__ 、干燥。
II.甲酸的制备
(4)一定条件下,CO能与NaOH固体发生反应:CO+NaOH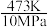 HCOONa,再将HCOONa酸化,即可得HCOOH。
HCOONa,再将HCOONa酸化,即可得HCOOH。
①为了证明“CO与NaOH固体发生了反应”,甲同学设计下列验证方案:取少许固体产物,配成溶液,在常温下测其pH,若pH>7,则得证。该方案是否可行__ (填“是”或“否”),请简述你的理由:__ 。
②乙同学设计了另一个定性验证方案:取固体产物,配成溶液,__ (请补充完整)。
III.甲酸铜的合成及纯度测定
(5)实验室按Cu(OH)2·CuCO3+4HCOOH+5H2O═2Cu(HCOO)2·4H2O+CO2↑反应制得甲酸铜晶体,按以下步骤测定其纯度。
步骤一:准确称取mg甲酸铜晶体样品,配成250mL溶液;
步骤二:移取25.00mL溶液于锥形瓶中,往溶液中加入足量KI摇匀,用cmol/LNa2S2O3溶液滴定至溶液变浅黄色时,加入10mL10%KSCN试剂,并加几滴淀粉溶液,继续用cmol/LNa2S2O3溶液滴定至终点,共消耗Na2S2O3溶液V1mL。
步骤三:用25.00mL蒸馏水代替甲酸铜溶液,重复步骤二,消耗Na2S2O3溶液V2mL;
已知:CuI难溶于水,能吸附I2;2Cu2++4I-=2CuI↓+I2;I2+2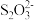 =
=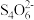 +2I-;CuI(s)+SCN-(aq)
+2I-;CuI(s)+SCN-(aq) CuSCN(s)+I-(aq)
CuSCN(s)+I-(aq)
①配制溶液时用到的玻璃仪器有:烧杯、量筒、玻璃棒和__ ;
②实验中加入10mL10%KSCN试剂的目的是__ 。
③甲酸铜晶体的纯度__ (列表达式即可,Cu(HCOO)2·4H2O的摩尔质量为226g/mol)。
I.碱式碳酸铜的制备
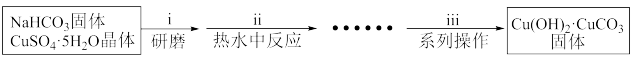
(1)“操作i”中研磨的目的是
(2)“操作ii”发生的反应是:2CuSO4+4NaHCO3═Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O。原料中NaHCO3必须过量的原因是
(3)“操作iii”中系列操作包括过滤、
II.甲酸的制备
(4)一定条件下,CO能与NaOH固体发生反应:CO+NaOH
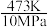 HCOONa,再将HCOONa酸化,即可得HCOOH。
HCOONa,再将HCOONa酸化,即可得HCOOH。①为了证明“CO与NaOH固体发生了反应”,甲同学设计下列验证方案:取少许固体产物,配成溶液,在常温下测其pH,若pH>7,则得证。该方案是否可行
②乙同学设计了另一个定性验证方案:取固体产物,配成溶液,
III.甲酸铜的合成及纯度测定
(5)实验室按Cu(OH)2·CuCO3+4HCOOH+5H2O═2Cu(HCOO)2·4H2O+CO2↑反应制得甲酸铜晶体,按以下步骤测定其纯度。
步骤一:准确称取mg甲酸铜晶体样品,配成250mL溶液;
步骤二:移取25.00mL溶液于锥形瓶中,往溶液中加入足量KI摇匀,用cmol/LNa2S2O3溶液滴定至溶液变浅黄色时,加入10mL10%KSCN试剂,并加几滴淀粉溶液,继续用cmol/LNa2S2O3溶液滴定至终点,共消耗Na2S2O3溶液V1mL。
步骤三:用25.00mL蒸馏水代替甲酸铜溶液,重复步骤二,消耗Na2S2O3溶液V2mL;
已知:CuI难溶于水,能吸附I2;2Cu2++4I-=2CuI↓+I2;I2+2
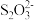 =
=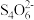 +2I-;CuI(s)+SCN-(aq)
+2I-;CuI(s)+SCN-(aq) CuSCN(s)+I-(aq)
CuSCN(s)+I-(aq)①配制溶液时用到的玻璃仪器有:烧杯、量筒、玻璃棒和
②实验中加入10mL10%KSCN试剂的目的是
③甲酸铜晶体的纯度
您最近一年使用:0次



