2018年5月,美国研究人员成功实现在常温常压下用氮气和水生产氨,其原理如图所示。下列说法不正确的是
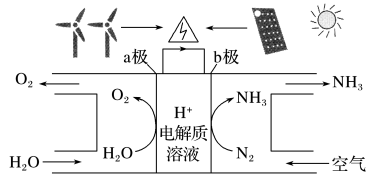

| A.图中能量转化的方式有2种 |
| B.b极的发生的电极反应方程式为:N2+6e-+6H+=2NH3 |
| C.H+向b极区移动 |
| D.a极上每产生22.4LO2,流过电极的电子数为4NA |
更新时间:2022-06-17 11:54:26
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】“打赢蓝天保卫战”,对污染防治要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如图。当该装置工作时,下列说法不正确的是


| A.电路中通过7.5mol电子时,共产生N2的体积为44.8L |
| B.盐桥中Cl-向X极移动 |
| C.电流由Y极沿导线流向X极 |
| D.Y极周围溶液pH减小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在盛有稀硫酸的烧杯中,放入用导线连接的铜片和锌片,下列说法正确的是
| A.负极发生还原反应 |
| B.电子通过导线由铜片流向锌片 |
| C.正极上有氢气逸出,正极电极反应式为:2H++2e-=H2↑ |
| D.负极附近的SO42-离子浓度逐渐增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】以葡萄糖为燃料的微生物燃料电池结构如图所示(假设M,N两电极均为惰性电极),下列说法正确的是
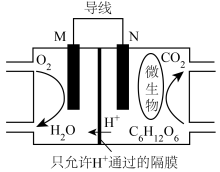

| A.N电极上发生氧化反应,得到电子 |
| B.电池工作时,外电路中电子的流动方向:N电极→导线→M电极 |
| C.M电极上的电极反应式:O2+4H+-4e-=2H2O |
| D.电路中每转移1.2mol电子,此时生成CO2的质量为13.2g |
您最近一年使用:0次
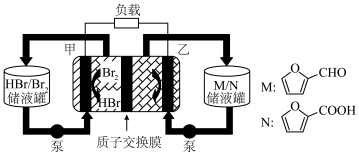
【推荐2】我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如图。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是


| A.放电时,a电极反应为I2Br-+2e-=2I-+Br- |
| B.放电时,溶液中离子的数目增大 |
| C.充电时,b电极每增重0.65g,溶液中有0.02molI-被还原 |
| D.充电时,a电极接外电源负极 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】HCOOH燃料电池的工作原理如图所示。下列说法正确的是
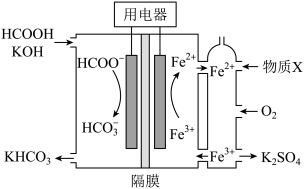

| A.放电时K+通过隔膜向右迁移 |
B.正极电极反应式为:HCOO-+2OH--2e-= +H2O +H2O |
| C.放电过程中需补充的物质X为H2SO4 |
| D.每转移0.4mol电子,理论上消耗标准状况下1.12LO2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列有关电池的说法中错误的是
| A.原电池放电过程中,负极发生氧化反应 |
| B.原电池工作时电子从负极出发,经外电路流向正极,再从正极经电解液回到负极构成闭合回路 |
C.某燃料电池用熔融碳酸盐作电解质,两极分别通入CO和O2,则通入CO的一极为负极,电极反应式为CO+2e-+CO =2CO2 =2CO2 |
| D.根据自发氧化还原反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑设计的原电池,可以是常温下用铁和铝作电极,用氢氧化钠溶液作电解质溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+8H2O+5Fe2(SO4)3+K2SO4设计如下原电池,盐桥中装有饱和K2SO4琼脂溶液,其阴、阳离子可向甲、乙做定向移动,从而把甲、乙连接以形成闭合回路,形成原电池。下列说法正确的是


A.a电极上发生的反应为: +8H++5e﹣═Mn2++4H2O +8H++5e﹣═Mn2++4H2O |
| B.外电路电子的流向是从a到b |
C.电池工作时,盐桥中的 移向甲烧杯 移向甲烧杯 |
| D.b电极上发生氧化反应 |
您最近一年使用:0次

 直至全部润湿。下列叙述正确的是
直至全部润湿。下列叙述正确的是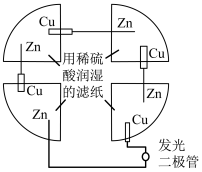
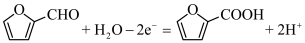
 通过质子交换膜向电极甲移动
通过质子交换膜向电极甲移动 使溶液复原,理论上消耗160g
使溶液复原,理论上消耗160g


