2020年有科学家通过观察金星的酸性云层,分析出金星存在磷化氢(PH3)气体,从而推测金星可能存在生命的迹象。
(1)P的原子结构示意图____ 。
(2)PH3中P原子与H原子之间的相互作用是____ (填“离子键”或“共价键”)。
(3)非金属性S强于P,从原子结构解释原因___ ,得电子能力S大于P。
(4)下列关于N、P元素及化合物的说法正确的是____ (填序号)。
①磷元素的最高正化合价为+5
②气态氢化物的稳定性:NH3<PH3
③磷的最高价氧化物对应的水化物属于酸
(1)P的原子结构示意图
(2)PH3中P原子与H原子之间的相互作用是
(3)非金属性S强于P,从原子结构解释原因
(4)下列关于N、P元素及化合物的说法正确的是
①磷元素的最高正化合价为+5
②气态氢化物的稳定性:NH3<PH3
③磷的最高价氧化物对应的水化物属于酸
更新时间:2022/07/04 10:04:54
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求回答下列问题:
(1)①基态原子的N层有1个未成对电子,M层未成对电子数最多的元素的价电子排布式为_____ 。
②最外层电子数是次外层电子数3倍的元素的轨道表示式为_____ 。
③Cu原子的结构示意图为_____ 。
(2)N原子核外有_____ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为_____ 。
(3)某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的_____ 区。
(1)①基态原子的N层有1个未成对电子,M层未成对电子数最多的元素的价电子排布式为
②最外层电子数是次外层电子数3倍的元素的轨道表示式为
③Cu原子的结构示意图为
(2)N原子核外有
(3)某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求填写
(1)原子的电子式
H___ 、Ca___ 、N___ 、O__ 、Cl___ 、C___ 、Al___
(2)离子的电子式
①简单阳离子:氢离子____ 、钾离子____ 、钙离子____
②简单阴离子:氯离子___ 、氧离子____
③复杂阴、阳离子:铵根离子___ 、氢氧根离子____
(3)用电子式表示化合物CaF2的形成过程____
(4)Ca2+结构示意图____
(1)原子的电子式
H
(2)离子的电子式
①简单阳离子:氢离子
②简单阴离子:氯离子
③复杂阴、阳离子:铵根离子
(3)用电子式表示化合物CaF2的形成过程
(4)Ca2+结构示意图
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列事实能说明氯元素原子得电子能力比硫元素原子强的是________ 。
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强
③HCl的稳定性比H2S的大 ④HCl的还原性比H2S的弱
⑤HClO4的酸性比H2SO4的强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑦Cl2能与H2S反应生成S ⑧在周期表中Cl位于S同周期的右侧
⑨还原性:Cl-<S2-
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强
③HCl的稳定性比H2S的大 ④HCl的还原性比H2S的弱
⑤HClO4的酸性比H2SO4的强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑦Cl2能与H2S反应生成S ⑧在周期表中Cl位于S同周期的右侧
⑨还原性:Cl-<S2-
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】从宏观和微观两个角度认识元素的单质及其化合物是学好中学化学的重要基础。
(1)组成 的三种元素,其对应的简单离子半径由小到大的顺序为
的三种元素,其对应的简单离子半径由小到大的顺序为___________ 。
(2) 、
、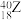 、
、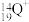 、
、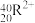 、
、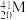 5种微粒,所属元素的种类有
5种微粒,所属元素的种类有___________ 种
(3)下列各组物质中,含有化学键类型都相同的是___________。
(4)将HCl和NaCl分别溶于水。下列说法正确的是___________。
(5)能用于比较Cl与S非金属性强弱的依据是___________。
(1)组成
 的三种元素,其对应的简单离子半径由小到大的顺序为
的三种元素,其对应的简单离子半径由小到大的顺序为(2)
 、
、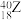 、
、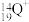 、
、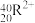 、
、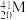 5种微粒,所属元素的种类有
5种微粒,所属元素的种类有(3)下列各组物质中,含有化学键类型都相同的是___________。
| A.HI和NaCl | B.NaF和KOH | C.CO和HCl | D. 和NaBr 和NaBr |
| A.HCl的离子键被破坏 | B.NaCl的共价键被破坏 |
| C.HCl和NaCl的化学键均遭破坏 | D.HCl和NaCl的化学键均未遭破坏 |
| A.熔沸点:硫单质>氯单质 | B.酸性: |
C.热稳定性: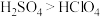 | D.氧化性: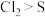 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】下列关于元素周期表及周期律的叙述,其中错误的是
| A.一般在过渡元素中寻找一些化学反应新型催化剂 |
| B.氯化氢HCl是比溴化氢HBr稳定的气体 |
| C.研制农药通常考虑含有元素周期表右上角元素(氟、氯、硫、磷等)的有机物 |
| D.按F2→I2的顺序单质氧化性逐渐减弱,故前面的卤素单质可将后面的卤素从它们的盐溶液里置换出来 |
| E.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
| F.砹(At)为ⅦA元素,推测单质砹为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸 |
| G.ⅠA族元素全部是金属元素,第ⅦA族位于元素周期表第7纵列 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】用电子式表示下列物质的形成过程。
(1)
_________
(2)
__________
(1)

(2)

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出下列物质形成过程的电子式:(离子键、极性键、非极性键)
(1)Cl2__________________ 含有________ 键
(2)HCl__________________ 含有________ 键
(3)MgCl2__________________ 含有________ 键
(4)H2O2______________ 含有________ 、________ 键
(5)NaOH______________ 含有________ 、________ 键
(1)Cl2
(2)HCl
(3)MgCl2
(4)H2O2
(5)NaOH
您最近一年使用:0次

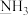
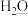

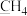
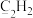
 键又有π键的是
键又有π键的是

