如图是氨元素的几种价态与物质类别的对应关系:

回答下列问题:
(1)写出氮元素在元素周期表的位置_______ 。
(2)从氢元素化合价分析, 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式:_______ ,这个反应 体现了
体现了_______ 性。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。写出用C检验 的存在的离子方程式
的存在的离子方程式_______ 。
(4)物质B为氮元素的气态氢化物,B的化学式为_______ ;实验室制取B的化学方程式为_______ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。

回答下列问题:
(1)写出氮元素在元素周期表的位置
(2)从氢元素化合价分析,
 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式: 体现了
体现了(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为 的存在的离子方程式
的存在的离子方程式(4)物质B为氮元素的气态氢化物,B的化学式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
更新时间:2022-07-22 12:41:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)写出一个化学方程式,其转化属于“氮的固定”:______________ 。
(2)写出实验室制取氨气的化学方程式:_________________________ ,实验室可以用_____________________________________ 试纸检验氨气。
(3)NO2与水反应的化学方程式为__________________________________________ ,该反应中氧化剂与还原剂的物质的量之比为____________ 。
(2)写出实验室制取氨气的化学方程式:
(3)NO2与水反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列反应的化学方程式雷雨发庄稼__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮气
(1)N2的物理性质
通常情况下,氮气是____ 、____ 的气体,密度比空气的____ ,____ 于水。
(2)N2的化学性质
氮分子内两个氮原子间以____ 结合,断开该化学键需要____ 的能量,所以氮气的化学性质很____ ,通常情况下____ 与其他物质发生化学反应,但在一定条件下氮气也可以和一些物质发生化学反应。写出氮气和下列物质反应的化学方程式。
①金属镁:____ ,氮气表现____ 性;
②氢气:____ ,氮气表现____ 性;
③氧气:____ ,氮气表现____ 性。
(1)N2的物理性质
通常情况下,氮气是
(2)N2的化学性质
氮分子内两个氮原子间以
①金属镁:
②氢气:
③氧气:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)联氨 又称联肼,N2H4,无色液体
又称联肼,N2H4,无色液体 是一种应用广泛的化工原料,可用作火箭燃料。
是一种应用广泛的化工原料,可用作火箭燃料。
①联氨电子式为______ ,其中氮的化合价为______ 。
②联氨为二元弱碱,在水中的电离方程式与氨相似。写出联氨的第一步电离方程式_______________ ,联氨与硫酸形成的酸式盐的化学式为______ 。
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为______  结果保留两位小数
结果保留两位小数 。
。
(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式______ ,反应中生成0.2molHNO3,转移的电子数目为______ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是______ 。
 又称联肼,N2H4,无色液体
又称联肼,N2H4,无色液体 是一种应用广泛的化工原料,可用作火箭燃料。
是一种应用广泛的化工原料,可用作火箭燃料。①联氨电子式为
②联氨为二元弱碱,在水中的电离方程式与氨相似。写出联氨的第一步电离方程式
(2)在100mLFeBr2溶液中通入标准状况下2.24LCl2,溶液中有
 的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 结果保留两位小数
结果保留两位小数 。
。(3)三氟化氮(NF3)是一种无色无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮元素的单质和常见化合物在工、农业生产中用途广泛。
(1)常用作食品袋中填充气的是_______ ,常用作制冷剂的化合物是_______ 。(填写化学式)
(2)铵盐大多在农业上用作化肥,实验室可用固体 与固体
与固体 加热反应来制备氨气,其化学方程式为
加热反应来制备氨气,其化学方程式为_______ 。欲吸收尾气中的 ,下列装置不宜选
,下列装置不宜选_______ (填字母)。(已知氨气难溶于有机溶剂 )
)
A.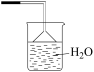 B.
B.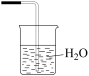 C.
C.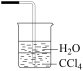 D.
D.
(3)用氢氟酸在玻璃上雕刻花纹,原理是_______ (用化学方程式表示);
(4)某稀硫酸和稀硝酸的混合溶液 ,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解
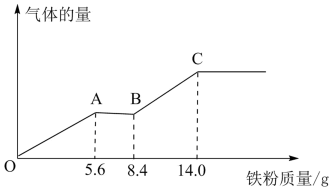
,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解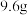 铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如下图所示(假设硝酸的还原产物为
铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如下图所示(假设硝酸的还原产物为 气体)。则原混合溶液中
气体)。则原混合溶液中 的物质的量为
的物质的量为_______ ,硫酸的物质的量浓度为_______ 。
(1)常用作食品袋中填充气的是
(2)铵盐大多在农业上用作化肥,实验室可用固体
 与固体
与固体 加热反应来制备氨气,其化学方程式为
加热反应来制备氨气,其化学方程式为 ,下列装置不宜选
,下列装置不宜选 )
)A.
 B.
B. C.
C. D.
D.
(3)用氢氟酸在玻璃上雕刻花纹,原理是
(4)某稀硫酸和稀硝酸的混合溶液
 ,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解
,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解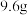 铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如下图所示(假设硝酸的还原产物为
铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如下图所示(假设硝酸的还原产物为 气体)。则原混合溶液中
气体)。则原混合溶液中 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
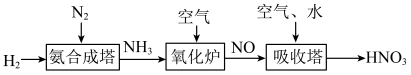
【推荐3】氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:_______ 。
(2)“吸收塔”尾部会有含NO、 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①氨转化法。已知7mol氨恰好能将含NO和 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为_______ 。
②NaClO溶液氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示: 和
和 ,其离子方程式:
,其离子方程式:_______ 。
Ⅱ.NaClO溶液的初始pH越小,NO转化率越高。其原因是_______ 。
(3)吸收塔中通常将NO和气从下面通入,水从上面喷入,这样做的目的是:_______ 。
(2)“吸收塔”尾部会有含NO、
 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:①氨转化法。已知7mol氨恰好能将含NO和
 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为②NaClO溶液氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示:
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示: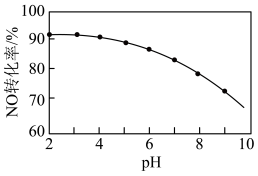
 和
和 ,其离子方程式:
,其离子方程式:Ⅱ.NaClO溶液的初始pH越小,NO转化率越高。其原因是
(3)吸收塔中通常将NO和气从下面通入,水从上面喷入,这样做的目的是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】为在冬奥会期间营造良好环境,京津冀地区开展秋冬季大气污染综合治理攻坚行动,取得显著成效。已知氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(1)以上污染物会造成的环境问题有____ (写一种即可)。
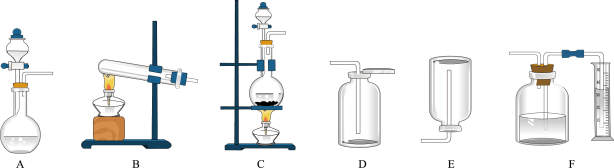
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是____ (填字母)。
(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图所示,写出该反应发生的化学方程式:____ 。

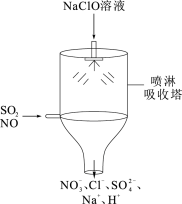
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是____ ,脱硝(NO)反应的离子方程式为____ 。
(5)某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4)3溶液吸收SO2反应的离子方程式:____ 。
②反应后,若要检验SO2是否过量,可用试剂为____ 。
(1)以上污染物会造成的环境问题有
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。催化反应机理如图所示,写出该反应发生的化学方程式:

(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是

(5)某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4)3溶液吸收SO2反应的离子方程式:
②反应后,若要检验SO2是否过量,可用试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有Fe、Cu组成的合金,其总物质的量为amol,Cu的物质的量分数为x;研成粉末后,全部投入含bmolHNO3的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为(写出所有可能情况)_______
(2)当溶液中金属离子只有Fe2+、Cu2+时,求b的取值范围(用含a、x的式子表示)_______
(3)当x=0.5,且溶液中Fe3+与Fe2+的物质的量相等时,在标准状况下共产生672mL气体,求a、b的值_______
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为(写出所有可能情况)
(2)当溶液中金属离子只有Fe2+、Cu2+时,求b的取值范围(用含a、x的式子表示)
(3)当x=0.5,且溶液中Fe3+与Fe2+的物质的量相等时,在标准状况下共产生672mL气体,求a、b的值
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知:氧化性:KMnO4>HNO3;Bi 元素+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,请回答下列问题:
(1)Bi和P元素在同一主族,试写出P在周期表中的位置____________________ ;
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为__________________________ ;
(3)实验④中的现象为:_______________________________________________ ;
(4)实验②反应的离子方程式是:________________________________________ ;
(5)实验③反应的离子方程式是:_______________________________________ 。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,请回答下列问题:
(1)Bi和P元素在同一主族,试写出P在周期表中的位置
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为
(3)实验④中的现象为:
(4)实验②反应的离子方程式是:
(5)实验③反应的离子方程式是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
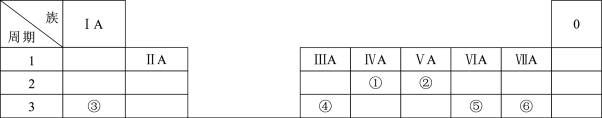
【推荐2】为纪念 Dmitri Mendeleev(德米特里·门德列夫)发明的元素周期表诞生150周年。联合国大会室布2019年是“国际化学元素周期表年。以下是元素周期表的一部分
回答下列问题:
(1)在上表中用实线画出元素周期表的上边界_______ 。
(2)元素X原子核外有_______ 种能量不同的电子,元素Y原子最外层电子的轨道表示式为_______ ;26号元素Z的最外层有2个电子,其原结构示意可以表示为_______ 。
(3)比较元素的金属性:X_______ Y(填“>”或“<),从原子结构的角度说明理由:_______ 。
(4)下列曲线分别表示元素的某种性质(y)与核电荷数(Z)的关系:

①若“y表示元素周期表中第一列元素单质熔点,则对应曲线的编号是_______ 。
②若“y”表示同一短周期元素的原子半径,则对应曲线的编号是_______ 。
(5)氮(N)元素的气态氢化物的电子式为_______ ,假设NH 是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第_______ 族,其“单质”在常温常压下_______ (填“能”或“不能”)导电。
| X | Y | ||||||||||||||||
| Z | |||||||||||||||||
(1)在上表中用实线画出元素周期表的上边界
(2)元素X原子核外有
(3)比较元素的金属性:X
(4)下列曲线分别表示元素的某种性质(y)与核电荷数(Z)的关系:

①若“y表示元素周期表中第一列元素单质熔点,则对应曲线的编号是
②若“y”表示同一短周期元素的原子半径,则对应曲线的编号是
(5)氮(N)元素的气态氢化物的电子式为
 是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
您最近一年使用:0次

 与I-、Fe2+、SO
与I-、Fe2+、SO 等离子均不能大量共存。(_____)
等离子均不能大量共存。(_____)