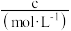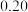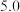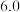某小组同学探究影响 分解反应速率的因素。
分解反应速率的因素。
(1)在 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为___________ 。
【实验方案】
(2)对比实验①和实验②,目的是探究___________ 对 分解反应速率的影响。
分解反应速率的影响。
(3)对比实验②和实验③,目的是探究 溶液的浓度对
溶液的浓度对 分解反应速率的影响,则实验③中x是
分解反应速率的影响,则实验③中x是___________ (填字母 )。
a.15 b.30
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如下图所示。
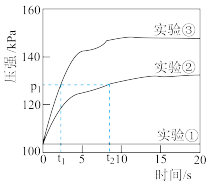
(4)上述实验方案中, 分解反应速率最快的是
分解反应速率最快的是___________ (填序号 )。
(5)能证明 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是___________ 。
 分解反应速率的因素。
分解反应速率的因素。(1)在
 作催化剂的条件下,
作催化剂的条件下, 发生分解反应的化学方程式为
发生分解反应的化学方程式为【实验方案】
| 实验编号 |  溶液 溶液 | 蒸馏水 | 催化剂 | 温度/℃ | |
 | V/mL | V/mL | |||
| ① | 3 | 10 | 20 | 无催化剂 | 20 |
| ② | 3 | 10 | 20 | 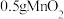 固体 固体 | 20 |
| ③ | 3 | 15 | x | 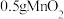 固体 固体 | 20 |
 分解反应速率的影响。
分解反应速率的影响。(3)对比实验②和实验③,目的是探究
 溶液的浓度对
溶液的浓度对 分解反应速率的影响,则实验③中x是
分解反应速率的影响,则实验③中x是a.15 b.30
【实验过程及分析】在恒温恒容的密闭容器中完成以上实验,测量反应过程中容器内的气体压强随时间的变化,实验数据如下图所示。

(4)上述实验方案中,
 分解反应速率最快的是
分解反应速率最快的是(5)能证明
 溶液的浓度对
溶液的浓度对 分解反应速率有影响的证据是
分解反应速率有影响的证据是
更新时间:2022-07-17 11:02:03
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】甲烷干法重整制 同时存在如下反应:
同时存在如下反应:
Ⅰ.
II.
Ⅲ.
(1)一定条件下,向 恒容密闭容器中通入
恒容密闭容器中通入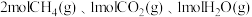 发生上述反应,达到平衡时,容器中
发生上述反应,达到平衡时,容器中 为
为 为
为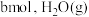 为
为 ,此时
,此时 的浓度为
的浓度为___________  ,反应Ⅲ的平衡常数为
,反应Ⅲ的平衡常数为___________ (用含a、b、c、V的代数式表示)。
(2)向恒容密闭容器中充入等物质的量的 和
和 ,若只发生反应Ⅰ和反应Ⅲ,则下列说法正确的是___________。
,若只发生反应Ⅰ和反应Ⅲ,则下列说法正确的是___________。
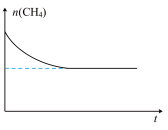
(3)恒温下,向恒压容器中通入物质的量为 的
的 和
和 的物质的量
的物质的量 随时间变化如图所示。在
随时间变化如图所示。在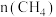 不变的条件下,改成加入
不变的条件下,改成加入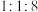 的
的 和
和 的混合气体,请在图中画出
的混合气体,请在图中画出 的物质的量随时间
的物质的量随时间 变化的曲线
变化的曲线___________ 。
(4)制约干重整工业化应用的主要问题是积碳 ,关键是开发出具有抗积碳性能
,关键是开发出具有抗积碳性能 的催化剂。催化剂A、B对积碳与消碳的影响如图所示:
的催化剂。催化剂A、B对积碳与消碳的影响如图所示:
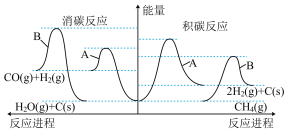
则工业生产时应选择的催化剂是___________ (填“A”或“B”),理由是___________ 。
 同时存在如下反应:
同时存在如下反应:Ⅰ.

II.

Ⅲ.

(1)一定条件下,向
 恒容密闭容器中通入
恒容密闭容器中通入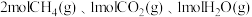 发生上述反应,达到平衡时,容器中
发生上述反应,达到平衡时,容器中 为
为 为
为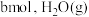 为
为 ,此时
,此时 的浓度为
的浓度为 ,反应Ⅲ的平衡常数为
,反应Ⅲ的平衡常数为(2)向恒容密闭容器中充入等物质的量的
 和
和 ,若只发生反应Ⅰ和反应Ⅲ,则下列说法正确的是___________。
,若只发生反应Ⅰ和反应Ⅲ,则下列说法正确的是___________。A.高温低压有利于提高 的平衡转化率 的平衡转化率 |
B.充分反应后的混合气体中, 的体积分数可能达到66.7% 的体积分数可能达到66.7% |
| C.充分反应后的混合气体通过生石灰,固体质量增大,说明干法重整反应存在限度 |
D.当混合气体中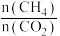 恒定时,反应达到平衡状态 恒定时,反应达到平衡状态 |
(3)恒温下,向恒压容器中通入物质的量为
 的
的 和
和 的物质的量
的物质的量 随时间变化如图所示。在
随时间变化如图所示。在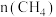 不变的条件下,改成加入
不变的条件下,改成加入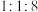 的
的 和
和 的混合气体,请在图中画出
的混合气体,请在图中画出 的物质的量随时间
的物质的量随时间 变化的曲线
变化的曲线
(4)制约干重整工业化应用的主要问题是积碳
 ,关键是开发出具有抗积碳性能
,关键是开发出具有抗积碳性能 的催化剂。催化剂A、B对积碳与消碳的影响如图所示:
的催化剂。催化剂A、B对积碳与消碳的影响如图所示:
则工业生产时应选择的催化剂是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】Ce2(CO3)3可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以CePO4形式存在,还含有SiO2、Al2O3、Fe2O3、CaF2等物质。以独居石为原料制备Ce2(CO3)3·nH2O的工艺流程如下:

回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为___________ 。
(2)为提高“水浸”效率,可采取的措施有____________________ (至少写两条)。
(3)滤渣Ⅲ的主要成分是___________ (填化学式)。
(4)“沉铈”过程中,生成Ce2(CO3)3·nH2O的离子方程式为___________ ,
(5)滤渣Ⅱ的主要成分为FePO4,在高温条件下,Li2CO3、葡萄糖(C6H12O6)和FePO4可制备电极材料LiFePO4,同时生成CO和H2O,该反应的化学方程式为______________________ 。

回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为
(2)为提高“水浸”效率,可采取的措施有
(3)滤渣Ⅲ的主要成分是
(4)“沉铈”过程中,生成Ce2(CO3)3·nH2O的离子方程式为
(5)滤渣Ⅱ的主要成分为FePO4,在高温条件下,Li2CO3、葡萄糖(C6H12O6)和FePO4可制备电极材料LiFePO4,同时生成CO和H2O,该反应的化学方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某小组利用 溶液和酸性
溶液和酸性 溶液反应来探究“反应条件对化学反应速率的影响”。
溶液反应来探究“反应条件对化学反应速率的影响”。
(1)向酸性 溶液中加入一定量的
溶液中加入一定量的 溶液,当溶液中的
溶液,当溶液中的 耗尽时,溶液紫色将褪去。为确保能观察到紫色褪去,初始
耗尽时,溶液紫色将褪去。为确保能观察到紫色褪去,初始 与
与 的物质的量需要满足关系
的物质的量需要满足关系
__________ 。
(2)为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案:
表中
____ ,理由是_________ 。
(3)已知(2)中实验①的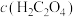 随反应时间t的变化曲线如图所示,若保持其他条件不变,请在图中画出50℃时
随反应时间t的变化曲线如图所示,若保持其他条件不变,请在图中画出50℃时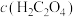 )随t的变化曲线
)随t的变化曲线_______ 。

 溶液和酸性
溶液和酸性 溶液反应来探究“反应条件对化学反应速率的影响”。
溶液反应来探究“反应条件对化学反应速率的影响”。(1)向酸性
 溶液中加入一定量的
溶液中加入一定量的 溶液,当溶液中的
溶液,当溶液中的 耗尽时,溶液紫色将褪去。为确保能观察到紫色褪去,初始
耗尽时,溶液紫色将褪去。为确保能观察到紫色褪去,初始 与
与 的物质的量需要满足关系
的物质的量需要满足关系
(2)为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案:
实验序号 | 反应温度 |
| 酸性 | 水 | ||
|
|
|
|
| ||
① | 25 |
|
|
|
| 0 |
② | 25 |
|
|
|
| x |

(3)已知(2)中实验①的
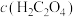 随反应时间t的变化曲线如图所示,若保持其他条件不变,请在图中画出50℃时
随反应时间t的变化曲线如图所示,若保持其他条件不变,请在图中画出50℃时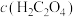 )随t的变化曲线
)随t的变化曲线
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】钼酸钠晶体(Na2MoO4·2H2O)是无公害型冷却水系统的金属缓蚀剂,由钼精矿(主要成分是MoS2,含少量PbS等)制备钼酸钠晶体的部分流程如图所示:
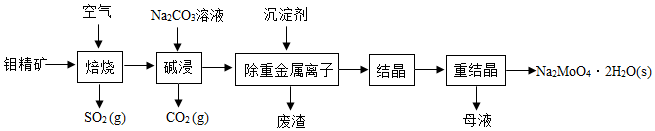
(1)Na2MoO4·2H2O中钼元素的化合价为______ ;
(2)焙烧时为了使钼精矿充分反应,可采取的措施是_______ (答出一条即可);
(3)试配平焙烧过程中钼精矿发生的主要反应的化学方程式
为__ MoS2+__ O2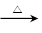
__ MoO3+___ SO2,该反应中氧化产物是________ (填化学式)
(4)碱浸时,MoO3与Na2CO3溶液反应的离子方程式为___________ ;
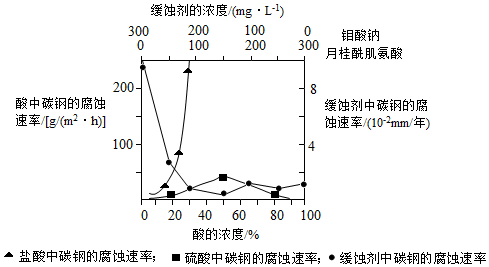
(5)下图是碳钢在3种不同介质中的腐蚀速率实验结果:
①碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异,其原因可能是____ 。
②空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4—Fe2O3保护膜。
密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入NaNO2。则NaNO2的作用是__ 。
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2 Lix(MoS2)n。则电池放电时的正极反应式是:
Lix(MoS2)n。则电池放电时的正极反应式是:__________________ 。

(1)Na2MoO4·2H2O中钼元素的化合价为
(2)焙烧时为了使钼精矿充分反应,可采取的措施是
(3)试配平焙烧过程中钼精矿发生的主要反应的化学方程式
为
(4)碱浸时,MoO3与Na2CO3溶液反应的离子方程式为
(5)下图是碳钢在3种不同介质中的腐蚀速率实验结果:

①碳钢在盐酸和硫酸中腐蚀速率随酸的浓度变化有明显差异,其原因可能是
②空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4—Fe2O3保护膜。
密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入NaNO2。则NaNO2的作用是
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2
 Lix(MoS2)n。则电池放电时的正极反应式是:
Lix(MoS2)n。则电池放电时的正极反应式是:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】亚硝酰硫酸(NOSO4H)主要用于分散染料重氮反应中取代亚硝酸钠,从而降低成本,提高产品质量。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。
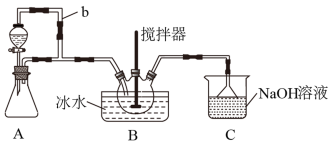
(1)装置A制取SO2,则A中反应的化学方程式为_______ ,导管b的作用是_______
(2)SO2与装置B中盛有的浓硫酸和浓硝酸的混合液在维持体系温度不得高于20℃的条件下,反应制得NOSO4H。反应过程中,亚硝酰硫酸和硝酸的物质的量随时间的变化如图所示。
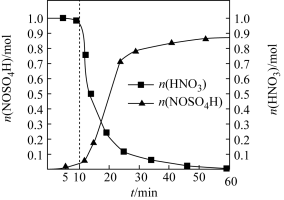
①装置B中发生反应的化学反应方程式为_______ 。
②反应进行到10min后,反应速度明显加快,其可能的原因是_______ 。
(3)装置C的主要作用是_______ 。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是_______ 。
(5)测定亚硝酰硫酸NOSO4H的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入0.1000mol·L−1、60.00mL的KMnO4标准溶液和10.00mL25%H2SO4溶液,然后摇匀。用0.2500mol·L−1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.0mL。已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4;2MnO +5C2O
+5C2O +16H+=2Mn2++10CO2↑+8H2O。达到滴定终点时的现象为
+16H+=2Mn2++10CO2↑+8H2O。达到滴定终点时的现象为_______ ,亚硝酰硫酸的纯度为_______ (精确到0.1%)。

(1)装置A制取SO2,则A中反应的化学方程式为
(2)SO2与装置B中盛有的浓硫酸和浓硝酸的混合液在维持体系温度不得高于20℃的条件下,反应制得NOSO4H。反应过程中,亚硝酰硫酸和硝酸的物质的量随时间的变化如图所示。

①装置B中发生反应的化学反应方程式为
②反应进行到10min后,反应速度明显加快,其可能的原因是
(3)装置C的主要作用是
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是
(5)测定亚硝酰硫酸NOSO4H的纯度:准确称取1.500g产品放入250mL的碘量瓶中,加入0.1000mol·L−1、60.00mL的KMnO4标准溶液和10.00mL25%H2SO4溶液,然后摇匀。用0.2500mol·L−1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.0mL。已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4;2MnO
 +5C2O
+5C2O +16H+=2Mn2++10CO2↑+8H2O。达到滴定终点时的现象为
+16H+=2Mn2++10CO2↑+8H2O。达到滴定终点时的现象为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】 (保险粉)是一种强还原剂,锌粉法制备
(保险粉)是一种强还原剂,锌粉法制备 的原理为
的原理为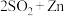
 、
、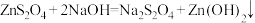 。制备
。制备 的装置(夹持及加热装置已省略)如图所示,回答下列问题:
的装置(夹持及加热装置已省略)如图所示,回答下列问题:
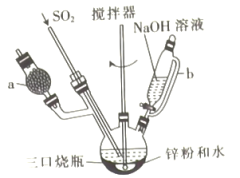
(1)仪器a中盛放的药品是___________ (填名称)。
(2)实验开始前,需要向三口烧瓶中充满 ,目的是
,目的是___________ 。
(3)通入三口烧瓶中的 是由铜屑与浓硫酸反应制得的,生成
是由铜屑与浓硫酸反应制得的,生成 的化学方程式为
的化学方程式为___________ 。
(4)制备 时,三口烧瓶的加热方式是
时,三口烧瓶的加热方式是___________ 。
(5)Zn粉消耗完全后,在搅拌下向三口烧瓶中加入NaOH溶液,充分反应后过滤,向滤液中加入NaCl固体,冷却结晶、过滤、蒸馏水洗涤,酒精洗涤及干燥得产品。加入NaCl固体的作用是_____________ ,酒精洗涤的目的是___________ 。
(6)取a g产品溶于适量NaOH溶液,加入亚甲基蓝指示剂,用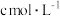 的
的 标准溶液滴定,至终点时消耗
标准溶液滴定,至终点时消耗 标准溶液V mL。已知:
标准溶液V mL。已知: 被还原为
被还原为 ,
, 被氧化为
被氧化为 。产品中
。产品中 的质量分数为
的质量分数为___________ (列出计算式)。
 (保险粉)是一种强还原剂,锌粉法制备
(保险粉)是一种强还原剂,锌粉法制备 的原理为
的原理为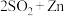
 、
、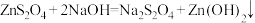 。制备
。制备 的装置(夹持及加热装置已省略)如图所示,回答下列问题:
的装置(夹持及加热装置已省略)如图所示,回答下列问题:
(1)仪器a中盛放的药品是
(2)实验开始前,需要向三口烧瓶中充满
 ,目的是
,目的是(3)通入三口烧瓶中的
 是由铜屑与浓硫酸反应制得的,生成
是由铜屑与浓硫酸反应制得的,生成 的化学方程式为
的化学方程式为(4)制备
 时,三口烧瓶的加热方式是
时,三口烧瓶的加热方式是(5)Zn粉消耗完全后,在搅拌下向三口烧瓶中加入NaOH溶液,充分反应后过滤,向滤液中加入NaCl固体,冷却结晶、过滤、蒸馏水洗涤,酒精洗涤及干燥得产品。加入NaCl固体的作用是
(6)取a g产品溶于适量NaOH溶液,加入亚甲基蓝指示剂,用
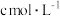 的
的 标准溶液滴定,至终点时消耗
标准溶液滴定,至终点时消耗 标准溶液V mL。已知:
标准溶液V mL。已知: 被还原为
被还原为 ,
, 被氧化为
被氧化为 。产品中
。产品中 的质量分数为
的质量分数为
您最近半年使用:0次