Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
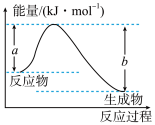
(1)如图表示某反应的能量变化关系,则此反应为___________ (填“吸收”或“放出”) ___________ kJ能量(用含有a、b的关系式表示)。
(2)反应H2(g)+ O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=___________ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为___________ 。
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
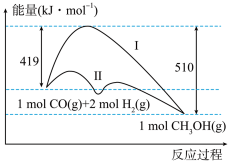
(4)计算当反应生成1.5molCH3OH(g)时,能量变化值是___________ kJ。
(5)推测反应CH3OH(g)⇌CO(g)+2H2(g)是___________ (填“吸热”或“放热”)反应。
Ⅲ.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。
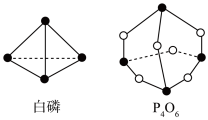
(6)则发生P4(白磷)+3O2(g)=P4O6(s)的反应,其中,生成1 mol P4O6需要___________ (“吸收或放出”)能量为___________ kJ
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |

(1)如图表示某反应的能量变化关系,则此反应为
(2)反应H2(g)+
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
II.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
CH3OH(g),反应过程中的能量变化情况如图所示。曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。
(4)计算当反应生成1.5molCH3OH(g)时,能量变化值是
(5)推测反应CH3OH(g)⇌CO(g)+2H2(g)是
Ⅲ.化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示:现提供以下化学键的键能(kJ·mol-1):P-P:198;P-O:360;O=O:498。

(6)则发生P4(白磷)+3O2(g)=P4O6(s)的反应,其中,生成1 mol P4O6需要
更新时间:2022-08-18 17:25:17
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)制氢的热化学方程式为_____________ 。
(2)H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。①H2S的平衡转化率
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。①H2S的平衡转化率 =
=____ %,反应平衡常数K=_____ 。
(3)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,已知25℃,NH3·H2O的Kb=1.8×10−5,H2SO3的Ka1=1.3×10−2,Ka2=6.2×10−8。若氨水的浓度为2.0 mol·L−1,溶液中的c(OH−)=________ mol·L−1。将SO2通入该氨水中,当c(OH−)降至1.0×10−7 mol·L−1时,溶液中的c( )/c(
)/c(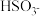 )=
)=___________________ 。
(1)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(Ⅰ)制氢的热化学方程式为
(2)H2S与CO2在高温下发生反应:H2S(g)+CO2(g)
 COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。①H2S的平衡转化率
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。①H2S的平衡转化率 =
=(3)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,已知25℃,NH3·H2O的Kb=1.8×10−5,H2SO3的Ka1=1.3×10−2,Ka2=6.2×10−8。若氨水的浓度为2.0 mol·L−1,溶液中的c(OH−)=
 )/c(
)/c( )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)NH3催化氧化可制备硝酸。NH3氧化时发生如下反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH1=-907.28 kJ·mol-1,
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH2=-1269.02kJ·mol-1,
则4NH3(g)+6NO(g)= 5N2(g)+6H2O(g) ΔH3=______ 。
(2)肼(N2H4)是一种火箭燃料。已知:N2(g)+2O2(g)= 2NO2(g) ΔH=+67.7 kJ·mol-1,N2H4(g)+O2(g)= N2(g)+2H2O(g) ΔH=-534.0 kJ·mol-1,NO2(g)= N2O4(g) ΔH=-28.0 kJ·mol-1,则反应2N2H4(g)+N2O4(g)= 3N2(g)+4H2O(g)的ΔH=
N2O4(g) ΔH=-28.0 kJ·mol-1,则反应2N2H4(g)+N2O4(g)= 3N2(g)+4H2O(g)的ΔH=____ kJ·mol-1。
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH2=-1269.02kJ·mol-1,
则4NH3(g)+6NO(g)= 5N2(g)+6H2O(g) ΔH3=
(2)肼(N2H4)是一种火箭燃料。已知:N2(g)+2O2(g)= 2NO2(g) ΔH=+67.7 kJ·mol-1,N2H4(g)+O2(g)= N2(g)+2H2O(g) ΔH=-534.0 kJ·mol-1,NO2(g)=
 N2O4(g) ΔH=-28.0 kJ·mol-1,则反应2N2H4(g)+N2O4(g)= 3N2(g)+4H2O(g)的ΔH=
N2O4(g) ΔH=-28.0 kJ·mol-1,则反应2N2H4(g)+N2O4(g)= 3N2(g)+4H2O(g)的ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)实验测得16 g甲醇[CH3OH(l)]在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25 kJ的热量,试写出甲醇燃烧热的热化学方程式:___ 。
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g) 2NH3(g) ΔH=akJ·mol-1。有关键能数据如下:
2NH3(g) ΔH=akJ·mol-1。有关键能数据如下:
试根据表中所列键能数据计算a=____ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的反应热为:ΔH=___ 。
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g)
 2NH3(g) ΔH=akJ·mol-1。有关键能数据如下:
2NH3(g) ΔH=akJ·mol-1。有关键能数据如下:| 化学键 | H—H | N—H | N≡N |
| 键能(kJ·mol-1) | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1
根据盖斯定律,计算298 K时由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的反应热为:ΔH=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】已知下列热化学方程式:
① H2(g) + O2(g) = H2O(l) △H = -285.8 kJ / mol
O2(g) = H2O(l) △H = -285.8 kJ / mol
② C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③ C(s) + H2O(g) =CO(g) + H2(g) △H= +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是_________ (填序号,下同),属于吸热反应的是_________ 。
(2)1 mol H2完全燃烧生成液态水,放出的热量为________________ 。
(3)碳的燃烧热△H=_______________ 。
(4)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式__________________________________ 。
① H2(g) +
 O2(g) = H2O(l) △H = -285.8 kJ / mol
O2(g) = H2O(l) △H = -285.8 kJ / mol② C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③ C(s) + H2O(g) =CO(g) + H2(g) △H= +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)1 mol H2完全燃烧生成液态水,放出的热量为
(3)碳的燃烧热△H=
(4)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知:
①H2O(g)=H2(g)+ O2(g) ΔH=+241.8kJ/mol
O2(g) ΔH=+241.8kJ/mol
②C(s)+ O2(g)=CO(g) ΔH=-110.5kJ/mol
O2(g)=CO(g) ΔH=-110.5kJ/mol
③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
请填写下列空白。
(1)上述反应中属于吸热反应的是_______ (填序号)。
(2)表示C的燃烧热的热化学方程式为_______ (填序号)。
(3)10gH2完全燃烧生成水蒸气,放出的热量为_______ kJ。
(4)写出CO燃烧的热化学方程式:_______ 。
(5)FeS2焙烧产生的 可用于制硫酸。已知
可用于制硫酸。已知 、
、 时:
时:
2SO2(g)+O2(g) 2SO3(g) ∆H1=-197kJ∙mol-1
2SO3(g) ∆H1=-197kJ∙mol-1
H2O(g) H2O(l) ∆H2=-44kJ∙mol-1
H2O(l) ∆H2=-44kJ∙mol-1
2SO2(g)+O2(g)+2H2O(g)= 2H2SO4(l) ∆H3=-545kJ∙mol-1
则SO3(g)与H2O(l)反应的热化学方程式是_______ 。
①H2O(g)=H2(g)+
 O2(g) ΔH=+241.8kJ/mol
O2(g) ΔH=+241.8kJ/mol②C(s)+
 O2(g)=CO(g) ΔH=-110.5kJ/mol
O2(g)=CO(g) ΔH=-110.5kJ/mol③C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)表示C的燃烧热的热化学方程式为
(3)10gH2完全燃烧生成水蒸气,放出的热量为
(4)写出CO燃烧的热化学方程式:
(5)FeS2焙烧产生的
 可用于制硫酸。已知
可用于制硫酸。已知 、
、 时:
时:2SO2(g)+O2(g)
 2SO3(g) ∆H1=-197kJ∙mol-1
2SO3(g) ∆H1=-197kJ∙mol-1H2O(g)
 H2O(l) ∆H2=-44kJ∙mol-1
H2O(l) ∆H2=-44kJ∙mol-12SO2(g)+O2(g)+2H2O(g)= 2H2SO4(l) ∆H3=-545kJ∙mol-1
则SO3(g)与H2O(l)反应的热化学方程式是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】2SO2(g)+O2(g) 2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
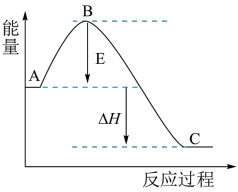
(1)图中A、表示:_____ (填“反应物能量”或“生成物能量 ”)。E的大小对该反应的反应热有无影响?_______ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点_____ (填“升高” “降低”)。
(2)图中ΔH=________ kJ/mol。
(3)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的总反应的ΔH=________ kJ/mol。
(4)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,表示氢气燃烧热的热化学方程式是_________
(5)已知中和热ΔH=-57.3kJ·mol-1,0.5 mol Ba(OH)2和0.5 molH2SO4的反应热ΔH_______ (填“>”“=”或“<”)-57.3kJ·mol-1
 2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
2SO3(g) ΔH反应过程的能量变化如图所示,已知1 mol SO2(g)被氧化为1 mol SO3(g)的ΔH=-98 kJ/mol。回答下列问题:
(1)图中A、表示:
(2)图中ΔH=
(3)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的总反应的ΔH=
(4)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,表示氢气燃烧热的热化学方程式是
(5)已知中和热ΔH=-57.3kJ·mol-1,0.5 mol Ba(OH)2和0.5 molH2SO4的反应热ΔH
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题:
(1)300℃,硅粉与HCl(g)反应生成1mol SiHCl3气体和H2(g) 时,放出225 kJ的热量。该反应的热化学方程式是_____________________ 。
(2)已知:CuCl2(s)=CuCl(s) + Cl2(g) ΔH1=+83 kJ/mol
Cl2(g) ΔH1=+83 kJ/mol
CuCl(s) + O2(g)=CuO(s) +
O2(g)=CuO(s) +  Cl2(g) ΔH2=-20 kJ/mol
Cl2(g) ΔH2=-20 kJ/mol
CuO(s) + 2HCl(g) = CuCl2(s) + H2O(g) ΔH3=-121 kJ/mol
则:4HCl(g) + O2(g) = 2Cl2(g) + 2H2O(g)的ΔH=_________ kJ/mol。
又知:
推算:断开1 mol H-O键与断开1 mol H-Cl键所需能量相差_______ kJ。
(1)300℃,硅粉与HCl(g)反应生成1mol SiHCl3气体和H2(g) 时,放出225 kJ的热量。该反应的热化学方程式是
(2)已知:CuCl2(s)=CuCl(s) +
 Cl2(g) ΔH1=+83 kJ/mol
Cl2(g) ΔH1=+83 kJ/molCuCl(s) +
 O2(g)=CuO(s) +
O2(g)=CuO(s) +  Cl2(g) ΔH2=-20 kJ/mol
Cl2(g) ΔH2=-20 kJ/molCuO(s) + 2HCl(g) = CuCl2(s) + H2O(g) ΔH3=-121 kJ/mol
则:4HCl(g) + O2(g) = 2Cl2(g) + 2H2O(g)的ΔH=
又知:

推算:断开1 mol H-O键与断开1 mol H-Cl键所需能量相差
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】Ⅰ.用碳棒作电极,电解下列水溶液:①Na2SO4溶液②AgNO3溶液③KCl溶液④CuCl2溶液。通过相同电量时,阴极产生的气体物质的量相同的是(填序号)_________ ;通过相同电量时,产生的气体总物质的量由多到少的排列顺序是(填序号)__________ 。
Ⅱ.到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)化学反应中放出的能量(焓变,△H)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=-185 kJ/mol
E(H-H)=436 kJ/mol, E(Cl-Cl)=247 kJ/mol,则E(H-Cl)=_____
(2)已知Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25 kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47 kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+19 kJ/mol
请写出CO还原FeO的热化学方程式:_________________________________ 。
(3)如图所示的装置:

该装置中Cu极为_____ 极;当铜片的质量变化了12.8g时,a极上消耗的O2在标准状况下的体积为_______ L。
Ⅱ.到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)化学反应中放出的能量(焓变,△H)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=-185 kJ/mol
E(H-H)=436 kJ/mol, E(Cl-Cl)=247 kJ/mol,则E(H-Cl)=
(2)已知Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-25 kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47 kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+19 kJ/mol
请写出CO还原FeO的热化学方程式:
(3)如图所示的装置:

该装置中Cu极为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】合成氨工业中,每生产2 mol NH3放出92.4 kJ热量。
(1)写出合成氨反应的热化学方程式为_______ 。
(2)已知:

1 mol N-H键断裂吸收的能量等于_______ kJ。
(3)已知关于铁的氧化物存在下列三个热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= -24.8 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.4 kJ/mol
则CO还原FeO的热化学方程式为CO(g)+FeO(s)=Fe(s)+CO2(g) △H=_______ kJ/mol。
(1)写出合成氨反应的热化学方程式为
(2)已知:

1 mol N-H键断裂吸收的能量等于
(3)已知关于铁的氧化物存在下列三个热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= -24.8 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.4 kJ/mol
则CO还原FeO的热化学方程式为CO(g)+FeO(s)=Fe(s)+CO2(g) △H=
您最近一年使用:0次



