回答下列问题:
(1)已知短周期元素A、B,A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为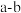 ,L层电子数为
,L层电子数为 ,则A为
,则A为___________ (填元素符号,下同),B为___________ 。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子多5,则X、Y分别为___________ 、___________ 。
(1)已知短周期元素A、B,A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为
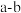 ,L层电子数为
,L层电子数为 ,则A为
,则A为(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子多5,则X、Y分别为
更新时间:2022-08-28 17:39:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____________ .
A.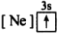 B.
B.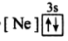 C.
C.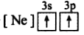 D.
D.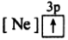
(2) 成为阳离子时首先失去
成为阳离子时首先失去____________ 轨道电子, 的价层电子排布式为
的价层电子排布式为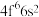 ,
,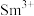 价层电子排布式为
价层电子排布式为____________ .比较离子半径:
____________ (填“大于”“小于”或“等于”) .
.
(3)在周期表中,与 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子核外 层电子的自旋
层电子的自旋___________ (填“相同”或“相反”). 中,电负性最高的元素是
中,电负性最高的元素是___________ .
(4) 基态核外电子排布式为
基态核外电子排布式为___________ .
A.
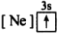 B.
B.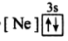 C.
C. D.
D.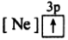
(2)
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式为
的价层电子排布式为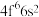 ,
,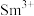 价层电子排布式为
价层电子排布式为
 .
.(3)在周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是 层电子的自旋
层电子的自旋 中,电负性最高的元素是
中,电负性最高的元素是(4)
 基态核外电子排布式为
基态核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有原子序数依次增大的A、B、C、D、E五种元素,A是短周期中族序数等于周期数的非金属元素;B元素的原子既不易失去也不易得到电子,其基态原子中每种能级电子数相同;C元素的价电子构型为nsnnpn+1;D的最外层电子数与电子层数之比为3:1;E是地壳中含量仅次于铝的金属元素,其合金用途最广,用量最大。
(1)E元素在周期表中的位置__________ ;E元素价电子排布式为__________ 。
(2)A分别与B、C、D能形成电子数为10的化合物,它们的沸点由高到低的顺序是______ (写分子式)。
(3)B与D形成的非极性分子的电子式为________ 。
(4)B、C、D三种元素的第一电离能由大到小的顺序是_____ (用元素符号表示)。
(5)C的单质分子中σ键和π键的个数比为________ 。
(6)已知在25℃、101kPa下:ABC(aq)+A2D(l)=BC-(aq)+A3D+(aq) ΔH=+45.6kJ·mol-1
A3D+(aq)+DA-(aq)=2A2D(l)ΔH=-57.3kJ·mol-1
则在25℃、101kPa的稀溶液中,ABC与DA-反应的热化学方程式是(以离子方程式表示):_______ 。
(1)E元素在周期表中的位置
(2)A分别与B、C、D能形成电子数为10的化合物,它们的沸点由高到低的顺序是
(3)B与D形成的非极性分子的电子式为
(4)B、C、D三种元素的第一电离能由大到小的顺序是
(5)C的单质分子中σ键和π键的个数比为
(6)已知在25℃、101kPa下:ABC(aq)+A2D(l)=BC-(aq)+A3D+(aq) ΔH=+45.6kJ·mol-1
A3D+(aq)+DA-(aq)=2A2D(l)ΔH=-57.3kJ·mol-1
则在25℃、101kPa的稀溶液中,ABC与DA-反应的热化学方程式是(以离子方程式表示):
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】金属“钙线”是炼制优质钢材的脱氧脱磷剂,某“钙线”的主要成分为金属M和Ca。
(1)Ca元素在元素周期表中的位置是_____ ,最外层电子排布式为________ 。
(2)CaF2的电子式为_____ ,CaF2熔点比SiF4熔点_______ (选填“高”、“低”或“相同”),原因是_____ 。
(3)将“钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n.则金属M为_____ ,检测Mn+的另一种方法是_____ 。
(4)配平下列化学方程式: P+ FeO+ CaO→ Ca3(PO4)2+ Fe,________ ,若生成的Fe为2.8g,则转移的电子数目为_____ 个。
(1)Ca元素在元素周期表中的位置是
(2)CaF2的电子式为
(3)将“钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n.则金属M为
(4)配平下列化学方程式: P+ FeO+ CaO→ Ca3(PO4)2+ Fe,
您最近一年使用:0次



