(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____________ .
A.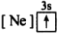 B.
B.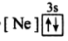 C.
C.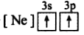 D.
D.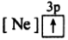
(2) 成为阳离子时首先失去
成为阳离子时首先失去____________ 轨道电子, 的价层电子排布式为
的价层电子排布式为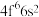 ,
,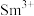 价层电子排布式为
价层电子排布式为____________ .比较离子半径:
____________ (填“大于”“小于”或“等于”) .
.
(3)在周期表中,与 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是___________ ,该元素基态原子核外 层电子的自旋
层电子的自旋___________ (填“相同”或“相反”). 中,电负性最高的元素是
中,电负性最高的元素是___________ .
(4) 基态核外电子排布式为
基态核外电子排布式为___________ .
A.
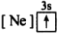 B.
B.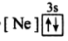 C.
C. D.
D.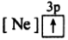
(2)
 成为阳离子时首先失去
成为阳离子时首先失去 的价层电子排布式为
的价层电子排布式为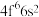 ,
,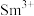 价层电子排布式为
价层电子排布式为
 .
.(3)在周期表中,与
 的化学性质最相似的邻族元素是
的化学性质最相似的邻族元素是 层电子的自旋
层电子的自旋 中,电负性最高的元素是
中,电负性最高的元素是(4)
 基态核外电子排布式为
基态核外电子排布式为
更新时间:2021-02-01 20:49:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是______ 个;
O2—、Na+、Cl—中半径最小的是_____________ 。
(2)NaCN晶体中含有的化学键类型为_____________________________ 。
(3)第二段过程中,产物属于双原子分子的结构式是___________ ,该物质一般要比其他共价化合物如:NH3、H2S等都要稳定,其原因为:___________________ ;写出该物质的一种用途:____________________ 。
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:2NaOCN+3NaClO→Na2CO3+CO2↑+3NaCl+N2↑
完成下列填空:
(1)上述反应涉及的元素中,氮原子核外价电子数是
O2—、Na+、Cl—中半径最小的是
(2)NaCN晶体中含有的化学键类型为
(3)第二段过程中,产物属于双原子分子的结构式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属“钙线”是炼制优质钢材的脱氧脱磷剂,某“钙线”的主要成分为金属M和Ca。
(1)Ca元素在元素周期表中的位置是_____ ,最外层电子排布式为________ 。
(2)CaF2的电子式为_____ ,CaF2熔点比SiF4熔点_______ (选填“高”、“低”或“相同”),原因是_____ 。
(3)将“钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n.则金属M为_____ ,检测Mn+的另一种方法是_____ 。
(4)配平下列化学方程式: P+ FeO+ CaO→ Ca3(PO4)2+ Fe,________ ,若生成的Fe为2.8g,则转移的电子数目为_____ 个。
(1)Ca元素在元素周期表中的位置是
(2)CaF2的电子式为
(3)将“钙线”试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n.则金属M为
(4)配平下列化学方程式: P+ FeO+ CaO→ Ca3(PO4)2+ Fe,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(2)基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式___________ ,该元素名称为___________ 。
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为___________ 。
(5)某有机物的结构简式为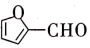 ,该分子内含有___________ (填序号)。
,该分子内含有___________ (填序号)。
(6)已知元素X的气态原子逐个失去第1个至第4个电子所需能量如下表所示:
元素X的常见化合价是___________(填序号)。
(1)Fe成为阳离子时首先失去
(2)基态S原子电子占据最高能级的电子云轮廓图为
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(5)某有机物的结构简式为
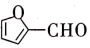 ,该分子内含有___________ (填序号)。
,该分子内含有___________ (填序号)。| A.11个σ键、2个π键 | B.10个σ键、2个π键 |
| C.10个σ键、3个π键 | D.11个σ键、3个π键 |
| I1 | I2 | I3 | I4 | |
| 电离能/(kJ·mol-1) | 578 | 1817 | 2745 | 11578 |
| A.+1 | B.+2 | C.+3 | D.+4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁及其化合物是中学化学中常见的物质。
(1)Fe基态原子核外电子排布式为____________________ 。
(2)钢铁生锈在生产和生活中比较普遍,可在钢铁设备上(如锅炉的内壁、船舶的外壳等)装上若干镁合金或锌块,以防止钢铁设备的腐蚀,这种方法通常被称为____________ 。
(3)铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,阴极的电极反应式为________ 。
(4)实验室中可用铁氰化钾溶液检验Fe2+,该反应的离子方程式为________________ 。
(5)常温时,FeCl3溶液pH<7,原因是(用离子方程式表示)____________________ 。
(6)FeCl3溶液加热蒸干并灼烧,所得到的固体物质是_____________ 。
(7)将0.1mol·L−1 FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该反应的离子方程式为________________ 。
(1)Fe基态原子核外电子排布式为
(2)钢铁生锈在生产和生活中比较普遍,可在钢铁设备上(如锅炉的内壁、船舶的外壳等)装上若干镁合金或锌块,以防止钢铁设备的腐蚀,这种方法通常被称为
(3)铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,阴极的电极反应式为
(4)实验室中可用铁氰化钾溶液检验Fe2+,该反应的离子方程式为
(5)常温时,FeCl3溶液pH<7,原因是(用离子方程式表示)
(6)FeCl3溶液加热蒸干并灼烧,所得到的固体物质是
(7)将0.1mol·L−1 FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置_______ ,钛原子核外有_______ 种空间运动状态不同的电子,Ti2+电子占据的最高能层的电子排布式为_______ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是_______ ,第一电离能介于Al、P之间的第三周期元素为_______ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为_______ ,B原子的杂化方式是_______ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有_______ (填序号)
①σ键②π键③氢键④配位键 ⑤离子键
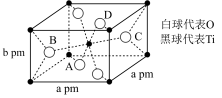
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为_______ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】H、C、N、O、Al、Fe是六种常见元素。
(1)Fe位于周期表第 周期,第 族,其基态原子未成对电子数为_______。碳的同素异形体中,金刚石熔点比C60 _____(填“高”、“低”)。
(2)用“>”或“<”填空:
(3)Al能将污水中NO3-转化为N2,同时铝的反应产物还能净化污水,该反应的离子方程式 ;其中产生的铝的化合物能净水的原理是 。
(4)已知①2H2(g) + O2(g) = 2H2O(l) △H=﹣571.66kJ•mol-1
②CH2=CH2(g) + 3O2(g) = 2CO2(g) + 2H2O(l) △H=﹣1306.42kJ•mol-1
写出利用CO2和H2合成(CH2=CH2)的热化学方程式为 。
(1)Fe位于周期表第 周期,第 族,其基态原子未成对电子数为_______。碳的同素异形体中,金刚石熔点比C60 _____(填“高”、“低”)。
(2)用“>”或“<”填空:
| 离子半径 | 电负性 | 第一电离能 | 沸点 |
| O2-____Al3+ | C___N | N____O | CH4____ NH3 |
(3)Al能将污水中NO3-转化为N2,同时铝的反应产物还能净化污水,该反应的离子方程式 ;其中产生的铝的化合物能净水的原理是 。
(4)已知①2H2(g) + O2(g) = 2H2O(l) △H=﹣571.66kJ•mol-1
②CH2=CH2(g) + 3O2(g) = 2CO2(g) + 2H2O(l) △H=﹣1306.42kJ•mol-1
写出利用CO2和H2合成(CH2=CH2)的热化学方程式为 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________ 。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_______ ,提供孤电子对的成键原子是________ 。
(3)单质铜及镍都是由______ 键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol–1、INi=1 753 kJ·mol–1,ICu> INi的原因是_______________________ 。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为
(3)单质铜及镍都是由
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料,光伏材料又称太阳能材料,只有半导体材料具有这种功能。硅(Si)、镓(Ga)、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:___________ 。硅烷很难像烷烃一样形成长链,这是因为硅的原子半径___________ (填“大于”“小于”或“等于”)碳的原子半径,因此键长___________ (填“长”或“短”),键能小。丁硅烯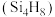 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是___________ 。
(3)光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是___________ 。
(4)硅和锗都能与氯元素形成四氯化物 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:___________ 。
(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
(1)硅能形成与烷烃类似的硅烷,写出乙硅烷的电子式:
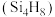 中
中 键与
键与 键的个数比为
键的个数比为(2)我国航天事业发展迅猛,太阳能电池材料使用的是砷化镓(GaAs)。基态砷原子中电子占据的最高能层符号是
(3)光催化还原
 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是
是该反应的良好催化剂。Zn、Ge、O电负性由大到小的顺序是(4)硅和锗都能与氯元素形成四氯化物
 和
和 ,从原子结构角度解释原因:
,从原子结构角度解释原因:(5)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定条件下,CO2与NH3反应可制得重要的化工产品三聚氰胺:3NH3 + 3CO2
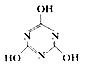 +3H2O。
+3H2O。
(1)基态N原子的价层电子排布图为____________ ,三聚氰胺的几种组成元素中电负性由大到小的顺序为____________ (用元素符号表示)。
(2)三聚氰胺中氮原子的杂化轨道类型为____________ 。
(3)上述合成三聚氰胺的反应过程中存在多种类型化学键的断裂与形成,但这些化学键中不包括____________ (填选项字母)。
a.α键 b.π键 c.非极性共价键 d.极性共价键
(4)三聚氰胺的熔点为250 ℃,则其晶体类型是____________ ,又知硝基苯的熔点为5.7 ℃,异致这两种物质熔点差异的原因是____________ 。
(5)随者科学技术的发展,科学家们已合成了由碳、氧两种元素形成的原子晶体.其晶胞结构如图(a) 所示:若晶胞参数为a pm,设NA表示阿伏伽德罗常数的值,则该晶胞的密度是____________ g • cm-3。

(6)SiO2晶体结构片断如图 (b)所示。通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
Si(s)+O2(g) SiO2(s),该反应的反应热△H =
SiO2(s),该反应的反应热△H = ___________

 +3H2O。
+3H2O。(1)基态N原子的价层电子排布图为
(2)三聚氰胺中氮原子的杂化轨道类型为
(3)上述合成三聚氰胺的反应过程中存在多种类型化学键的断裂与形成,但这些化学键中不包括
a.α键 b.π键 c.非极性共价键 d.极性共价键
(4)三聚氰胺的熔点为250 ℃,则其晶体类型是
(5)随者科学技术的发展,科学家们已合成了由碳、氧两种元素形成的原子晶体.其晶胞结构如图(a) 所示:若晶胞参数为a pm,设NA表示阿伏伽德罗常数的值,则该晶胞的密度是

(6)SiO2晶体结构片断如图 (b)所示。通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
| 化学键 | Si-O | Si-Si | O=O |
| 键能/ KJ·mol-1 | 460 | 176 | 498 |
Si(s)+O2(g)
 SiO2(s),该反应的反应热△H =
SiO2(s),该反应的反应热△H =
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】第四周期中的18种元素具有重要的用途。
(1)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则GeBr4晶体类型为_______ ,中心原子的杂化类型为_______ 。
(2)第四周期VA-ⅦA族的元素中,电负性由大到小的顺序为(用元素符号表示)_______ 。
(3)金属镍在材料科学上也有重要作用,它易形成配合物,如:Ni(CO)4、[Ni (NH3)6]2+等。写出一种与配体CO互为等电子体的阴离子_______ ;配体NH3分子的空间构型为_______ 。
(4)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为_______ ,第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,但Ga的第一电离能却明显低于Zn,原因是_______ 。
(1)已知四溴化锗是电子工业中的一种常用试剂,其熔点为26.1℃,沸点为186℃,则GeBr4晶体类型为
(2)第四周期VA-ⅦA族的元素中,电负性由大到小的顺序为(用元素符号表示)
(3)金属镍在材料科学上也有重要作用,它易形成配合物,如:Ni(CO)4、[Ni (NH3)6]2+等。写出一种与配体CO互为等电子体的阴离子
(4)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价电子排布式为
您最近一年使用:0次

 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此,你的解释是
再失去1个电子难,对此,你的解释是

