铁及其化合物是中学化学中常见的物质。
(1)Fe基态原子核外电子排布式为____________________ 。
(2)钢铁生锈在生产和生活中比较普遍,可在钢铁设备上(如锅炉的内壁、船舶的外壳等)装上若干镁合金或锌块,以防止钢铁设备的腐蚀,这种方法通常被称为____________ 。
(3)铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,阴极的电极反应式为________ 。
(4)实验室中可用铁氰化钾溶液检验Fe2+,该反应的离子方程式为________________ 。
(5)常温时,FeCl3溶液pH<7,原因是(用离子方程式表示)____________________ 。
(6)FeCl3溶液加热蒸干并灼烧,所得到的固体物质是_____________ 。
(7)将0.1mol·L−1 FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该反应的离子方程式为________________ 。
(1)Fe基态原子核外电子排布式为
(2)钢铁生锈在生产和生活中比较普遍,可在钢铁设备上(如锅炉的内壁、船舶的外壳等)装上若干镁合金或锌块,以防止钢铁设备的腐蚀,这种方法通常被称为
(3)铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,阴极的电极反应式为
(4)实验室中可用铁氰化钾溶液检验Fe2+,该反应的离子方程式为
(5)常温时,FeCl3溶液pH<7,原因是(用离子方程式表示)
(6)FeCl3溶液加热蒸干并灼烧,所得到的固体物质是
(7)将0.1mol·L−1 FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该反应的离子方程式为
更新时间:2020-05-19 13:00:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是人类较早使用的金属之一、运用所学知识,回答下列问题。
(1)用赤铁矿来进行高炉炼铁,总共消耗了标况下6.72 LCO气体,则生成Fe的质量为_____ 。
(2)不仅溶液中Fe2+易被氧化成Fe2+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式_________ ,现象为_________ 。
(3)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
①甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变血红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________ 。
②乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_________ 。
③丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_________ 。
(1)用赤铁矿来进行高炉炼铁,总共消耗了标况下6.72 LCO气体,则生成Fe的质量为
(2)不仅溶液中Fe2+易被氧化成Fe2+,溶液中白色沉淀Fe(OH)2更易被O2氧化,请写出反应的化学方程式
(3)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
①甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变血红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
②乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
③丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在人类的生活和工业生产中扮演着不可替代的角色。
(1)不锈钢在生活中的应用十分广泛,不锈钢通常是铁和碳、镍等形成的的合金,关于不锈钢和纯铁的比较,描述错误的是___________。
(2)FeSO4是补血剂的主要成分,若要检验某补血剂是否完全变质,可选择试剂___________。
(1)不锈钢在生活中的应用十分广泛,不锈钢通常是铁和碳、镍等形成的的合金,关于不锈钢和纯铁的比较,描述错误的是___________。
| A.不锈钢的硬度比纯铁高 | B.不锈钢比纯铁更耐腐蚀 |
| C.不锈钢是混合物 | D.不锈钢中所含的元素都是过渡元素 |
| A.NaOH | B.Fe | C.KSCN | D.KMnO4 |
您最近一年使用:0次
【推荐3】某种催化剂为铁的氧化物。化学兴趣小组对该催化剂中铁元素的价态进行了探究。请回答下列实验方案中的有关问题:
(一)实验仪器与试剂
仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;
试剂:3mol·L-1H2SO4、6mol·L-1HNO3、0.01mol·L-1KMnO4、NaOH稀溶液、20%KSCN溶液、蒸馏水。
(二)实验原理
Fe2+能使酸性KMnO4溶液紫色褪去;Fe3+溶液中滴加KSCN溶液变红色。
(1)一位同学将少许样品溶于稀硝酸中,取少许溶液滴加KSCN溶液后出现红色。由此得出为铁元素为+3价的结论。该结论是否合理___ ,并说明理由___ 。
(三)实验设计
(2)提出合理假设。
假设1:催化剂中铁元素全部为+3价;
假设2:催化剂中铁元素全部为+2价;
假设3:___ 。
(3)设计实验证明假设。请完成下表中的实验操作步骤,预期现象与结论。
(一)实验仪器与试剂
仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;
试剂:3mol·L-1H2SO4、6mol·L-1HNO3、0.01mol·L-1KMnO4、NaOH稀溶液、20%KSCN溶液、蒸馏水。
(二)实验原理
Fe2+能使酸性KMnO4溶液紫色褪去;Fe3+溶液中滴加KSCN溶液变红色。
(1)一位同学将少许样品溶于稀硝酸中,取少许溶液滴加KSCN溶液后出现红色。由此得出为铁元素为+3价的结论。该结论是否合理
(三)实验设计
(2)提出合理假设。
假设1:催化剂中铁元素全部为+3价;
假设2:催化剂中铁元素全部为+2价;
假设3:
(3)设计实验证明假设。请完成下表中的实验操作步骤,预期现象与结论。
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:用滴管取一定量3mol·L-1H2SO4于试管中,加热煮沸数分钟以出去溶于其中的氧气。 | 无明显现象 |
| 步骤2:用药匙取少量样品于试管中,用滴管加入除氧的3mol·L-1H2SO4,并加热,充分反应后得A溶液。 | 固体溶解,溶液颜色发生变化 |
| 步骤3:取少许A溶液于试管中滴加1~2滴20%KSCN溶液,振荡 | 若溶液不呈红色,则假设2成立;若溶液呈红色,则假设1或假设3成立 |
| 步骤4:另取少许A溶液于试管中, | 结合③,若 |
您最近一年使用:0次
【推荐1】某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5 (直径≤2.5μm的悬浮颗粒物,已知1μm=1×10-6 m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、 NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填 “属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为______ (填 “酸”或“碱”)性。
(3)煤燃烧排放的烟气含有SO2和NOx形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。_________
____ClO +_____NO+_______=____Cl-+_____
+_____NO+_______=____Cl-+_____ +________。
+________。
(4)洗涤含SO2的烟气,以下物质可作洗涤剂的是_______ (填字母)。
a.Ca(OH)2 b.CaCl2 c. Na2CO3 d. NaHSO3
(5)汽车燃油不完全燃烧时产生CO,目前在汽车尾气系统中装置催化转化器,可将CO和NO转化为两种无污染的气体,其化学反应方程式为__________________ 。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断待测试样为
(3)煤燃烧排放的烟气含有SO2和NOx形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
____ClO
 +_____NO+_______=____Cl-+_____
+_____NO+_______=____Cl-+_____ +________。
+________。(4)洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.CaCl2 c. Na2CO3 d. NaHSO3
(5)汽车燃油不完全燃烧时产生CO,目前在汽车尾气系统中装置催化转化器,可将CO和NO转化为两种无污染的气体,其化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】相同温度下,等物质的量浓度的NaX、NaY、NaZ三种正盐溶液,测得溶液的pH分别是7、9、10。则相对应的酸HX、HY、HZ的酸性强弱顺序为_______
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
(1)常温下,0.1mol/LCH3COONa溶液呈_________ (填“酸”、“碱”或“中”)性,溶液中c(Na+)______ c(CH3COO-)(填“>”、“<”或“=”);
(2)常温下,在浓度均为0.1mol/L的盐酸和NH4Cl溶液中,水的电离程度大小关系是:0.1mol/L盐酸______ 0.1mol/LNH4Cl溶液(填“>”、“<”或“=”);
(3)已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,生成沉淀量的关系是:m(AgCl)_______ m(AgBr)(填“>”、“<”或“=”)。
(1)常温下,0.1mol/LCH3COONa溶液呈
(2)常温下,在浓度均为0.1mol/L的盐酸和NH4Cl溶液中,水的电离程度大小关系是:0.1mol/L盐酸
(3)已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,生成沉淀量的关系是:m(AgCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】《化学与生活》
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为( ) 。
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是_______ ;可直接进入血液,补充能量的是______ ;应用最广泛的抗生素之一的是______ ;即可作为调味剂,又可作为防腐剂、着色剂的是______ ;食用过多会引起血压升高、肾脏受损的________ 。
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是( ) 。
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度__________ (填大、小)。
③_______ 腐蚀是造成钢铁腐蚀的主要原因,自行车的钢圈通常采用________ (填涂油漆或镀Cr)防腐蚀。
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①蛋白质是人体必需的营养物质,它在人体内最终分解为
A.葡萄糖 B.氨基酸 C.脂肪酸
②现有下列五种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是
A.酒精 B.蔗糖 C.甲醛
②一般情况下,合金比组成它的成分金属硬度
③
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用,请说明原因:__________ 。
(2)若电极材料选铜和石墨,电解质溶液选氯化铁溶液,外加导线,构成原电池。请写出正极电极方程式:______________ 。
(2)若电极材料选铜和石墨,电解质溶液选氯化铁溶液,外加导线,构成原电池。请写出正极电极方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)如图所示是 Zn 和Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是______ (填序号)。

实验后的记录:
① Cu 为负极,Zn 为正极
② Cu 极上有气泡产生,发生还原反应
③ SO 向Cu 极移动
向Cu 极移动
④若有 0.5mol 电子流经导线,则可产生 0.25mol 气体
⑤电子的流向是:Cu→Zn
⑥ 正极反应式:Cu-2e- =Cu2+,发生氧化反应
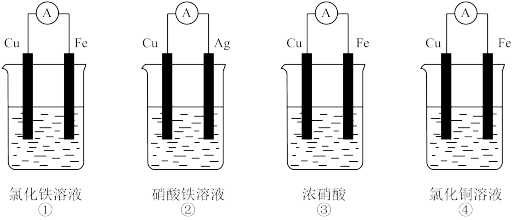
(2)为了验证 Fe3+与 Cu2+氧化性强弱,下列装置能达到实验目的是_____ (填序号)。
(3)图为青铜器在潮湿环境中因发生电化学反应而被腐蚀的原理示意图。

①腐蚀过程中,负极是____ (填图中字母“a”或“b”或“c”);
②环境中的 Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 Cu2(OH)3Cl,其离子方程式为____ ;

实验后的记录:
① Cu 为负极,Zn 为正极
② Cu 极上有气泡产生,发生还原反应
③ SO
 向Cu 极移动
向Cu 极移动④若有 0.5mol 电子流经导线,则可产生 0.25mol 气体
⑤电子的流向是:Cu→Zn
⑥ 正极反应式:Cu-2e- =Cu2+,发生氧化反应
(2)为了验证 Fe3+与 Cu2+氧化性强弱,下列装置能达到实验目的是

(3)图为青铜器在潮湿环境中因发生电化学反应而被腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的 Cl- 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 Cu2(OH)3Cl,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】N、P、As及其化合物在生产生活方面都有重要的用途。回答下列问题:
(1)As原子的基态核外电子排布式为___________ 。
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是___________ 。顺铂在水中溶解度较大,反铂在水中溶解度小,顺铂在水中溶解度较大的原因是___________ 。
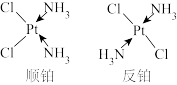
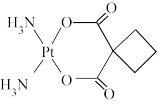
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为___________ 。
(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为___________ (用文字描述),该反应的化学方程式为___________ 。

(1)As原子的基态核外电子排布式为
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是
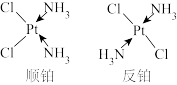
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为

(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据所学知识,回答下列问题:A、B、C代表三种元素,D是由A、B两种元素组成的物质。
(1)基态A原子核外只有一种运动状态的电子,基态B原子的最外层电子排布式为 ,则
,则
___________ 。
(2)C的单质在常温、常压下是气体,基态C原子的M层上有1个未成对的p电子,C的气态氢化物和氟化氢相比,稳定性较强的是___________ ,其原因是___________ ;沸点较高的是___________ ,其原因是___________ 。(填写化学式,并从微粒间作用力的角度分析原因)
(3)D是由短周期元素构成的中性四核粒子,有14个电子,分子中仅含共价键,其结构式为___________ ;D分子内所含 键与
键与 键的数目之比为
键的数目之比为___________ ; 键与
键与 键的强度大小关系为
键的强度大小关系为 键
键___________ (填“>”“<”或“=”) 键,原因是
键,原因是___________ 。
(4)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti),其基态原子价层电子轨道表示式为___________ 。
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价层电子排布式为 ,该元素的名称是
,该元素的名称是___________ 。
(1)基态A原子核外只有一种运动状态的电子,基态B原子的最外层电子排布式为
 ,则
,则
(2)C的单质在常温、常压下是气体,基态C原子的M层上有1个未成对的p电子,C的气态氢化物和氟化氢相比,稳定性较强的是
(3)D是由短周期元素构成的中性四核粒子,有14个电子,分子中仅含共价键,其结构式为
 键与
键与 键的数目之比为
键的数目之比为 键与
键与 键的强度大小关系为
键的强度大小关系为 键
键 键,原因是
键,原因是(4)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti),其基态原子价层电子轨道表示式为
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价层电子排布式为
 ,该元素的名称是
,该元素的名称是
您最近一年使用:0次



