相同温度下,等物质的量浓度的NaX、NaY、NaZ三种正盐溶液,测得溶液的pH分别是7、9、10。则相对应的酸HX、HY、HZ的酸性强弱顺序为_______
2022高二·全国·专题练习 查看更多[1]
(已下线)第20讲 盐类水解的影响因素及应用(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
更新时间:2022-10-28 17:46:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】自然界是各类物质相互依存、各种变化相互制约的复杂平衡体系,而水溶液中的离子平衡是其中一个重要方面。请根据所学知识,回答下列问题:
Ⅰ.电离平衡常数是衡量弱电解质电离程度的量,已知如表数据(25℃):
(1)0.1 mol/L的CH3COOK溶液和0.1 mol/LHCOONa溶液相比,c(K+)-c(CH3COO-)______________ c(Na+)-c(HCOO-) (填“<”、“=”或“>”)。
(2)25℃时,向NaA溶液中通入少量CO2,所发生反应的化学方程式为_____________ 。
(3)向0.1 mol/LHCOOH溶液中滴加相同浓度的NaOH溶液,当溶液中c(HCOOH):c(HCOO-)=5:9时,此时溶液的pH=______________ 。
Ⅱ.常温下,向20 mL某浓度的硫酸中滴入0.1 mol/L氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示:

请回答下列问题:
(4)a、b、c、d四个点水电离程度由大到小的顺序为______________ 。
(5)V=______________ mL,c点溶液中离子浓度由大到小顺序为______________ 。
(6)a、b、c、d四个点溶液显中性的是______________ 。
(7)NH3·H2O的电离常数K约为______________ 。
Ⅰ.电离平衡常数是衡量弱电解质电离程度的量,已知如表数据(25℃):
| 化学式 | CH3COOH | H2CO3 | HA | HClO | HCOOH |
| 电离常数 |  | 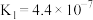  |  |  |  |
(2)25℃时,向NaA溶液中通入少量CO2,所发生反应的化学方程式为
(3)向0.1 mol/LHCOOH溶液中滴加相同浓度的NaOH溶液,当溶液中c(HCOOH):c(HCOO-)=5:9时,此时溶液的pH=
Ⅱ.常温下,向20 mL某浓度的硫酸中滴入0.1 mol/L氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示:

请回答下列问题:
(4)a、b、c、d四个点水电离程度由大到小的顺序为
(5)V=
(6)a、b、c、d四个点溶液显中性的是
(7)NH3·H2O的电离常数K约为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】25℃,几种物质的pH和浓度如下表所示。回答下列问题:
(1)c1____ (填“>”“<”或“=”)c2。
(2)溶液中水的电离程度②____ (填“>”“<”或“=”)③。
(3)分别加水稀释10倍,稀释后四种溶液的pH由大到小的顺序为____ (填序号)。
(4)①溶液与④溶液等体积混合,溶液的pH____ 7(填“>”“<“或“=”),用④溶液滴定①溶液,滴定过程中不可能出现的结果是____ 。
A. c(NH4+)>c(Cl-)>c(OH-)>c(H+)
B. c(NH4+)=c(Cl-)>c(OH-)=c(H+)
C. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D. c(Cl-)>c(NH4+)>c(H+)>c(OH-)
E. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(5)氢氧化铜悬浊液中有如下平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),常温下,Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液使之pH>
Cu2+(aq)+2OH-(aq),常温下,Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液使之pH>_____ 。
| 序号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| 浓度 | c1 | c2 | c3 | c4 |
(1)c1
(2)溶液中水的电离程度②
(3)分别加水稀释10倍,稀释后四种溶液的pH由大到小的顺序为
(4)①溶液与④溶液等体积混合,溶液的pH
A. c(NH4+)>c(Cl-)>c(OH-)>c(H+)
B. c(NH4+)=c(Cl-)>c(OH-)=c(H+)
C. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D. c(Cl-)>c(NH4+)>c(H+)>c(OH-)
E. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(5)氢氧化铜悬浊液中有如下平衡:Cu(OH)2(s)
 Cu2+(aq)+2OH-(aq),常温下,Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液使之pH>
Cu2+(aq)+2OH-(aq),常温下,Ksp=c(Cu2+)·c2(OH-)=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液使之pH>
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】常温下,现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作回答问题:
(1)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为: pH(甲)___________ pH(乙)(填“大于”、“小于”或“等于”)。
(2)各取25mL的甲、乙两溶液,分别用等浓度的 NaOH 稀溶液中和至 pH=7,则消耗的 NaOH 溶 液的体积大小关系为:V(甲)_____________ V(乙)(填“大于”、“小于”或“等于”)。
(3)pH=2的醋酸溶液中由水电离出的c(H+)________ 0.01mol/LHCl溶液中由水电离出的c(H+)。(填“>”、“<”、或“=”)
(1)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为: pH(甲)
(2)各取25mL的甲、乙两溶液,分别用等浓度的 NaOH 稀溶液中和至 pH=7,则消耗的 NaOH 溶 液的体积大小关系为:V(甲)
(3)pH=2的醋酸溶液中由水电离出的c(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,有浓度均为0.2mol·L-1的下列五种溶液,请回答问题。
①HCl ②NaCl ③CH3COOH ④CH3COONa ⑤Na2CO3
资料:室温下,醋酸Ka=1.7×10-5;碳酸Ka1=4.4×10-7,Ka2=4.7×10-11;次氯酸Ka=4.0×10–8
(1)上述溶液中水的电离被抑制的是________ (填序号,下同),水的电离被促进的是_______ ,用离子方程式表示促进水电离程度最大的溶质与水的作用:________ 。
(2)上述溶液的pH由大到小的顺序为___________ 。
(3)等体积的①和③分别于足量的锌粉反应,起始速率:①____ ③(填“<”、“=”或“>”);生成氢气的量:①____ ③(填“<”、“=”或“>”)。
(4)比较溶液③和④中CH3COO-的物质的量浓度:③____ ④(填“<”、“=”或“>”)。
(5)向溶液①中加水稀释至原体积的2倍,恢复至室温,所得溶液的pH为______ 。
(6)依据电离平衡常数数据,下列方程式书写合理的是______ 。(填字母)
a.CH3COONa溶液中滴加次氯酸:HClO+CH3COONa=CH3COOH+NaClO
b.Na2CO3溶液中滴加少量醋酸:CH3COOH+Na2CO3=NaHCO3+CH3COONa
c.NaClO溶液中通入CO2:CO2+H2O+2NaClO=Na2CO3+2HClO
d.NaHCO3溶液中滴加过量氯水:NaHCO3+Cl2=NaCl+HClO+CO2↑
(7)常温下0.1mol/LCH3COOH溶液加水稀释后,下列各项中数值变大的是______ 。
a.c(H+) b. c.c(H+)·c(OH−) d.
c.c(H+)·c(OH−) d.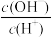 e.
e.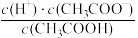
(8)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是
CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是_______ 。
a.加入少量0.10mol·L−1的稀盐酸 b.加热
c.加水稀释至0.010mol·L−1 d.加入少量冰醋酸
(9)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图所示。则HX的电离平衡常数______ (填“大于”、“等于”或“小于”下同)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)______ 醋酸溶液水电离出来c(H+)。

①HCl ②NaCl ③CH3COOH ④CH3COONa ⑤Na2CO3
资料:室温下,醋酸Ka=1.7×10-5;碳酸Ka1=4.4×10-7,Ka2=4.7×10-11;次氯酸Ka=4.0×10–8
(1)上述溶液中水的电离被抑制的是
(2)上述溶液的pH由大到小的顺序为
(3)等体积的①和③分别于足量的锌粉反应,起始速率:①
(4)比较溶液③和④中CH3COO-的物质的量浓度:③
(5)向溶液①中加水稀释至原体积的2倍,恢复至室温,所得溶液的pH为
(6)依据电离平衡常数数据,下列方程式书写合理的是
a.CH3COONa溶液中滴加次氯酸:HClO+CH3COONa=CH3COOH+NaClO
b.Na2CO3溶液中滴加少量醋酸:CH3COOH+Na2CO3=NaHCO3+CH3COONa
c.NaClO溶液中通入CO2:CO2+H2O+2NaClO=Na2CO3+2HClO
d.NaHCO3溶液中滴加过量氯水:NaHCO3+Cl2=NaCl+HClO+CO2↑
(7)常温下0.1mol/LCH3COOH溶液加水稀释后,下列各项中数值变大的是
a.c(H+) b.
 c.c(H+)·c(OH−) d.
c.c(H+)·c(OH−) d.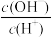 e.
e.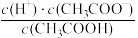
(8)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH
 CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是
CH3COO−+H+ ΔH>0,下列方法中,可以使0.10mol·L−1CH3COOH溶液中CH3COOH电离程度增大的是a.加入少量0.10mol·L−1的稀盐酸 b.加热
c.加水稀释至0.010mol·L−1 d.加入少量冰醋酸
(9)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图所示。则HX的电离平衡常数

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电离平衡常数是衡量弱电解质电离程度的量。已知如表数据(25℃):
(1)25℃,等浓度的三种溶液(a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液)的pH由大到小的顺序为_______ 。(填写序号)
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为______ 。
(3)现有浓度为0.02mol/L的HCN与0.01mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_____ 。
A.c(H+)>c(OH-) B.c(H+)<c(OH-)
C.c(H+)+c(HCN)=c(OH-) D.c(HCN)+c(CN-)=0.01mol/L
(4)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表
①从a组情况分析,HA是强酸还是弱酸______ 。
②b组情况表明,c____ 0.2(选填“大于”、“小于”或“等于”)。该混合液中离子浓度c(A-)_____ c(Na+)(选填“大于”、“小于”或“等于”)。
③a组实验所得混合溶液中由水电离出的c(OH-)=____ mol/L。写出该混合溶液中下列算式的精确结果。c(Na+)-c(A-)=____ mol/L。
(5)100℃时,水的离子积为1×10-12,将pH=11的NaOH溶液V1L与pH=2的H2SO4溶液V2L均匀混合后,若所得混合溶液的pH=10,则V1:V2为______
(6)HA为弱酸,在室温下,用蒸馏水稀释0.01mol/L HA溶液时,下列呈减小趋势的是_____ 。(填字母)
A. B.
B. C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值 E.水的电离程度
C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值 E.水的电离程度
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1)25℃,等浓度的三种溶液(a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液)的pH由大到小的顺序为
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为
(3)现有浓度为0.02mol/L的HCN与0.01mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是
A.c(H+)>c(OH-) B.c(H+)<c(OH-)
C.c(H+)+c(HCN)=c(OH-) D.c(HCN)+c(CN-)=0.01mol/L
(4)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表
| 实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 反应后溶液pH |
| a | 0.1 | 0.1 | pH=8 |
| b | c | 0.2 | pH=7 |
①从a组情况分析,HA是强酸还是弱酸
②b组情况表明,c
③a组实验所得混合溶液中由水电离出的c(OH-)=
(5)100℃时,水的离子积为1×10-12,将pH=11的NaOH溶液V1L与pH=2的H2SO4溶液V2L均匀混合后,若所得混合溶液的pH=10,则V1:V2为
(6)HA为弱酸,在室温下,用蒸馏水稀释0.01mol/L HA溶液时,下列呈减小趋势的是
A.
 B.
B. C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值 E.水的电离程度
C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值 E.水的电离程度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.常温下,如果取0.2 mol/LCH3COOH溶液与0.2 mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=9,试回答以下问题:
(1)混合溶液的pH=9的原因是:(用离子方程式表示)___________ 。
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比值为___________ 。
(3)求该混合溶液中下列算式的计算结果:
c(Na+)-c(CH3COO-)=___________ mol/L(代入数据,列出算式即可)
c(OH-)-c(CH3COOH)=___________ moL/L。
Ⅱ.(4)25℃下,向20 mL 0.1 mol•L-1 Na2CO3溶液中逐滴加入0.1 mol•L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴),随溶液pH变化的部分情况如图所示。回答下列问题:

①在同一溶液中,H2CO3、HCO 、CO
、CO
___________ (填“能”或“不能”)大量共存;
②当pH=7时,溶液中Na+、Cl-、HCO 三种离子的浓度大小关系为
三种离子的浓度大小关系为___________ ;
③已知在25℃时,CO 的第一步水解常数Kh1=2.0×10-4,当溶液中c(HCO
的第一步水解常数Kh1=2.0×10-4,当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,溶液的pH=
)=2∶1时,溶液的pH=___________ 。
(5)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是___________ (填字母序号)。
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3⑤NaHCO3⑥高锰酸钾
A.③④ B.①③④ C.①②③④⑤ D.全部
(1)混合溶液的pH=9的原因是:(用离子方程式表示)
(2)该混合溶液中由水电离出的c(H+)和pH=9的NaOH溶液中由水电离出c(H+)的比值为
(3)求该混合溶液中下列算式的计算结果:
c(Na+)-c(CH3COO-)=
c(OH-)-c(CH3COOH)=
Ⅱ.(4)25℃下,向20 mL 0.1 mol•L-1 Na2CO3溶液中逐滴加入0.1 mol•L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴),随溶液pH变化的部分情况如图所示。回答下列问题:

①在同一溶液中,H2CO3、HCO
 、CO
、CO
②当pH=7时,溶液中Na+、Cl-、HCO
 三种离子的浓度大小关系为
三种离子的浓度大小关系为③已知在25℃时,CO
 的第一步水解常数Kh1=2.0×10-4,当溶液中c(HCO
的第一步水解常数Kh1=2.0×10-4,当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,溶液的pH=
)=2∶1时,溶液的pH=(5)下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是
①胆矾 ②氯化铝 ③硫酸铝 ④Na2CO3⑤NaHCO3⑥高锰酸钾
A.③④ B.①③④ C.①②③④⑤ D.全部
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】磷酸是三元弱酸,常温下三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13,解答下列问题:常温下同浓度①Na3PO4、②Na2HPO4、③NaH2PO4的pH由小到大的顺序___________ (填序号);常温下,Na2HPO4的水溶液呈___________ (填“酸”“碱”或“中”)性,用Ka与Kh的相对大小,说明判断理由:___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为__________________ 。
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)__________ c(CH3COO-)(填“>”、“<”或“=”)。
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为___________ 。
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=___________ 。
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=
您最近一年使用:0次



