N、P、As及其化合物在生产生活方面都有重要的用途。回答下列问题:
(1)As原子的基态核外电子排布式为___________ 。
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是___________ 。顺铂在水中溶解度较大,反铂在水中溶解度小,顺铂在水中溶解度较大的原因是___________ 。
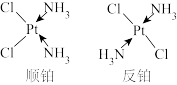
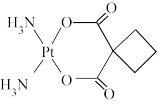
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为___________ 。
(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为___________ (用文字描述),该反应的化学方程式为___________ 。

(1)As原子的基态核外电子排布式为
(2)Pt(NH3)2Cl2有如图所示两种结构,Pt2+的配位体是
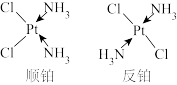
(3)碳铂是一种广谱抗癌药物,其结构如图。其分子中碳原子轨道杂化类型为

(4)PCl3和BCl3混合与H2在1000℃条件下可得到一种半导体材料,其晶胞结构如图所示。BCl3的空间构型为

更新时间:2022-03-31 18:45:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.有四种化合物W、X、Y、Z,它们是由短周期元素A、B、C、D、E中的两种元素组成。已知
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C 同周期;
(2)W由A、B组成,其分子中原子个数比为A:B=4:1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A:C=1:1
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1:1
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2:1 则B为__________ ,W为_________ ,X的结构式________ Y的电子式为______________ 。
II.(1).一元素原子的N层上只有1个电子,该元素原子各内层均已充满,写出该原子电子排布式:________________ ,
(2)一元素属于短周期元素,该元素的原子核外所有P轨道全满或者半满,写出该元素原子的价电子轨道排布图__________________ ,
(3)乙烯分子中有__________ 个σ键,___________ π键。
(1)A、B、C、D、E的原子序数依次增大,且A、D同主族,C、E同主族;B、C 同周期;
(2)W由A、B组成,其分子中原子个数比为A:B=4:1,常温为气态。
(3)X由A、C组成,其分子中原子数比为A:C=1:1
(4)Y是C、D形成的离子化合物,且Y晶体中相应元素的原子个数比为1:1
(5)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阳离子数与阴离子数之比为2:1 则B为
II.(1).一元素原子的N层上只有1个电子,该元素原子各内层均已充满,写出该原子电子排布式:
(2)一元素属于短周期元素,该元素的原子核外所有P轨道全满或者半满,写出该元素原子的价电子轨道排布图
(3)乙烯分子中有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是_____ 。与钛同周期的过渡元素中,基态原子的成对电子数与钛相同的有_____ 种。
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为_____ 。
(3)单晶衍射实验证实,配合物[Cr3O(CH3COO)6(H2O)3]Cl•8H2O的阳离子的结构如图甲所示:
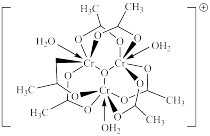
该配合物中中心离子的配位数是_____ ,铬元素的化合价为_____ 。
(4)某科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是_____ (填字母)。
(5)“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),写出该合金的化学式:_____ 。
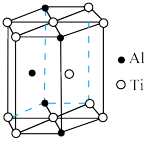
(1)金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为
(3)单晶衍射实验证实,配合物[Cr3O(CH3COO)6(H2O)3]Cl•8H2O的阳离子的结构如图甲所示:

该配合物中中心离子的配位数是
(4)某科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是
A. | B. | C.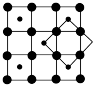 | D. |

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】小斌在复习选必二课本时发现了下面的物质,遗憾的是元素符号发生了错乱,只知道其中X,Y,Z,W为主族序数依次增大的前16号元素,Q为短周期元素,Y与W组成的一种化合物可作充气薄膜建材。试为他找出正确的说法_______ 。

A. 阳离子中含
阳离子中含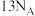 个
个 键
键
B. 元素和与
元素和与 同族的短周期元素
同族的短周期元素 可形成一种空间结构为三角锥型的极性分子
可形成一种空间结构为三角锥型的极性分子
C. 与
与 可形成一种常见的配体离子
可形成一种常见的配体离子
D.该物质熔点比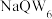 大
大
E.该物质常作为有机合成的溶剂

A.
 阳离子中含
阳离子中含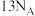 个
个 键
键B.
 元素和与
元素和与 同族的短周期元素
同族的短周期元素 可形成一种空间结构为三角锥型的极性分子
可形成一种空间结构为三角锥型的极性分子C.
 与
与 可形成一种常见的配体离子
可形成一种常见的配体离子D.该物质熔点比
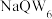 大
大E.该物质常作为有机合成的溶剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】sp3杂化与CH4分子的空间构型
(1)杂化轨道的形成
碳原子2s轨道上的1个电子进入2p空轨道,_______ 个2s轨道和_______ 个2p轨道“混合”,形成_______ 相等、_______ 相同的_______ 个sp3杂化轨道。
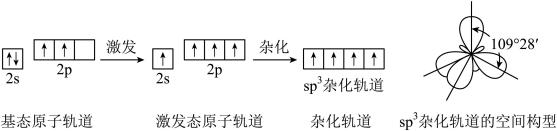
4个sp3杂化轨道在空间呈_______ ,轨道之间的夹角为_______ ,每个轨道上都有一个未成对电子。
(2)共价键的形成
碳原子的4个_______ 轨道分别与4个氢原子的_______ 轨道重叠,形成4个相同的_______ 键。

(3)CH4分子的空间构型
CH4分子为空间_______ 结构,分子中C—H键之间的夹角都是_______ 。
(4)正四面体结构的分子或离子的中心原子,一般采用sp3杂化轨道形成共价键,如CCl4、NH 等。金刚石中的碳原子、晶体硅和石英(SiO2)晶体中的硅原子也是采用
等。金刚石中的碳原子、晶体硅和石英(SiO2)晶体中的硅原子也是采用_______ 杂化轨道形成共价键的。
(1)杂化轨道的形成
碳原子2s轨道上的1个电子进入2p空轨道,

4个sp3杂化轨道在空间呈
(2)共价键的形成
碳原子的4个

(3)CH4分子的空间构型
CH4分子为空间
(4)正四面体结构的分子或离子的中心原子,一般采用sp3杂化轨道形成共价键,如CCl4、NH
 等。金刚石中的碳原子、晶体硅和石英(SiO2)晶体中的硅原子也是采用
等。金刚石中的碳原子、晶体硅和石英(SiO2)晶体中的硅原子也是采用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.有下列分子或离子:BF3、H2O、NH 、SO2、HCHO、PCl3、CO2
、SO2、HCHO、PCl3、CO2
(1)粒子构型为直线型的为:______
(2)粒子的立体构型为V型的为:______
(3)粒子的立体构型为平面三角形的为:______
(4)粒子的立体构型为三角锥型的为:______
(5)粒子的立体构型为正四面体的为______
II.在下列分子中,①H2,②CO2,③H2O2,④HCN(填序号)。分子中只有σ键的是______ ,分子中含有π键的是 ______ ,分子中所有原子都满足最外层为8个电子结构的是______ ,分子中含有由两个原子的s轨道重叠形成的σ键的是 ______ ,分子中含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是______ ,分子中既含有极性键又含有非极性键的是______ 。
 、SO2、HCHO、PCl3、CO2
、SO2、HCHO、PCl3、CO2(1)粒子构型为直线型的为:
(2)粒子的立体构型为V型的为:
(3)粒子的立体构型为平面三角形的为:
(4)粒子的立体构型为三角锥型的为:
(5)粒子的立体构型为正四面体的为
II.在下列分子中,①H2,②CO2,③H2O2,④HCN(填序号)。分子中只有σ键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1) 在水溶液中与
在水溶液中与 发生如下反应:
发生如下反应: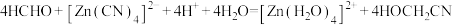 。
。
①在 中含有
中含有 键的数目为
键的数目为___________ 。
② 中
中 与
与 的C原子形成配位键。不考虑空间构型,
的C原子形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为___________ 。
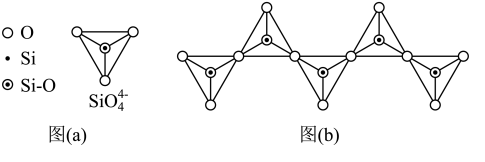
(2)在硅酸盐中, 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为___________ 。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为___________ ,微粒之间存在的作用力是___________ 。
(4)硫酸镍溶于氨水形成 蓝色溶液。在
蓝色溶液。在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为___________ ,提供孤电子对的成键原子是___________ 。
(5)氨的沸点___________ (填“高于”或“低于”)膦 ,原因是
,原因是___________ 。
(6)氮元素是植物生长所需的元素,常见氮肥有铵盐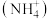 、尿素(
、尿素(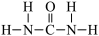 )等,
)等, 中
中 键角
键角___________ (填“>”“<”或“=”) 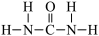 中
中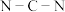 键角。
键角。
(7)硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用。硫单质有多种同素异形体,其中一种单质分子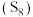 的结构为
的结构为 ,其熔点和沸点要比二氧化硫的高很多,主要原因为
,其熔点和沸点要比二氧化硫的高很多,主要原因为___________ 。
(8)在气体分析中,常用 的盐酸溶液吸收并定量测定
的盐酸溶液吸收并定量测定 的含量,其化学反应:
的含量,其化学反应: ;
; 是一种配合物,其结构如图所示:
是一种配合物,其结构如图所示:
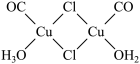
该配合物中, 作配体时配位原子是C而不是O的原因是
作配体时配位原子是C而不是O的原因是___________ 。
(1)
 在水溶液中与
在水溶液中与 发生如下反应:
发生如下反应: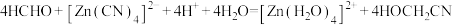 。
。①在
 中含有
中含有 键的数目为
键的数目为②
 中
中 与
与 的C原子形成配位键。不考虑空间构型,
的C原子形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为(2)在硅酸盐中,
 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(4)硫酸镍溶于氨水形成
 蓝色溶液。在
蓝色溶液。在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为(5)氨的沸点
 ,原因是
,原因是(6)氮元素是植物生长所需的元素,常见氮肥有铵盐
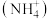 、尿素(
、尿素(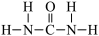 )等,
)等, 中
中 键角
键角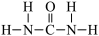 中
中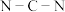 键角。
键角。(7)硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用。硫单质有多种同素异形体,其中一种单质分子
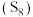 的结构为
的结构为 ,其熔点和沸点要比二氧化硫的高很多,主要原因为
,其熔点和沸点要比二氧化硫的高很多,主要原因为(8)在气体分析中,常用
 的盐酸溶液吸收并定量测定
的盐酸溶液吸收并定量测定 的含量,其化学反应:
的含量,其化学反应: ;
; 是一种配合物,其结构如图所示:
是一种配合物,其结构如图所示:
该配合物中,
 作配体时配位原子是C而不是O的原因是
作配体时配位原子是C而不是O的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________ 。
(2)NH3是一种很好的配体,NH3的沸点______ (填“>”“=”或“<”)AsH3。
(3)N原子核外有______ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为_____ 。
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为________ 。

(5)As 的卤化物的熔点如下:
表中卤化物熔点差异的原因是________________ 。
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_______ ,Fe3+的配位数为______ 。

(1)Fe2+的核外电子排布式为
(2)NH3是一种很好的配体,NH3的沸点
(3)N原子核外有
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为

(5)As 的卤化物的熔点如下:
| AsCl3 | AsBr3 | AsI3 | |
| 熔点/K | 256.8 | 304 | 413 |
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钛酸钙具有特殊的物理、化学性质,钛酸钙结构材料是当前材料科学研究领域的热点之一,回答下列问题。
(1)钛在元素周期表中的位置是_______ 。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的则用-
表示,与之相反的则用- 表示,称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为_______ 。从结构角度解释TiCl3中Ti还原性较强的原因_______ 。
(3)离子半径Ca2+>Ti4+,理由是_______ 。
(4)钛酸钙的晶胞如图所示,晶胞中Ca2+、Ti4+、O2-分别处于顶角、体心、面心位置。

①1个晶胞中含有O2-的个数是_______ ;钛酸钙的化学式是_______ 。
②晶体密度ρ可以用晶胞的质量除以体积来求算。已知钛酸钙晶胞的棱长为apm(1pm=1×10-10cm),则钛酸钙晶体密度ρ=_______ g•cm-3(列出计算式)。
(1)钛在元素周期表中的位置是
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的则用-
表示,与之相反的则用- 表示,称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为(3)离子半径Ca2+>Ti4+,理由是
(4)钛酸钙的晶胞如图所示,晶胞中Ca2+、Ti4+、O2-分别处于顶角、体心、面心位置。

①1个晶胞中含有O2-的个数是
②晶体密度ρ可以用晶胞的质量除以体积来求算。已知钛酸钙晶胞的棱长为apm(1pm=1×10-10cm),则钛酸钙晶体密度ρ=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某离子晶体晶胞的结构如图所示,X(●)位于立方体顶点,Y(○)位于立方体中心。试分析:
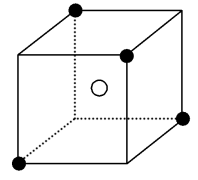
(1)晶体中距离最近的2个X与1个Y形成的夹角∠XYX是___________ 。
(2)设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X之间的距离为___________ cm。

(1)晶体中距离最近的2个X与1个Y形成的夹角∠XYX是
(2)设该晶体的摩尔质量为M g·mol-1,晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的X之间的距离为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:
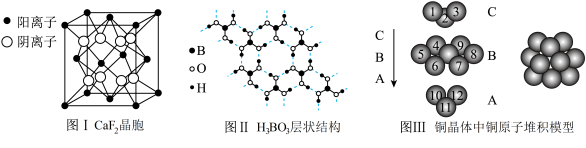
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为_______ ,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为_______ 。
(2)三种晶体中熔点最低的是________ ,其晶体受热熔化时,克服的微粒之间的相互作用为________ 。
(3)结合CaF2晶体的晶胞示意图,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为________ g·cm-3(精确到小数点后一位数,NA用具体数字代进去计算)。

(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为
(2)三种晶体中熔点最低的是
(3)结合CaF2晶体的晶胞示意图,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为
您最近一年使用:0次

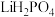 是制备锂电池的一种重要原料。
是制备锂电池的一种重要原料。 和
和

