某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5 (直径≤2.5μm的悬浮颗粒物,已知1μm=1×10-6 m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、 NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填 “属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为______ (填 “酸”或“碱”)性。
(3)煤燃烧排放的烟气含有SO2和NOx形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。_________
____ClO +_____NO+_______=____Cl-+_____
+_____NO+_______=____Cl-+_____ +________。
+________。
(4)洗涤含SO2的烟气,以下物质可作洗涤剂的是_______ (填字母)。
a.Ca(OH)2 b.CaCl2 c. Na2CO3 d. NaHSO3
(5)汽车燃油不完全燃烧时产生CO,目前在汽车尾气系统中装置催化转化器,可将CO和NO转化为两种无污染的气体,其化学反应方程式为__________________ 。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断待测试样为
(3)煤燃烧排放的烟气含有SO2和NOx形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
____ClO
 +_____NO+_______=____Cl-+_____
+_____NO+_______=____Cl-+_____ +________。
+________。(4)洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.CaCl2 c. Na2CO3 d. NaHSO3
(5)汽车燃油不完全燃烧时产生CO,目前在汽车尾气系统中装置催化转化器,可将CO和NO转化为两种无污染的气体,其化学反应方程式为
20-21高一上·浙江绍兴·阶段练习 查看更多[4]
(已下线)【浙江新东方】在线化学 (16)(已下线)【浙江新东方】在线化学34(已下线)2022年新高考化学时事热点情境化考题---化学与文化生活(已下线)第03讲 物质的组成、性质和分类(练)-2023年高考化学一轮复习讲练测(全国通用)
更新时间:2021-01-16 14:51:39
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求回答下列问题:
(1)现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
a. 以上物质中能导电的是________________________________ 。
b. 以上物质中属于电解质的是_______________________ ,属于非电解质的是_______________________ 。
c. 以上物质中,溶于水且能导电的物质是_______________________ 。
(2)胶体和溶液的本质区别是________________ ,鉴别胶体和溶液所采用的方法是观察是否能发生___________ 效应。
(3)下列3个反应,按要求填写相关量。
①2Na2O2+2H2O=4NaOH+ O2↑反应中,每消耗1 mol Na2O2生成_____ g O2。
②在NaHCO3的热分解反应中,每消耗168 g NaHCO3,标准状况下生成_____ L CO2。
③Cl2+H2O=HCl+HClO反应中,标准状况下每消耗22.4LCl2,转移_____ mol电子。
(4)在一个密闭容器中放入以下四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
①该变化的基本反应类型是_____ 反应;
②物质Q在反应中起的作用是_____ 。
(1)现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
a. 以上物质中能导电的是
b. 以上物质中属于电解质的是
c. 以上物质中,溶于水且能导电的物质是
(2)胶体和溶液的本质区别是
(3)下列3个反应,按要求填写相关量。
①2Na2O2+2H2O=4NaOH+ O2↑反应中,每消耗1 mol Na2O2生成
②在NaHCO3的热分解反应中,每消耗168 g NaHCO3,标准状况下生成
③Cl2+H2O=HCl+HClO反应中,标准状况下每消耗22.4LCl2,转移
(4)在一个密闭容器中放入以下四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
| 物质 | M | N | Q | P |
| 反应前质量(g) | 50 | 1 | 3 | 12 |
| 反应后质量(g) | x | 26 | 3 | 30 |
②物质Q在反应中起的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)胶体分散质粒子直径范围:___________ 。
(2)写出硫酸与氢氧化钡溶液反应的离子反应方程式:___________ 。
(3)写出盐酸与纯碱溶液反应的离子反应方程式:___________ ;
(4)写出碳酸钙与盐酸溶液反应的离子方程式:___________ ;
(5)写出Al2(SO4)3的电离方程式___________
(2)写出硫酸与氢氧化钡溶液反应的离子反应方程式:
(3)写出盐酸与纯碱溶液反应的离子反应方程式:
(4)写出碳酸钙与盐酸溶液反应的离子方程式:
(5)写出Al2(SO4)3的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下几种物质(或微粒):
①Cu丝;② ;③
;③ ;④液态HCl;⑤
;④液态HCl;⑤ 溶液;⑥熔融
溶液;⑥熔融 ;⑦冰醋酸;⑧饱和
;⑦冰醋酸;⑧饱和 溶液;⑨消毒酒精
溶液;⑨消毒酒精
回答下列问题:
(1)以上物质中属于分散系的是___________ 。(填代号)
(2)⑤中溶质熔融状态的电离方程式为___________ 。
(3)向⑤中逐滴加入 溶液至中性,其离子方程式为
溶液至中性,其离子方程式为___________ 。
(4)弱电解质 与KOH溶液反应生成的酸式盐只有一种,写出它与KOH反应生成正盐的离子方程式
与KOH溶液反应生成的酸式盐只有一种,写出它与KOH反应生成正盐的离子方程式___________ ;
(5)配平下列方程式___________ 。

①Cu丝;②
 ;③
;③ ;④液态HCl;⑤
;④液态HCl;⑤ 溶液;⑥熔融
溶液;⑥熔融 ;⑦冰醋酸;⑧饱和
;⑦冰醋酸;⑧饱和 溶液;⑨消毒酒精
溶液;⑨消毒酒精回答下列问题:
(1)以上物质中属于分散系的是
(2)⑤中溶质熔融状态的电离方程式为
(3)向⑤中逐滴加入
 溶液至中性,其离子方程式为
溶液至中性,其离子方程式为(4)弱电解质
 与KOH溶液反应生成的酸式盐只有一种,写出它与KOH反应生成正盐的离子方程式
与KOH溶液反应生成的酸式盐只有一种,写出它与KOH反应生成正盐的离子方程式(5)配平下列方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。下列反应可制得ClO2:NaClO3+ H2O2+ H2SO4→ClO2↑+Na2SO4+O2↑+H2O(未配平)
(1)反应中被氧化的元素是________ ,每生成2a个ClO2时有______ 个电子转移。
(2)写出配平后的方程式:___________ ,并用双线桥表示电子转移的方向和数目。
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:_____________________ 。
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(1)反应中被氧化的元素是
(2)写出配平后的方程式:
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将
 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐2】Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
您最近一年使用:0次
【推荐3】Ⅰ.已知下列反应:Fe + S = FeS;2Fe + 3Cl2 =2FeCl3;3Fe + 2O2 =Fe3O4。则S,Cl2,O2 的氧化性:______ >_____ >______
Ⅱ.实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平),此反应常温下就可以迅速进行。结合信息,回答下列问题:
(1)上述反应中被氧化的元素为______ ,还原产物是_______ 。
(2)Fe2+也能与MnO 反应生成Mn2+,反应后Fe2+转化为
反应生成Mn2+,反应后Fe2+转化为_____ 。反应中Fe2+表现_____ (填“氧化”或“还原”,下同)性,发生______ 反应。
(3)如果上述化学方程式中KMnO4和 MnCl2的化学计量数都是2,则HCl的化学计量数是___ 。
(4)实验室通常利用MnO2与浓盐酸共热反应制得氯气,据此可知KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为_______ 。
Ⅱ.实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平),此反应常温下就可以迅速进行。结合信息,回答下列问题:
(1)上述反应中被氧化的元素为
(2)Fe2+也能与MnO
 反应生成Mn2+,反应后Fe2+转化为
反应生成Mn2+,反应后Fe2+转化为(3)如果上述化学方程式中KMnO4和 MnCl2的化学计量数都是2,则HCl的化学计量数是
(4)实验室通常利用MnO2与浓盐酸共热反应制得氯气,据此可知KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮及其化合物与生产生活及环境息息相关。请回答下列问题:
(1) 在常温下性质很稳定,任意写出一种与此性质有关的用途:
在常温下性质很稳定,任意写出一种与此性质有关的用途:_______ 。
(2)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是_______ 。
A.酸雨 B.光化学烟雾 C.臭氧层空洞 D.白色污染 E.温室效应
②在含有a g 的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有
的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有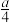 g
g  被还原,则
被还原,则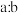 可能为
可能为_______ 。
A.2:1 B.3:1 C.4:1 D.9:2
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式_______ ,氧化产物与还原产物的物质的量之比为_______ 。
(4)氮的同族元素锑(Sb)可形成酸性超过100%硫酸的酸——氟锑酸( ),称为超强酸。氟锑酸可由
),称为超强酸。氟锑酸可由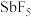 与HF混合得到。
与HF混合得到。
①制备氟锑酸一般在塑料容器中进行,不在玻璃仪器中进行的原因是_______ (用化学方程式回答)
②1966年,美国研究员J·Lukas无意中将蜡烛扔进 溶液中,发现蜡烛很快溶解,并放出
溶液中,发现蜡烛很快溶解,并放出 。已知碳正离子稳定性:
。已知碳正离子稳定性: ,写出等物质的量的异丁烷(
,写出等物质的量的异丁烷(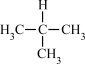 )与
)与 发生反应的化学方程式:
发生反应的化学方程式:_______ 。
(1)
 在常温下性质很稳定,任意写出一种与此性质有关的用途:
在常温下性质很稳定,任意写出一种与此性质有关的用途:(2)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是
A.酸雨 B.光化学烟雾 C.臭氧层空洞 D.白色污染 E.温室效应
②在含有a g
 的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有
的稀硝酸中,加入b g铁粉充分反应,铁全部溶解并生成NO,有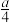 g
g  被还原,则
被还原,则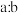 可能为
可能为A.2:1 B.3:1 C.4:1 D.9:2
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式
(4)氮的同族元素锑(Sb)可形成酸性超过100%硫酸的酸——氟锑酸(
 ),称为超强酸。氟锑酸可由
),称为超强酸。氟锑酸可由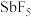 与HF混合得到。
与HF混合得到。①制备氟锑酸一般在塑料容器中进行,不在玻璃仪器中进行的原因是
②1966年,美国研究员J·Lukas无意中将蜡烛扔进
 溶液中,发现蜡烛很快溶解,并放出
溶液中,发现蜡烛很快溶解,并放出 。已知碳正离子稳定性:
。已知碳正离子稳定性: ,写出等物质的量的异丁烷(
,写出等物质的量的异丁烷( )与
)与 发生反应的化学方程式:
发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】判断正误:
1.硫在自然界中仅以化合态存在。(_______)
2.硫在空气中燃烧的产物是二氧化硫,在纯氧中燃烧的产物是三氧化硫。(_______)
3.硫黄易溶于CS2,所以可用CS2溶解试管内壁的硫。(_______)
4.残留在试管内壁上的硫可用CS2溶解除去,也可用热的NaOH溶液除去。(_______)
5.铜与硫化合的产物是CuS。(_______)
6.硫单质与变价金属反应时一般生成低价态的金属硫化物。(_______)
7.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。(_______)
8.单质硫或含硫物质燃烧时,氧气少量时生成SO2,氧气足量时生成SO3。(_______)
9.富含硫黄的矿物在工业上可用于制造硫酸。(_______)
10.改燃煤为燃气,可以减少废气中SO2等有害物质的排放量,是治理“雾霾”等灾害天气的一种措施。(_______)
11.向煤中加入适量石灰石,使煤燃烧产生的SO2最终生成CaSO3,可减少对大气的污染。(_______)
12.大量燃烧化石燃料排放的废气中含SO2,从而使雨水的pH<5.6形成酸雨。(_______)
13.硫和氮的氧化物是形成酸雨的主要物质。(_______)
1.硫在自然界中仅以化合态存在。(_______)
2.硫在空气中燃烧的产物是二氧化硫,在纯氧中燃烧的产物是三氧化硫。(_______)
3.硫黄易溶于CS2,所以可用CS2溶解试管内壁的硫。(_______)
4.残留在试管内壁上的硫可用CS2溶解除去,也可用热的NaOH溶液除去。(_______)
5.铜与硫化合的产物是CuS。(_______)
6.硫单质与变价金属反应时一般生成低价态的金属硫化物。(_______)
7.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。(_______)
8.单质硫或含硫物质燃烧时,氧气少量时生成SO2,氧气足量时生成SO3。(_______)
9.富含硫黄的矿物在工业上可用于制造硫酸。(_______)
10.改燃煤为燃气,可以减少废气中SO2等有害物质的排放量,是治理“雾霾”等灾害天气的一种措施。(_______)
11.向煤中加入适量石灰石,使煤燃烧产生的SO2最终生成CaSO3,可减少对大气的污染。(_______)
12.大量燃烧化石燃料排放的废气中含SO2,从而使雨水的pH<5.6形成酸雨。(_______)
13.硫和氮的氧化物是形成酸雨的主要物质。(_______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下图是依据一定的分类标准,对某些物质与水反应情况进行分类:
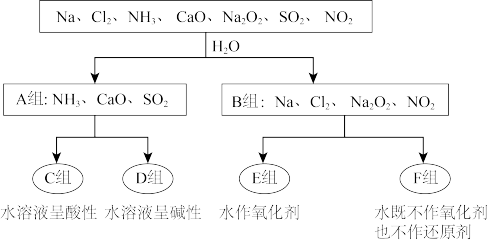
(1)根据物质与水反应的情况,这种分类方法叫_______ ,分成A、B组的分类依据是_______ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为_______ (填序号)。
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是_______ (填化学式),写出B组中红棕色气体与水反应的化学方程式_______ 。
(4)工业上常用D组中的_______ (填化学式)消除C组中物质对大气的污染。
(5)实验室用Al3+制备 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为_______
(6)C组中某一物质可使酸性 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因_______ 。
(7)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是_______ (填字母)。
a.碳氧化物 b.硫氧化物 c.氮氧化物

(1)根据物质与水反应的情况,这种分类方法叫
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是
(4)工业上常用D组中的
(5)实验室用Al3+制备
 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为(6)C组中某一物质可使酸性
 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因(7)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是
a.碳氧化物 b.硫氧化物 c.氮氧化物
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)碳酸钠溶液中各离子按照浓度从大到小的顺序依次为: __________________ 。
(2)下表是几种常见弱酸的电离平衡常数(25℃)
①根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是________ ;下列反应不能发生的是________ (填字母)。
a. CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
b. ClO-+CH3COOH=CH3COO-+HClO
c. CO32-+2HClO=CO2↑+H2O+2ClO-
d. 2ClO-+CO2+H2O=CO32-+2HClO
②25℃时, 等浓度的Na2CO3、CH3COONa 和NaClO三种溶液的pH从小到大依次是____________ 。
(3) 25℃时, Ksp[Mg(OH)2]=5.61×10-12, Ksp[MgF2]=7.42×10-11。 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,___________ (填化学式)溶液中的c(Mg2+)大。
(4)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中 c(CH3COO-)-c(Na+)=_________ mol·L-1(填计算式,不用求具体值)。
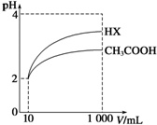
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。稀释后,HX溶液中水电离出来的c(H+)_____ (填“>”、“=”或“<”)醋酸溶液中水电离出来的c(H+);
(2)下表是几种常见弱酸的电离平衡常数(25℃)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
①根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是
a. CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
b. ClO-+CH3COOH=CH3COO-+HClO
c. CO32-+2HClO=CO2↑+H2O+2ClO-
d. 2ClO-+CO2+H2O=CO32-+2HClO
②25℃时, 等浓度的Na2CO3、CH3COONa 和NaClO三种溶液的pH从小到大依次是
(3) 25℃时, Ksp[Mg(OH)2]=5.61×10-12, Ksp[MgF2]=7.42×10-11。 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,
(4)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中 c(CH3COO-)-c(Na+)=
(5)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。稀释后,HX溶液中水电离出来的c(H+)

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空:
(1)FeCl3的水溶液 pH______ 7(填>、=、<),其原因为______________ (用离子方程式表示),将其溶液加热蒸干并灼烧最终得到物质是______ (填化学式)
(2)温度相同,浓度均为0.1mol•L-1的:①(NH4)2CO3,②(NH4)2Fe(SO4)2,③氨水,④NH4NO3,⑤NH4HSO4溶液,它们中的c(NH4+)由大到小的排列顺序是______________ 。 (用序号表示)
(3)常温下两种溶液:a.pH=4 NH4Cl b.pH=4盐酸溶液,其中水电离出c(H+)之比为_____________ 。
(4)室温,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸的体积比为____________ 。
(1)FeCl3的水溶液 pH
(2)温度相同,浓度均为0.1mol•L-1的:①(NH4)2CO3,②(NH4)2Fe(SO4)2,③氨水,④NH4NO3,⑤NH4HSO4溶液,它们中的c(NH4+)由大到小的排列顺序是
(3)常温下两种溶液:a.pH=4 NH4Cl b.pH=4盐酸溶液,其中水电离出c(H+)之比为
(4)室温,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
(1)常温下,0.1mol/LCH3COONa溶液呈_________ (填“酸”、“碱”或“中”)性,溶液中c(Na+)______ c(CH3COO-)(填“>”、“<”或“=”);
(2)常温下,在浓度均为0.1mol/L的盐酸和NH4Cl溶液中,水的电离程度大小关系是:0.1mol/L盐酸______ 0.1mol/LNH4Cl溶液(填“>”、“<”或“=”);
(3)已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,生成沉淀量的关系是:m(AgCl)_______ m(AgBr)(填“>”、“<”或“=”)。
(1)常温下,0.1mol/LCH3COONa溶液呈
(2)常温下,在浓度均为0.1mol/L的盐酸和NH4Cl溶液中,水的电离程度大小关系是:0.1mol/L盐酸
(3)已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,生成沉淀量的关系是:m(AgCl)
您最近一年使用:0次



