下图是依据一定的分类标准,对某些物质与水反应情况进行分类:
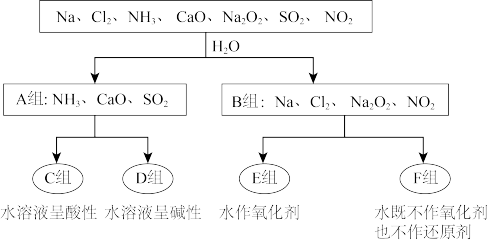
(1)根据物质与水反应的情况,这种分类方法叫_______ ,分成A、B组的分类依据是_______ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为_______ (填序号)。
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是_______ (填化学式),写出B组中红棕色气体与水反应的化学方程式_______ 。
(4)工业上常用D组中的_______ (填化学式)消除C组中物质对大气的污染。
(5)实验室用Al3+制备 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为_______
(6)C组中某一物质可使酸性 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因_______ 。
(7)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是_______ (填字母)。
a.碳氧化物 b.硫氧化物 c.氮氧化物

(1)根据物质与水反应的情况,这种分类方法叫
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是
(4)工业上常用D组中的
(5)实验室用Al3+制备
 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为(6)C组中某一物质可使酸性
 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因(7)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是
a.碳氧化物 b.硫氧化物 c.氮氧化物
更新时间:2022/12/02 09:13:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】I.对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替代的。如:纯净物根据其组成和性质可进行如图分类。
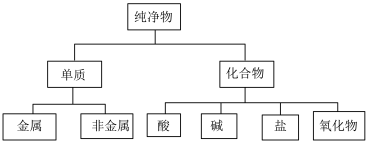
(1)如图所示的分类方法属于___________ 。
II.有下列物质是生活生产中常见的物质:① 晶体②液态
晶体②液态 ③冰醋酸(固态醋酸)④汞⑤
③冰醋酸(固态醋酸)④汞⑤ 固体⑥
固体⑥ 胶体⑦酒精
胶体⑦酒精 ⑧熔化
⑧熔化 ⑨盐酸⑩金属铜,请回答下列问题(用序号):
⑨盐酸⑩金属铜,请回答下列问题(用序号):
(2)以上物质中能导电的是___________ 。属于电解质的是___________ ;属于非电解质的是___________ 。
(3)以上物质中属于混合物的是___________ 。
(4)制备⑥的离子方程式为___________ 。
(5) 在水溶液中的电离方程式是
在水溶液中的电离方程式是___________ 。
(6)⑤的水溶液与⑨反应的化学方程式___________ 。

(1)如图所示的分类方法属于
II.有下列物质是生活生产中常见的物质:①
 晶体②液态
晶体②液态 ③冰醋酸(固态醋酸)④汞⑤
③冰醋酸(固态醋酸)④汞⑤ 固体⑥
固体⑥ 胶体⑦酒精
胶体⑦酒精 ⑧熔化
⑧熔化 ⑨盐酸⑩金属铜,请回答下列问题(用序号):
⑨盐酸⑩金属铜,请回答下列问题(用序号):(2)以上物质中能导电的是
(3)以上物质中属于混合物的是
(4)制备⑥的离子方程式为
(5)
 在水溶液中的电离方程式是
在水溶液中的电离方程式是(6)⑤的水溶液与⑨反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】分类在化学的学习中起着非常重要的作用,化学计量是化学定量研究的基础。
(1)下列分类标准合理的是___ (填序号)。
①仅根据物质在水溶液中能否导电,将物质分为电解质和非电解质
②根据反应中电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系中分散质粒子的大小,将分散系分为溶液、胶体和浊液
④根据是否有离子参加或生成,将水溶液中的反应分为离子反应和非离子反应
⑤根据碳酸钠溶于水形成的溶液呈碱性,将碳酸钠归为碱类
(2)现有以下物质:
①NaCl溶液,②二氧化碳,③H2SO4,④铜,⑤NaOH固体,⑥蔗糖,⑦硫酸钡,⑧水。其中,属于电解质的是:___ (填序号)。
(3)“纳米材料”是粒子直径为1nm~100nm的材料,纳米碳就是其中的一种。某研究所将纳米碳均匀的分散到蒸馏水中,得到的物质:①是溶液,②是胶体,③可观察到丁达尔效应,④静止后会出现黑色沉淀。上述说法中正确的是:____ (填序号)。
(4)等物质的量的CH4和H2,其分子个数比为___ ,质量比为___ ,氢原子的个数比为___ 。等质量的CH4和H2,其分子个数比为___ ,氢原子的个数比为___ ,标准状况下气体的体积比为___ 。
(5)5.4g水与___ g氨气所含氢原子数相同。
(1)下列分类标准合理的是
①仅根据物质在水溶液中能否导电,将物质分为电解质和非电解质
②根据反应中电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系中分散质粒子的大小,将分散系分为溶液、胶体和浊液
④根据是否有离子参加或生成,将水溶液中的反应分为离子反应和非离子反应
⑤根据碳酸钠溶于水形成的溶液呈碱性,将碳酸钠归为碱类
(2)现有以下物质:
①NaCl溶液,②二氧化碳,③H2SO4,④铜,⑤NaOH固体,⑥蔗糖,⑦硫酸钡,⑧水。其中,属于电解质的是:
(3)“纳米材料”是粒子直径为1nm~100nm的材料,纳米碳就是其中的一种。某研究所将纳米碳均匀的分散到蒸馏水中,得到的物质:①是溶液,②是胶体,③可观察到丁达尔效应,④静止后会出现黑色沉淀。上述说法中正确的是:
(4)等物质的量的CH4和H2,其分子个数比为
(5)5.4g水与
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,名不符实的一种物质是_________________ (填化学式);
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时):__________ ,____________ ;
(3)烧碱、纯碱溶液均可吸收CO2。向含有7.2 gNaOH的溶液中通入CO2,当通入的CO2与溶液中NaOH物质的量之比为7∶9时,则所得溶液中NaHCO3的质量为______ g。
(1)从物质的分类角度看,名不符实的一种物质是
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时):
(3)烧碱、纯碱溶液均可吸收CO2。向含有7.2 gNaOH的溶液中通入CO2,当通入的CO2与溶液中NaOH物质的量之比为7∶9时,则所得溶液中NaHCO3的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】2022年1月,南太平洋岛国汤加境内发生了“21世纪至今最剧烈的火山喷发”,对该国造成了严重的破坏。火山喷发过程部分化学反应如下:
①
②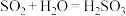
③
(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有_____ (填化学式),属于酸的有_____ (填化学式)。
(2)SO2与CO2具有某些相似的化学性质,写出用NaOH溶液吸收SO2的化学方程式:_____ 。
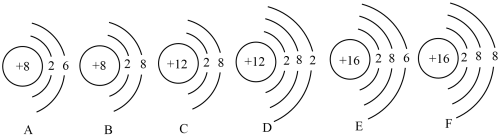
(3)下列粒子结构示意图中,表示原子的是_____ (填字母),表示阴离子的是_____ (填字母)。
(4)H2S是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。
①标况下3.36LH2S分子中含有_____ 个原子,其中S元素的质量为_____ 。
②将H2S气体通入石蕊试液中,试液由紫色变为_____ 色。
③Na2CO3称为正盐,NaHCO3称为酸式盐,写出H2S的一种酸式盐的化学式:_____ 。
①

②
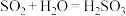
③

(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有
(2)SO2与CO2具有某些相似的化学性质,写出用NaOH溶液吸收SO2的化学方程式:
(3)下列粒子结构示意图中,表示原子的是

(4)H2S是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。
①标况下3.36LH2S分子中含有
②将H2S气体通入石蕊试液中,试液由紫色变为
③Na2CO3称为正盐,NaHCO3称为酸式盐,写出H2S的一种酸式盐的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有①酒精②石墨③Fe(OH)3胶体④醋酸⑤金刚石⑥熔融NaCl⑦稀硫酸七种物质,若根据物质的组成将它们进行分类,则:
(1)属于混合物的有___________
(2)属于能导电的电解质的有___________
(3)属于非电解质的有___________
(4)②和⑤的关系是___________
(5)制备③的离子方程式___________
(1)属于混合物的有
(2)属于能导电的电解质的有
(3)属于非电解质的有
(4)②和⑤的关系是
(5)制备③的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据酸碱的质子理论,“凡是能给出质子( )的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:①
)的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥HClO,⑦
,⑥HClO,⑦ ,⑧
,⑧ 。
。
(1)只属于酸的微粒是:_______ ;属于两性的微粒是:_______ 。(填标号)。
(2)写出⑤和⑥反应的离子方程式_______ 。
(3)经检测某工业废水显酸性,且废水中含有大量 、
、 和上述③、⑦、⑧离子。
和上述③、⑦、⑧离子。
a.下列离子中不可能大量存在该废水的是_______ (填标号)。
A. B.
B. C.
C. D.
D.
b.将该废水调节至碱性;废水中存在的离子产生的现象是_______ 。
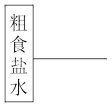
(4)用流程图表示除去粗盐水中 、
、 、
、 离子的方案设计。
离子的方案设计。
(可选用试剂有:稀盐酸、稀硫酸、 溶液、
溶液、 溶液、NaOH溶液。)
溶液、NaOH溶液。)
_______ 。
 )的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:①
)的分子或离子都是酸;凡是能结合质子的分子或离子都是碱。”按这个理论,下列微粒中:① ,②
,② ,③
,③ ,④
,④ ,⑤
,⑤ ,⑥HClO,⑦
,⑥HClO,⑦ ,⑧
,⑧ 。
。(1)只属于酸的微粒是:
(2)写出⑤和⑥反应的离子方程式
(3)经检测某工业废水显酸性,且废水中含有大量
 、
、 和上述③、⑦、⑧离子。
和上述③、⑦、⑧离子。a.下列离子中不可能大量存在该废水的是
A.
 B.
B. C.
C. D.
D.
b.将该废水调节至碱性;废水中存在的离子产生的现象是
(4)用流程图表示除去粗盐水中
 、
、 、
、 离子的方案设计。
离子的方案设计。(可选用试剂有:稀盐酸、稀硫酸、
 溶液、
溶液、 溶液、NaOH溶液。)
溶液、NaOH溶液。)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2是常见的大气污染物,燃煤是产生SO2的主要原因。工业上有多种方法可以减少SO2的排放。
(1)往煤中添加一些生石灰,可使燃煤过程中产生的SO2转化成硫酸钙。该反应的化学方程式为____ 。
(2)可用多种溶液做燃煤烟气中SO2的吸收液。
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO3时,两种吸收液体积比V(Na2SO3)∶V(NaOH)=____ 。
②NaOH溶液吸收了足量的SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式为____ 。
(3)甲同学认为BaCl2溶液可以做SO2的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀。
②____ 。
为证明SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
③试管B中试剂是溶液____ ;滴加浓硫酸之前的操作是____ 。
④通过甲乙两位同学的实验,得出的结论是____ 。
(1)往煤中添加一些生石灰,可使燃煤过程中产生的SO2转化成硫酸钙。该反应的化学方程式为
(2)可用多种溶液做燃煤烟气中SO2的吸收液。
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO3时,两种吸收液体积比V(Na2SO3)∶V(NaOH)=
②NaOH溶液吸收了足量的SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式为
(3)甲同学认为BaCl2溶液可以做SO2的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
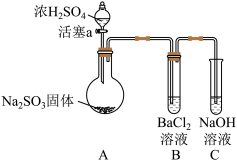
乙同学认为B中的白色沉淀是BaSO4,产生BaSO4的原因是
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀。
②
为证明SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
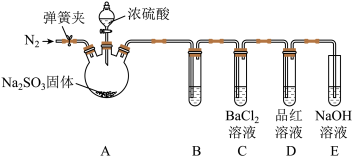
③试管B中试剂是溶液
④通过甲乙两位同学的实验,得出的结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与生活息息相关。请根据你所学知识回答下列问题。
(1)在葡萄酒酸制过程中添加适量二氧化硫不仅能杀菌,还能防止葡萄酒中的一些成分被氧化,起到保质的作用。这是利用了二氧化硫___________ 、能杀菌消毒和___________ 的性质。
(2)一些化工生产以及煤、石油的燃烧都可能生成二氧化硫,若任由其排放会造成大气污染,还可能形成___________ ,危害地面生物。在煤中加入适量生石灰可有效防止二氧化硫的排放,原因是___________ (用化学方程式表示)。某化学兴趣小组的同学收集到我市某电厂的尾气,将其___________ (填操作及现象),说明尾气中无二氧化硫。
(3)为早日实现“碳达峰、碳中和”的目标,我国大力发展光伏发电代替火力发电。光伏电池所用材料是___________ ;“碳达峰、碳中和”中的“碳”指的是___________ 。北京冬奥会亮相的氢燃料电动汽车是典型的绿色环保车,电池采用碱性电解质,工作时的负极反应方程式为___________ 。
(1)在葡萄酒酸制过程中添加适量二氧化硫不仅能杀菌,还能防止葡萄酒中的一些成分被氧化,起到保质的作用。这是利用了二氧化硫
(2)一些化工生产以及煤、石油的燃烧都可能生成二氧化硫,若任由其排放会造成大气污染,还可能形成
(3)为早日实现“碳达峰、碳中和”的目标,我国大力发展光伏发电代替火力发电。光伏电池所用材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知甲是短周期某主族元素的最简单氢化物,该物质有如下转化关系(反应条件部分省略)。
甲 乙
乙 丙
丙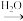 丁
丁
Ⅰ.若丙在常温常压为红棕色气体。
(1)写出实验室制取甲的化学方程式:__________ 。
(2)写出甲→乙的化学方程式:__________ 。
Ⅱ.若乙是具有刺激性气味的气体,丁为二元酸。某小组欲通过以下装置探究乙的部分性质。__________ 。
(4)试管A的作用为__________ 。
(5)若M是 溶液,试管B中观察到的现象为
溶液,试管B中观察到的现象为__________ ;为证明乙的氧化产物在溶液中的存在形式,某同学向试管B反应后的溶液中加入硝酸酸化的 溶液,判断是否出现白色沉淀。该做法
溶液,判断是否出现白色沉淀。该做法__________ (填“合理”或“不合理”),理由是__________ 。
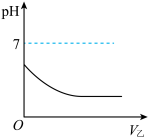
(6)将乙逐渐通入M溶液,测得溶液pH随通入乙气体体积的变化如图所示,则M溶液可能是__________ (填标号)。
甲
 乙
乙 丙
丙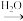 丁
丁Ⅰ.若丙在常温常压为红棕色气体。
(1)写出实验室制取甲的化学方程式:
(2)写出甲→乙的化学方程式:
Ⅱ.若乙是具有刺激性气味的气体,丁为二元酸。某小组欲通过以下装置探究乙的部分性质。
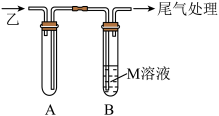
(4)试管A的作用为
(5)若M是
 溶液,试管B中观察到的现象为
溶液,试管B中观察到的现象为 溶液,判断是否出现白色沉淀。该做法
溶液,判断是否出现白色沉淀。该做法(6)将乙逐渐通入M溶液,测得溶液pH随通入乙气体体积的变化如图所示,则M溶液可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】贯彻落实习近平生态文明思想需要加强生态环境保护,中国科学院官方微信发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如图所示。
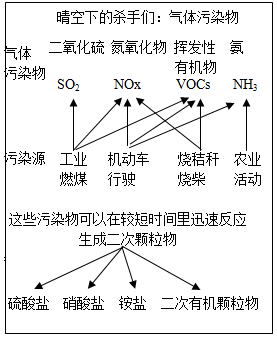
(1)根据如图信息可以看出,下列哪种气体污染物不是由机动车行驶造成的___ 。
a.SO2 b.NOx c.VOCs d.NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式___ 。
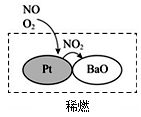
(3)在汽车的排气管上装一个催化转化装置是治理汽车尾气中NO和CO的一种方法,反应生成两种无污染的气体,方程式为___ 。
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:
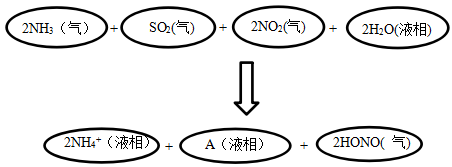
请判断A的化学式:____ 。
(5)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
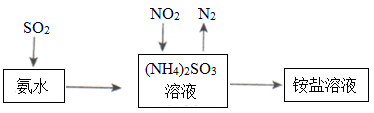
NO2被吸收过程的离子方程式是___ 。
(6)取某空气样本用蒸馏水处理制成待测液,其中所含的离子及其浓度如表:
根据表中数据计算:a=____ mol⋅L-1

(1)根据如图信息可以看出,下列哪种气体污染物不是由机动车行驶造成的
a.SO2 b.NOx c.VOCs d.NH3
(2)机动车大量行驶是污染源之一。汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式

(3)在汽车的排气管上装一个催化转化装置是治理汽车尾气中NO和CO的一种方法,反应生成两种无污染的气体,方程式为
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:

请判断A的化学式:
(5)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是
(6)取某空气样本用蒸馏水处理制成待测液,其中所含的离子及其浓度如表:
| 离子 | K+ | Na+ | NH | H+ | SO | NO | Cl- |
| 浓度/mol⋅L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据计算:a=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学对环境和人类生活都会带来影响。
(1)燃煤产生的二氧化硫在气溶胶表界面可被燃煤时产生的锰催化,快速生成硫酸盐加重空气中PM2.5污染。下列措施不能减少燃煤对大气造成污染的是_______ 。
①安装除尘脱氨脱硫设备 ②应用煤炭洗选加工技术 ③将煤炭气化转化为可燃性气体
④燃煤工厂烟囱加高 ⑤开发利用氢能、风能等清洁能源
(2)下列关于胶体的说法正确的是_______ (填标号)。
a.胶体与溶液的本质区别是丁达尔现象
b.按照分散剂的不同可将胶体分为液溶胶、气溶胶和固溶胶
c.已知土壤胶体中的胶粒带负电,施用含氮总量相同的 与
与 ,肥效相同
,肥效相同
(3)明胶是水溶性蛋白质混合物,溶于水可形成胶体。由工业明胶制成的胶囊往往含有超标的重金属铬( ),从而对人体造成伤害。已知
),从而对人体造成伤害。已知 是一种酸根离子,则
是一种酸根离子,则 属于
属于_______ (填“酸”“碱”“盐”或“氧化物”),含有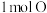 原子的
原子的 质量为
质量为_______  。
。
(4)将少量混有 的明胶胶体装入半透膜内浸入盛蒸馏水的烧杯中,证明
的明胶胶体装入半透膜内浸入盛蒸馏水的烧杯中,证明 能透过半透膜的实验操作是:取烧杯中的少量液体,向其中加入稀盐酸,再加入
能透过半透膜的实验操作是:取烧杯中的少量液体,向其中加入稀盐酸,再加入_______ ,若产生_______ ,则证明 能透过半透膜。
能透过半透膜。
(1)燃煤产生的二氧化硫在气溶胶表界面可被燃煤时产生的锰催化,快速生成硫酸盐加重空气中PM2.5污染。下列措施不能减少燃煤对大气造成污染的是
①安装除尘脱氨脱硫设备 ②应用煤炭洗选加工技术 ③将煤炭气化转化为可燃性气体
④燃煤工厂烟囱加高 ⑤开发利用氢能、风能等清洁能源
(2)下列关于胶体的说法正确的是
a.胶体与溶液的本质区别是丁达尔现象
b.按照分散剂的不同可将胶体分为液溶胶、气溶胶和固溶胶
c.已知土壤胶体中的胶粒带负电,施用含氮总量相同的
 与
与 ,肥效相同
,肥效相同(3)明胶是水溶性蛋白质混合物,溶于水可形成胶体。由工业明胶制成的胶囊往往含有超标的重金属铬(
 ),从而对人体造成伤害。已知
),从而对人体造成伤害。已知 是一种酸根离子,则
是一种酸根离子,则 属于
属于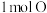 原子的
原子的 质量为
质量为 。
。(4)将少量混有
 的明胶胶体装入半透膜内浸入盛蒸馏水的烧杯中,证明
的明胶胶体装入半透膜内浸入盛蒸馏水的烧杯中,证明 能透过半透膜的实验操作是:取烧杯中的少量液体,向其中加入稀盐酸,再加入
能透过半透膜的实验操作是:取烧杯中的少量液体,向其中加入稀盐酸,再加入 能透过半透膜。
能透过半透膜。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】保持洁净安全的生存环境已成为全人类的共识。
(1)家庭装修所用的复合板材中常会放出对人体有严重危害的物质,这种有害物质主要是指________ (填名称)。
(2)天然水中含有的细小悬浮颗粒可以用明矾做进行净化处理,明矾水解得到的________ 可以吸附细小悬浮颗粒。
(3)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量.为控制大气中二氧化硫的排放,常采取的措施是在煤炭中加入石灰石粉末对化石燃料进行脱硫处理,其原理用方程式可表示为________ 。
(1)家庭装修所用的复合板材中常会放出对人体有严重危害的物质,这种有害物质主要是指
(2)天然水中含有的细小悬浮颗粒可以用明矾做进行净化处理,明矾水解得到的
(3)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量.为控制大气中二氧化硫的排放,常采取的措施是在煤炭中加入石灰石粉末对化石燃料进行脱硫处理,其原理用方程式可表示为
您最近一年使用:0次



