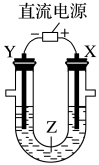
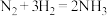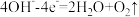利用下列装置(夹持装置略)进行实验,能达到实验目的的是
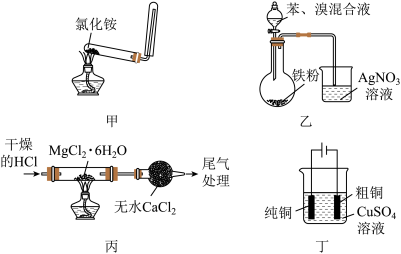

A.用甲装置制备并收集 |
| B.用乙装置制备溴苯并验证有HBr产生 |
C.用丙装置制备无水 |
| D.用丁装置进行铜的电解精炼 |
更新时间:2022-09-07 09:43:44
|
相似题推荐
【推荐1】碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,当外电路中通过0.04 mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
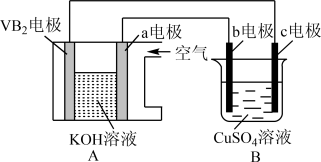

| A.VB2电极发生的电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,c电极表面先有红色物质析出,然后有气泡产生 |
| D.若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.2mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
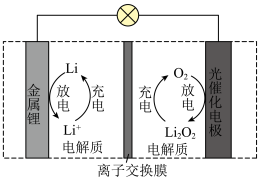
【推荐2】Li-O2电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电Li-O2电池,光照时,光催化电极产生电子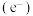 和空穴
和空穴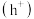 ,驱动某极反应(
,驱动某极反应( )和另一极反应
)和另一极反应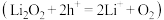 对电池进行充电。下列叙述
对电池进行充电。下列叙述不正确 的是
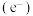 和空穴
和空穴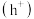 ,驱动某极反应(
,驱动某极反应( )和另一极反应
)和另一极反应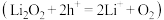 对电池进行充电。下列叙述
对电池进行充电。下列叙述
| A.电解质不可选择LiCl水溶液 |
B.放电时,正极发生反应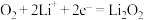 |
| C.充电时,每生成标准状况下22.4LO2,电路中转移4mol电子 |
D.放电时, 从左通过离子交换膜向右迁移 从左通过离子交换膜向右迁移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关四个常用电化学装置的叙述中,正确的是



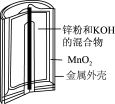 |  | 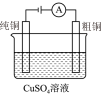 |  |
| 图Ⅰ碱性锌锰电池 | 图Ⅱ铅蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ氢氧燃料电池 |
| A.图Ⅰ所示电池中,MnO2是正极,电极反应式是2H2O+2e-=H2↑+2OH- |
| B.图Ⅱ所示电池放电过程中,当外电路通过1mol电子时,理论上负极板的质量增加96g |
| C.图Ⅲ所示装置工作过程中,阳极质量减少量等于阴极的质量增加量 |
| D.图Ⅳ所示电池中,不管KOH溶液换成H2SO4溶液还是Na2SO4溶液,电池的总反应式不变 |
您最近一年使用:0次
【推荐2】下列有关电化学装置完全正确的是
 | 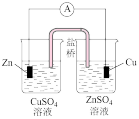 | 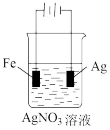 | 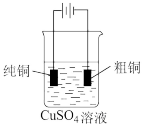 |
| A.防止Fe被腐蚀 | B.设计铜锌原电池 | C.铁上镀银 | D.铜的精炼 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 水溶液实现
水溶液实现