酸性锌锰干电池是一种常用的一次电池,其结构如图所示。该电池在放电过程产生MnOOH和Zn(NH3)2Cl2。回答下列问题:
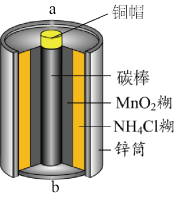
(1)该电池的正极为____ (填“a”或“b”)极,该电池总反应的化学方程式为____ 。
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。
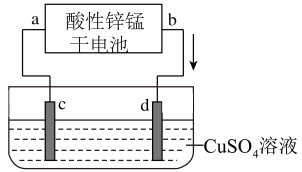
①电解一段时间后,石墨电极d出现的现象为____ ;石墨电极c上的电极反应式为____ 。
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为_____ (忽略电解前后溶液体积变化)。欲将电解后的溶液恢复至原溶液,应加入的试剂是____ ,其质量为____ g。

(1)该电池的正极为
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。

①电解一段时间后,石墨电极d出现的现象为
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为
更新时间:2022-09-06 12:51:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成问题
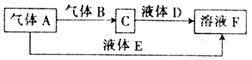
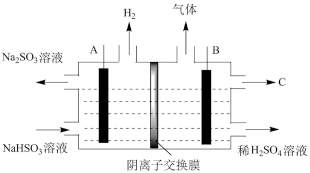
 通过如图所示电解装置可将
通过如图所示电解装置可将 转化为硫酸,电极材料皆为石墨。则A为电解池的
转化为硫酸,电极材料皆为石墨。则A为电解池的_________  填“阴极”或“阳极”
填“阴极”或“阳极” 。C为
。C为________  填物质名称
填物质名称 。若将阴离子交换膜换成阳离子交换膜,写出阳极区域发生的电极反应:
。若将阴离子交换膜换成阳离子交换膜,写出阳极区域发生的电极反应:_______ 。
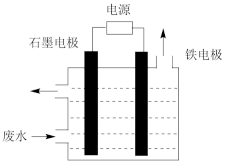
 用如图所示装置处理含
用如图所示装置处理含 废水时,控制溶液pH为
废水时,控制溶液pH为 并加入NaCl,一定条件下电解,阳极产生的
并加入NaCl,一定条件下电解,阳极产生的 将
将 氧化为无害物质而除去。铁电极为
氧化为无害物质而除去。铁电极为_________  填“阴极”或“阳极”
填“阴极”或“阳极” ,阳极产生
,阳极产生 的电极反应为
的电极反应为_______ ,阳极产生的 将
将 氧化为无害物质而除去的离子方程式为
氧化为无害物质而除去的离子方程式为______ 。
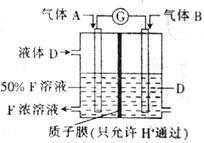
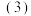 以连二亚硫酸根离子
以连二亚硫酸根离子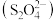 为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
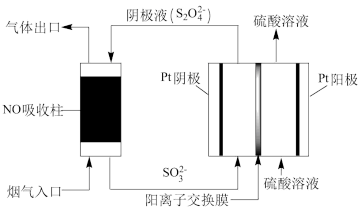
阴极区的电极反应式为__________ 。
 通过如图所示电解装置可将
通过如图所示电解装置可将 转化为硫酸,电极材料皆为石墨。则A为电解池的
转化为硫酸,电极材料皆为石墨。则A为电解池的 填“阴极”或“阳极”
填“阴极”或“阳极” 。C为
。C为 填物质名称
填物质名称 。若将阴离子交换膜换成阳离子交换膜,写出阳极区域发生的电极反应:
。若将阴离子交换膜换成阳离子交换膜,写出阳极区域发生的电极反应:
 用如图所示装置处理含
用如图所示装置处理含 废水时,控制溶液pH为
废水时,控制溶液pH为 并加入NaCl,一定条件下电解,阳极产生的
并加入NaCl,一定条件下电解,阳极产生的 将
将 氧化为无害物质而除去。铁电极为
氧化为无害物质而除去。铁电极为 填“阴极”或“阳极”
填“阴极”或“阳极” ,阳极产生
,阳极产生 的电极反应为
的电极反应为 将
将 氧化为无害物质而除去的离子方程式为
氧化为无害物质而除去的离子方程式为
 以连二亚硫酸根离子
以连二亚硫酸根离子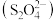 为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
阴极区的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某研究性学习小组将下列装置如图连接,a、b、c、d、g、h都是惰性电极。A中盛有100ml CuSO4溶液;B中盛有100g质量分数为16%的氢氧化钠溶液;将电源接通后,在g极附近显红色。
试回答下列问题:
(1)电源M极的名称是______ 。
(2)通电一段时间,取出电极,向A中加入4.9g Cu(OH)2,溶液与电解前相同,则电解时电路中通过的电子为_________ mol,原CuSO4溶液物质的量浓度为________ mol•L-1;
(3)B中d的电极反应式为________________________________________________ ,d极上产生的气体体积为____________ L(标况)。
(4)欲用C装置给铜镀银,f是__________ (填银或铜),电镀液是__________ 溶液。
(5)电解后将D中溶液倒入烧杯,稀释至200ml,此时溶液的pH=_______ 。

试回答下列问题:
(1)电源M极的名称是
(2)通电一段时间,取出电极,向A中加入4.9g Cu(OH)2,溶液与电解前相同,则电解时电路中通过的电子为
(3)B中d的电极反应式为
(4)欲用C装置给铜镀银,f是
(5)电解后将D中溶液倒入烧杯,稀释至200ml,此时溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
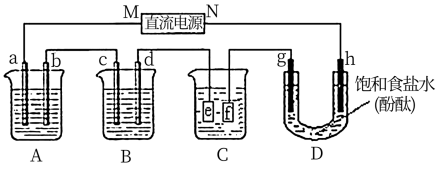
【推荐3】我国科学家设计了一种锂离子电池,并用此电池来电解含有Na2SO3的工业废水,可获得硫酸等物质,该过程示意图如图:
(1)锂离子电池工作时,a极发生_______ (填“氧化”或“还原”)反应, Li+移向_____ (填“a”或“b”)极, 写出b极的电极反应__________ 。
(2)电解池中物质A的化学式是_________ ,其中右侧交换膜的作用是______ ,写出 d极的电极反应___________ 。
(3)若电解池左侧溶液的体积为2 L,其浓度由2 mol/L变为4 mol/L时,理论上电路中通过的电子是____ mol。

(1)锂离子电池工作时,a极发生
(2)电解池中物质A的化学式是
(3)若电解池左侧溶液的体积为2 L,其浓度由2 mol/L变为4 mol/L时,理论上电路中通过的电子是
您最近一年使用:0次
填空题
|
适中
(0.65)
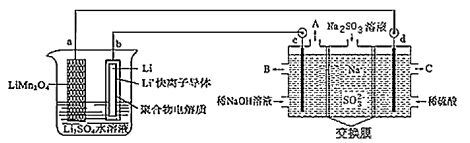
【推荐1】如图所示,四支电极均为铂电极,供选择的四组电解质溶液如下表:
要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;②b、c两极放电离子的物质的量相等。则:
(1)应选用的电解液是________ 组。
(2)甲槽的电解方程式为:_____________ ;乙槽的电解方程式为:_______________ 。
| 组 | A | B | C | D |
| 甲槽 | NaOH溶液 | AgNO3溶液 | H2SO4溶液 | NaCl溶液 |
| 乙槽 | CuSO4溶液 | CuCl2溶液 | AgNO3溶液 | AgNO3溶液 |

要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;②b、c两极放电离子的物质的量相等。则:
(1)应选用的电解液是
(2)甲槽的电解方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾( K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1是高铁电池的模拟实验装置:
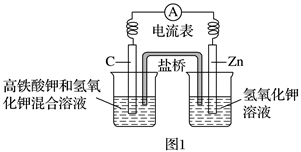
(1)该电池放电时正极的电极反应式为______________________________________ ;若维持电流强度为1 A,电池工作10 min,理论消耗Zn________ g(已知F=96 500 C·mol-1)。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向________ (填“左”或“右”,下同)池移动;若用阳离子交换膜代替盐桥,则钾离子向________ 移动。
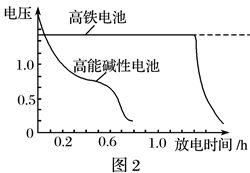
(3)图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有________________________________________________________________________ 。
Ⅱ.电解制取KIO3
电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH===5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为___________________________________ ;电解过程中阴极附近溶液pH________ (填“变大”、“变小”或“不变”)。

(1)该电池放电时正极的电极反应式为
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
(3)图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

Ⅱ.电解制取KIO3
电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH===5KI+KIO3+3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为
您最近一年使用:0次