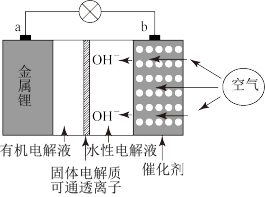
某学习小组用利用反应2Fe3++Cu=2Fe2++Cu2+设计原电池,装置如图所示。请回答下列问题。
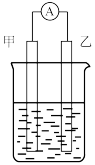
(1)实验过程中观察到电流表指针向右偏转(电流方向),则电极乙所用材料是____ ,电解质溶液是____ ,甲电极上发生的电极反应式是____ ,乙电极上发生的电极反应式是____ 。
(2)电池工作过程中,电解质溶液中的阳离子向____ 极移动(填“甲”或“乙”)。若电池反应过程共转移0.6mole-,则电解质溶液质量变化为____ 。
(3)电流表指针为0时,将乙电极换为铁电极,此时,乙电极为电池的____ 极(填“正”或“负”),电池总反应为____ 。

(1)实验过程中观察到电流表指针向右偏转(电流方向),则电极乙所用材料是
(2)电池工作过程中,电解质溶液中的阳离子向
(3)电流表指针为0时,将乙电极换为铁电极,此时,乙电极为电池的
更新时间:2022-09-10 13:23:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于___ (“离子化合物”或“共价化合物”)。
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为___________ 。
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从___________ (填“a”或“b”)通入,该电池的正极是___________ (填“M”或“N”)电极,其中在N极发生的电极反应式是___________ 。
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为___________ L。
(1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。
①甲硅烷(SiH4)属于
②已知室温下1 g甲硅烷自燃生成SiO2和液态水放出热量44.6 kJ,则甲硅烷自燃的热化学方程式为
(2)氢氧燃料电池的总反应为2H2+O2=2H2O,其工作原理如下图所示。

①图中H2从
②如果在外电路中有1 mol e-发生转移,则消耗标准状况下O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
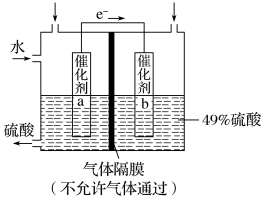
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识某同学自己动手设计了一个原电池。实验原理为:Fe+2H+=Fe2++H2,请填写下列空白
负材料可以用________ 其电极反应式为_________ 正极材料可以用_____________ 其电极反应式为______________
负材料可以用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,左侧石墨上通入 ,右侧石墨上通入
,右侧石墨上通入 ,电解质溶液为
,电解质溶液为 溶液。完成下列问题:
溶液。完成下列问题:
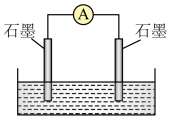
(1)负极反应式为_________ ;正极反应式为___________ ;电池总反应为________________ 。
(2)放电时 向
向_____ (填“正”或“负”)极移动。
(3)当外电路通过电子的物质的量为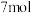 时,负极通入的
时,负极通入的 在标准状况下的体积为
在标准状况下的体积为_______ (假设能量全部转化为电能)。
 ,右侧石墨上通入
,右侧石墨上通入 ,电解质溶液为
,电解质溶液为 溶液。完成下列问题:
溶液。完成下列问题:
(1)负极反应式为
(2)放电时
 向
向(3)当外电路通过电子的物质的量为
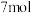 时,负极通入的
时,负极通入的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图1、图2。
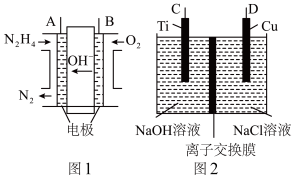
(1)①肼燃料电池中A极发生的电极反应为___________ 。
②上述装置中D电极应连接肼燃料电池的___________ 极(填“A”或“B”),该电解池的阳极反应式为___________ 。
③当反应生成14.4gCu2O时,停止电解,至少需要肼___________ mol,通过离子交换膜的阴离子的物质的量为___________ mol。(离子交换膜只允许OH-通过)
(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2也可制备纳米级Cu2O,同时放出N2,该反应的化学方程式为___________ 。
(3)发射火箭时以液态肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水。已知:①2H2O2(1)=2H2O(l)+O2(g) △H=-196kJmol-1;②H2O(l)=H2O(g) △H=43.98kJmol-1;③肼的燃烧热为-622.08kJmol-1。写出上述反应的热化学方程式___________ 。

(1)①肼燃料电池中A极发生的电极反应为
②上述装置中D电极应连接肼燃料电池的
③当反应生成14.4gCu2O时,停止电解,至少需要肼
(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2也可制备纳米级Cu2O,同时放出N2,该反应的化学方程式为
(3)发射火箭时以液态肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水。已知:①2H2O2(1)=2H2O(l)+O2(g) △H=-196kJmol-1;②H2O(l)=H2O(g) △H=43.98kJmol-1;③肼的燃烧热为-622.08kJmol-1。写出上述反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
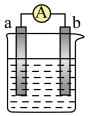
(1)若电极a为Zn,电极b为石墨
①当电解质溶液为稀硫酸时,该电池的负极的电极反应式为:_____ ;当反应中收集到标准状况下448mL气体时,电池中所转移的电子数目为_____ 。
②当电解质溶液为NaCl溶液时,该电池的正极的电极反应式为:_____ ;反应过程中,Na+移向_____ 电极(填字母“a”或“b”)。
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷(CH4)为燃料,采用氢氧化钠溶液为电解质溶液,则氧气应通入_____ 极(填“a”或“b”),另一电极的电极反应式_____ 。

(1)若电极a为Zn,电极b为石墨
①当电解质溶液为稀硫酸时,该电池的负极的电极反应式为:
②当电解质溶液为NaCl溶液时,该电池的正极的电极反应式为:
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷(CH4)为燃料,采用氢氧化钠溶液为电解质溶液,则氧气应通入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的有______ (填字母)。
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为_________ (只要求写一种)。
(3)有学者设想以下图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
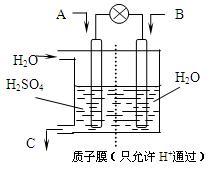
①若A为CO2,B为H2,C为CH3OH,则正极电极反应式为______________ 。
②若A为SO2,B为O2,C为H2SO4。科研人员希望每分钟从C处获得100mL10mol/LH2SO4,则A处通入烟气(SO2的体积分数为1%)的速率为_______ L/min(标准状况)。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的有
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为
(3)有学者设想以下图所示装置用电化学原理将CO2、SO2转化为重要化工原料。

①若A为CO2,B为H2,C为CH3OH,则正极电极反应式为
②若A为SO2,B为O2,C为H2SO4。科研人员希望每分钟从C处获得100mL10mol/LH2SO4,则A处通入烟气(SO2的体积分数为1%)的速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)高铁酸钾 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为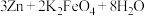
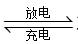
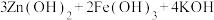 ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:

①该电池盐桥中盛有饱和 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向______ (填“左”或“右”)移动。
②该电池放电时正极的电极反应式为______ ;充电时每转移0.3mol电子,有______ mol 生成,正极附近溶液的碱性
生成,正极附近溶液的碱性______ (填“增强”,“不变”或“减弱”)。
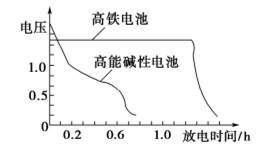
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_________________ 。
(2)“ ”电池可将
”电池可将 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为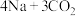

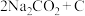 。放电时该电池“吸入”
。放电时该电池“吸入” ,其工作原理如图所示:
,其工作原理如图所示:
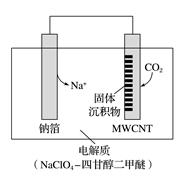
①充电时,正极的电极反应式为________________________________ 。
②放电时,若生成的 和
和 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol 时,两极的质量差为
时,两极的质量差为______ 。
 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为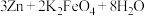

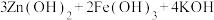 ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:
①该电池盐桥中盛有饱和
 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向②该电池放电时正极的电极反应式为
 生成,正极附近溶液的碱性
生成,正极附近溶液的碱性
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)“
 ”电池可将
”电池可将 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为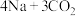

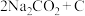 。放电时该电池“吸入”
。放电时该电池“吸入” ,其工作原理如图所示:
,其工作原理如图所示:
①充电时,正极的电极反应式为
②放电时,若生成的
 和
和 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol 时,两极的质量差为
时,两极的质量差为
您最近一年使用:0次