有四种常见药物①维生素C;②青霉素;③胃舒平;④麻黄碱。回答下列问题:
(1)某同学胃酸过多,应选用的药物是_______ (填序号)。抗酸药是治疗胃酸过多的一类药物,写出一种抗酸药与胃酸反应的化学方程式_______ 。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是_______ (填序号)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是_______ (填序号)。
(4)_______ (填序号)又称为抗坏血酸,它的分子式为_______ 。
(5)为预防缺铁性贫血,一些食品中加入了铁元素(含Fe2+物质)。若向铁强化牛奶中滴加KSCN溶液,发现牛奶变为红色,说明_______ ,此时若向其中加入一片维生素C,则发现红色消失,该实验说明维生素C具有_______ 性。
(1)某同学胃酸过多,应选用的药物是
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是
(4)
(5)为预防缺铁性贫血,一些食品中加入了铁元素(含Fe2+物质)。若向铁强化牛奶中滴加KSCN溶液,发现牛奶变为红色,说明
21-22高二上·甘肃甘南·期中 查看更多[3]
(已下线)第八章 化学与可持续发展【单元测试A卷】(已下线)第八章 化学与可持续发展(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)甘肃省甘南藏族自治州合作第一中学2021-2022学年高二上学期期中考试化学试题(文)
更新时间:2022-08-18 09:13:49
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】(1)用FeSO4·7H2O配制FeSO4溶液时,需加入稀H2SO4和________ 。
(2)在过量FeSO4溶液中滴入稀硫酸,再滴入几滴H2O2溶液,溶液立即变黄。上述反应的离子方程式为______________________________________ 。
(3)为检验上述反应中的氧化产物,甲同学取少许上述反应后的溶液,加入_____________ ,出现血红色溶液,证明氧化产物为Fe3+;乙同学取少许上述反应后的溶液,加入_________ 溶液,溶液变蓝,证明氧化产物为Fe3+,该反应的离子方程式为_________ 。
(4)为证明上述反应后的溶液中仍存在过量的Fe2+,可向其中滴加_________ 溶液。
(2)在过量FeSO4溶液中滴入稀硫酸,再滴入几滴H2O2溶液,溶液立即变黄。上述反应的离子方程式为
(3)为检验上述反应中的氧化产物,甲同学取少许上述反应后的溶液,加入
(4)为证明上述反应后的溶液中仍存在过量的Fe2+,可向其中滴加
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】含有下列离子的五种溶液①Ag+ ②Mg2+ ③Fe2+ ④Al3+ ⑤Fe3+试回答下列问题:
(1)既能被氧化又能被还原的离子是____________ (填离子符号,下同)
(2)向③中加入NaOH溶液并在空气中放置,现象是______ 有关化学方程式为__
(3)加入过量Na2O2溶液无沉淀的是_____________
(4)加铁粉溶液质量增重的是_________ ,溶液质量减轻的___________
(5)遇KSCN溶液呈红色的是_________________________
(6)能用来鉴别Cl–存在的离子是___________
(1)既能被氧化又能被还原的离子是
(2)向③中加入NaOH溶液并在空气中放置,现象是
(3)加入过量Na2O2溶液无沉淀的是
(4)加铁粉溶液质量增重的是
(5)遇KSCN溶液呈红色的是
(6)能用来鉴别Cl–存在的离子是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】1875年,虽然当时未受到门捷列夫预言的启发,法国化学家布瓦博德朗却发现了门捷列夫在他的第一张周期表上留下的空位中的元素“类铝”,并将其命名为镓,同时发表论文提出其密度为4.7g/cm3,门捷列夫在得知这一发现后指出镓和“类铝”是同一种物质,同时认为镓的密度应为5.9—6.0g/cm3,并写信建议布瓦博德重新测定镓的密度,布瓦博德没有固执己见,重新提纯了镓,最后测得的密度果然为5.94g/cm3。
(1)阅读上述材料,你得到什么启示?____ (至少答3条)
(2)已知镓与铝同主族,并位于第四周期,据此可推测氧化镓是一种_____ 氧化物(填“酸性”、“碱性”或“两性”)。
(1)阅读上述材料,你得到什么启示?
(2)已知镓与铝同主族,并位于第四周期,据此可推测氧化镓是一种
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】合成材料的应用与发展,大大方便了人类的生活,但由于合成材料废弃物的急剧增加带来了环境问题,废弃塑料带来的“白色污染”尤为严重。请你就怎样解决“白色污染”提出至少三条切实可行的措施。
(1)_________________________________ ;
(2)_________________________________ ;
(3)_________________________________ ;
(4)_________________________________ 。
(1)
(2)
(3)
(4)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)青奥会将于2014年8月在南京举行。青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念。
①用于青奥村工程的隔热保温材料聚氨酯属于______ (填字母)。
a.有机高分子材料 b.无机非金属材料 c.金属材料
②青奥中心外墙的复合保温材料采用铝合金锁边。有关铝合金的性质正确的是___ (填字母)。
a.强度小 b.耐腐蚀 c.密度大
③青奥会议中心双塔采用了玻璃幕墙设计。制造玻璃的主要原料为纯碱、石灰石和___ (填字母)。
a.金刚砂 b.石英 c.水玻璃
(2)如图为某品牌酱油标签的一部分。

①氨基酸态氮的含量是酱油质量的重要指标,这些氨基酸是由大豆中的主要营养物质_____ 水解而来的。
②配料清单中属于防腐剂的是______ 。
③小麦中的主要营养物质是_____ ,写出这种物质完全水解的化学方式:______ 。
(3)A、B、C三个城市全年雨水的月平均pH变化如图所示。
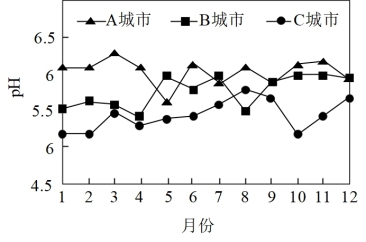
①受酸雨危害最严重的是____ 城市。
②导致硫酸型酸雨形成主要气体是___ ,减少燃煤过程产生该气体的措施有_________ 。
③汽车尾气中含有NO2、NO、CO等有害气体。写出由NO2形成硝酸型酸雨的化学方程式:______ ;汽车安装尾气净化装置可将NO、CO转化为无害气体,写出该反应的化学方程式:_______ 。
①用于青奥村工程的隔热保温材料聚氨酯属于
a.有机高分子材料 b.无机非金属材料 c.金属材料
②青奥中心外墙的复合保温材料采用铝合金锁边。有关铝合金的性质正确的是
a.强度小 b.耐腐蚀 c.密度大
③青奥会议中心双塔采用了玻璃幕墙设计。制造玻璃的主要原料为纯碱、石灰石和
a.金刚砂 b.石英 c.水玻璃
(2)如图为某品牌酱油标签的一部分。

①氨基酸态氮的含量是酱油质量的重要指标,这些氨基酸是由大豆中的主要营养物质
②配料清单中属于防腐剂的是
③小麦中的主要营养物质是
(3)A、B、C三个城市全年雨水的月平均pH变化如图所示。

①受酸雨危害最严重的是
②导致硫酸型酸雨形成主要气体是
③汽车尾气中含有NO2、NO、CO等有害气体。写出由NO2形成硝酸型酸雨的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】甲亢是现代社会一种常见的甲状腺疾病,它是甲状腺分泌甲状腺激素过多,容易机体代谢加快,交感神经兴奋,以暗器食欲增加但却消瘦。其中合成甲状腺激素中一种重要的卤素是___________ (填元素符号)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】合理选择饮食,正确使用药物,可以促进身心健康。
(1)现有下列七种物质:A.食盐 B.小苏打 C.维生素B D.葡萄糖 E.青霉素 F.阿司匹林 G.麻黄碱。请按下列要求填空(填序号)。
①食用过多会引起血压升高、肾脏受损的是_______ 。
②人体牙龈出血、患坏血病主要是缺乏_______ 。
③既可作为疏松剂,又可治疗胃酸过多的是_______ 。
④应用最广泛的抗生素之一的是_______ 。
⑤可直接进入血液,补充能量的是_______ 。
⑥可用作治疗支气管哮喘的药物是_______ 。
⑦可用作治感冒的药物是_______ 。
(2)复方氢氧化铝可治疗胃酸过多,氢氧化铝与胃酸( )反应的离子方程式为
)反应的离子方程式为_______ 。
(1)现有下列七种物质:A.食盐 B.小苏打 C.维生素B D.葡萄糖 E.青霉素 F.阿司匹林 G.麻黄碱。请按下列要求填空(填序号)。
①食用过多会引起血压升高、肾脏受损的是
②人体牙龈出血、患坏血病主要是缺乏
③既可作为疏松剂,又可治疗胃酸过多的是
④应用最广泛的抗生素之一的是
⑤可直接进入血液,补充能量的是
⑥可用作治疗支气管哮喘的药物是
⑦可用作治感冒的药物是
(2)复方氢氧化铝可治疗胃酸过多,氢氧化铝与胃酸(
 )反应的离子方程式为
)反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有四种常见药物①阿司匹林②青霉素③胃舒平④麻黄碱。请回答:
(1)某同学胃酸过多,应选用的药物是________ (填序号,下同);从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是________ ;滥用药物________ 会导致不良后果,如过量服用会出现水杨酸中毒,应立即停药,并静脉注射NaHCO3。
(2)人体中胃酸的主要成分是盐酸。胃酸可帮助消化食物,但胃酸过多会是人感到不适,服用适量的小苏打可使症状明显减轻。写出小苏打和盐酸反应的化学方程式:_________________________________ 。Mg(OH)2也是一种胃酸中和剂,写出Mg(OH)2中和胃酸的化学方程式:_______________ 。如果你是内科医生,给胃酸过多的胃溃疡病人(其症状之一是胃壁受损伤而变薄)开药方时,最好选用Mg(OH)2的理由是_____________________ 。
(1)某同学胃酸过多,应选用的药物是
(2)人体中胃酸的主要成分是盐酸。胃酸可帮助消化食物,但胃酸过多会是人感到不适,服用适量的小苏打可使症状明显减轻。写出小苏打和盐酸反应的化学方程式:
您最近一年使用:0次



