300 mL某溶液中可能含有Na+、NH 、Mg2+、Ba2+、CO
、Mg2+、Ba2+、CO 、SO
、SO 、Cl-中的若干种,现将此溶液分成三等份,进行如下实验:
、Cl-中的若干种,现将此溶液分成三等份,进行如下实验:
①向第一份中加入AgNO3溶液,有白色沉淀产生;
②向第二份中加足量KOH溶液并加热,收集到气体0.04 mol;
③向第三份中加足量BaCl2溶液,得到沉淀6.27 g,加入足量盐酸充分反应后,剩余沉淀2.33 g。根据上述实验,回答下列问题:
(1)实验③中生成沉淀的离子方程式为_______ 、_______ ,沉淀溶解的离子方程式为_______ 。
(2)溶液中一定不存在的离子有_______ 。
(3)实验①中加入AgNO3溶液,有沉淀产生,能否说明原溶液中含有Cl-?_______ (填“能”或否”)理由是:_______ 。
(4)用双线桥法表示电子转移的方向和数目:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O _______
 、Mg2+、Ba2+、CO
、Mg2+、Ba2+、CO 、SO
、SO 、Cl-中的若干种,现将此溶液分成三等份,进行如下实验:
、Cl-中的若干种,现将此溶液分成三等份,进行如下实验:①向第一份中加入AgNO3溶液,有白色沉淀产生;
②向第二份中加足量KOH溶液并加热,收集到气体0.04 mol;
③向第三份中加足量BaCl2溶液,得到沉淀6.27 g,加入足量盐酸充分反应后,剩余沉淀2.33 g。根据上述实验,回答下列问题:
(1)实验③中生成沉淀的离子方程式为
(2)溶液中一定不存在的离子有
(3)实验①中加入AgNO3溶液,有沉淀产生,能否说明原溶液中含有Cl-?
(4)用双线桥法表示电子转移的方向和数目:KClO3+6HCl(浓)
 KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O
更新时间:2022-09-13 16:02:11
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某强酸性溶液X含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验内容如图。
中的一种或几种,取该溶液进行连续实验,实验内容如图。
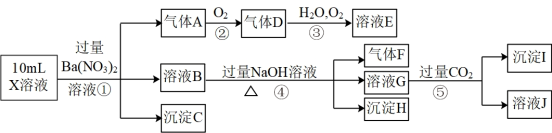
根据以上信息,回答下列问题:
(1)反应③的化学方程式为___________ 。
(2)沉淀C、H和气体F的化学式分别为__________ 。
(3)写出有关反应的离子方程式。
①中生成A:___________ 。
⑤:___________ 。
(4)上述离子中,溶液X中肯定不含有的离子是________ ,可能含有的离子是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种,取该溶液进行连续实验,实验内容如图。
中的一种或几种,取该溶液进行连续实验,实验内容如图。
根据以上信息,回答下列问题:
(1)反应③的化学方程式为
(2)沉淀C、H和气体F的化学式分别为
(3)写出有关反应的离子方程式。
①中生成A:
⑤:
(4)上述离子中,溶液X中肯定不含有的离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题:
I.对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘_______ ;
(2)除去食盐溶液中的水_______ ;
(3)淡化海水_______ ;
(4)KCl中含有KClO3_______ 。
II.某有色电解质溶液中,可能存在大量的Ag+、Fe3+、H+、 、OH-、Cl-。
、OH-、Cl-。
(5)你认为一定有的离子是_______ ,一定没有的离子是_______ ,还需进一步确认的离子是_______ ,请写出可行的实验方案_______ (包括操作、现象和结论)。
III.配平以下方程式。
(6)HClO3+P4+H2O→HCl+H3PO4,________________ 。
I.对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘
(2)除去食盐溶液中的水
(3)淡化海水
(4)KCl中含有KClO3
II.某有色电解质溶液中,可能存在大量的Ag+、Fe3+、H+、
 、OH-、Cl-。
、OH-、Cl-。(5)你认为一定有的离子是
III.配平以下方程式。
(6)HClO3+P4+H2O→HCl+H3PO4,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知某无色透明溶液中可能含有下列离子中的若干种:K+、Mg2+、Fe3+、Ba2+、 、OH-、
、OH-、 和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)
和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)
I.取少量原溶液,滴入紫色石蕊试液,溶液呈蓝色;
Ⅱ.取少量原溶液,滴入BaCl2溶液,无明显现象;
Ⅲ.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀产生;
Ⅳ.取少量原溶液,滴入少量稀H2SO4,有白色沉淀产生。
(1)某同学提出,不用实验即可判断原溶液中不存在的离子是_____ (填离子符号,下同)。
(2)由Ⅱ可以判断出原溶液中不存在的离子是_____ 。
(3)Ⅲ是为了判断_____ 离子的存在,先滴加足量稀硝酸的目的是_____ 。写出Ⅲ中发生反应的离子方程式_____ 。
(4)原溶液中一定含有的离子是_____ (填离子符号)。
(5)原溶液中可能含有的离子是_____ (填离子符号),为确认该离子的存在,可通过_____ (填实验名称)来检验。
 、OH-、
、OH-、 和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)
和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)I.取少量原溶液,滴入紫色石蕊试液,溶液呈蓝色;
Ⅱ.取少量原溶液,滴入BaCl2溶液,无明显现象;
Ⅲ.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀产生;
Ⅳ.取少量原溶液,滴入少量稀H2SO4,有白色沉淀产生。
(1)某同学提出,不用实验即可判断原溶液中不存在的离子是
(2)由Ⅱ可以判断出原溶液中不存在的离子是
(3)Ⅲ是为了判断
(4)原溶液中一定含有的离子是
(5)原溶液中可能含有的离子是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】粗盐中常含Ca2+、Mg2+、 以及泥沙等杂质,一种制备精盐的实验方案及步骤如下(用于沉淀的试剂饱和Na2CO3溶液、BaCl2溶液、NaOH溶液均稍过量):
以及泥沙等杂质,一种制备精盐的实验方案及步骤如下(用于沉淀的试剂饱和Na2CO3溶液、BaCl2溶液、NaOH溶液均稍过量):

(1)若试剂①选用NaOH溶液,则试剂②加入的主要目的是_____ 。判断滴加试剂③已过量的方法是:加入试剂③后,静置,在上层清液中,_______ 。
(2)操作I需要用到的玻璃仪器有烧杯、____ 。溶液丙中,溶质除NaCl外还含有_____ (填化学式)等。
(3)食用盐常在精盐中加入KIO3。为了检验实验中是否含KIO3,可以用以下反应进行:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。
①用双线桥分析以上反应中电子转移的方向和数目:_________ 。
②从反应后溶液中获得纯净的碘单质,可采用的实验操作方法的名称是_______ 。
 以及泥沙等杂质,一种制备精盐的实验方案及步骤如下(用于沉淀的试剂饱和Na2CO3溶液、BaCl2溶液、NaOH溶液均稍过量):
以及泥沙等杂质,一种制备精盐的实验方案及步骤如下(用于沉淀的试剂饱和Na2CO3溶液、BaCl2溶液、NaOH溶液均稍过量):
(1)若试剂①选用NaOH溶液,则试剂②加入的主要目的是
(2)操作I需要用到的玻璃仪器有烧杯、
(3)食用盐常在精盐中加入KIO3。为了检验实验中是否含KIO3,可以用以下反应进行:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。
①用双线桥分析以上反应中电子转移的方向和数目:
②从反应后溶液中获得纯净的碘单质,可采用的实验操作方法的名称是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】利用氯元素的价类二维图可以从不同角度研究含氯物质的性质及其转化关系。图中①~⑩均含氯元素。回答下列问题:

(1)④的化学式为__________ 。
(2)工业上常用 制备
制备 ,该反应的化学方程式为
,该反应的化学方程式为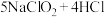 (稀)
(稀)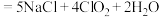 ,
,__________ (用双线桥标明电子转移方向和数目),氧化产物与还原产物物质的量之比为__________ 。
(3)比较⑥和⑦溶液的酸性强弱__________ (填可以或不可以)用pH试纸分别测定。

(1)④的化学式为
(2)工业上常用
 制备
制备 ,该反应的化学方程式为
,该反应的化学方程式为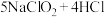 (稀)
(稀)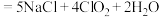 ,
,(3)比较⑥和⑦溶液的酸性强弱
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某课外活动小组利用下列装置迅速制备少量氯气。提供的试剂有:浓盐酸、饱和食盐水、氢氧化钠溶液、高锰酸钾固体。(2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O)
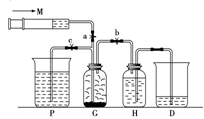
试回答:
(1)装置H中盛放的试剂是_________________________________________ 。
(2)尾气处理时关闭弹簧夹a和弹簧夹________________ ,打开弹簧夹________________ 。
(3)处理尾气时,发生反应的化学方程式是____________________________ 。
(4)从装置G中出来的Cl2中含有________________ 气体,可用________________ 试剂除去。
(5)标出该反应的电子转移方向和数目:2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O_______ ,此反应中的氧化剂是________ ,被氧化的元素是________ ,若参加反应的氧化剂的物质的量是1mol,则产生的氯气在标准状况下的体积为________ ,被氧化的物质的物质的量为________ (有单位的需注明单位)

试回答:
(1)装置H中盛放的试剂是
(2)尾气处理时关闭弹簧夹a和弹簧夹
(3)处理尾气时,发生反应的化学方程式是
(4)从装置G中出来的Cl2中含有
(5)标出该反应的电子转移方向和数目:2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O
您最近一年使用:0次



