在微观、宏观、符号之间建立联系是化学学科特有的特点。
图1是钾元素、硫元素在元素周期表中的信息,图2是一种微粒的结构示意图。
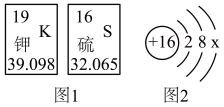
(1)钾元素的原子序数为_______ ,该元素属于_______ (填“金属元素”或“非金属元素”)
(2)硫元素的核内质子数为_______ ,其相对原子质量为_______ 。
a.若图2是硫原子的结构示意图,则x的值是_______ 。
b.若图2是硫离子的结构示意图,则x的值是_______ ,写出硫离子符号_______ 。
(3)写出由钾元素和硫元素组成的物质的化学式_______ 。
图1是钾元素、硫元素在元素周期表中的信息,图2是一种微粒的结构示意图。

(1)钾元素的原子序数为
(2)硫元素的核内质子数为
a.若图2是硫原子的结构示意图,则x的值是
b.若图2是硫离子的结构示意图,则x的值是
(3)写出由钾元素和硫元素组成的物质的化学式
更新时间:2022-09-15 17:11:37
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)三大化石燃料有__________ 、___________ 、___________ 。
(2)分别画出S、S2-、Al3+的结构示意图:___________ 、___________ 、___________ 。
(2)分别画出S、S2-、Al3+的结构示意图:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)现有①氯化氢②酒精③液氯④纯碱⑤熔融的氢氧化钠⑥水银⑦二氧化硫⑧一氧化碳⑨澄清石灰水等物质中,属于盐的是___________ (填序号,下同),属于酸性氧化物的是___________ ,能导电的是___________ ,属于电解质的是___________ 。
(2)有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的 ,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。
,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。
①写出甲、乙、丙、丁四种元素组成的化合物在水中的电离方程式_____ 。
②画出甲元素的离子结构示意图_____ 。
(1)现有①氯化氢②酒精③液氯④纯碱⑤熔融的氢氧化钠⑥水银⑦二氧化硫⑧一氧化碳⑨澄清石灰水等物质中,属于盐的是
(2)有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的
 ,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。
,乙元素原子核内无中子,丙元素原子核内有8个质子,丁元素原子最外层电子数是次外层电子数的2倍。①写出甲、乙、丙、丁四种元素组成的化合物在水中的电离方程式
②画出甲元素的离子结构示意图
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】元素周期表是化学学习和化学研究的重要工具。表为元素周期表的一部分,表中①~⑩分别代表一种元素。回答下列问题:
(1)上述元素中非金属性最强的是_______ (用元素符号表示);有一种元素的氧化物和氢氧化物都是两性化合物,画出该元素的原子结构示意图_______ ;地壳中含量最多的元素在周期表中的位置是_______ 。
(2)⑦、⑧、⑨元素的离子半径由大到小的顺序为_______ (用离子符号表示)。①与⑤形成的10电子离子为_______
(3)由①、⑥、⑩组成的一种化合物有强氧化性,具有杀菌漂白的能力,则该化合物的电子式为_______ 。
(4)由⑤、⑥两元素组成的气态化合物常见的有两种,其中有一种不能用排水法收集,试用化学方程式解释原因_______ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(1)上述元素中非金属性最强的是
(2)⑦、⑧、⑨元素的离子半径由大到小的顺序为
(3)由①、⑥、⑩组成的一种化合物有强氧化性,具有杀菌漂白的能力,则该化合物的电子式为
(4)由⑤、⑥两元素组成的气态化合物常见的有两种,其中有一种不能用排水法收集,试用化学方程式解释原因
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请利用原子结构的知识回答下列问题。
(1)预测:金属钠和金属铝哪一种更容易与氟气反应_______ ?为什么_______ ?
(2)元素的化合价与原子的电子层结构,特别是最外层电子数有关。请尝试概括核电荷数为1~20的元素的化合价与元素原子最外层电子数之间的关系_______ 。
(1)预测:金属钠和金属铝哪一种更容易与氟气反应
(2)元素的化合价与原子的电子层结构,特别是最外层电子数有关。请尝试概括核电荷数为1~20的元素的化合价与元素原子最外层电子数之间的关系
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某小组在研究前18号元素时发现:依据不同的标准和规律,元素周期表有不同的排列形式。如果将它们按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“●”代表一种元素,其中A代表氢元素。
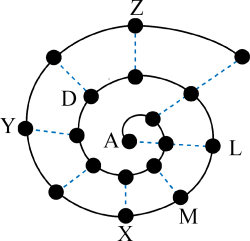
(1)X的元素符号为______ ,I元素在周期表中的位置为______ 。
(2)M与Z两种元素形成的化合物的化学式为______ 。
(3)下列说法正确的是______ (填序号)。
a.I元素形成的单质通入LZ的溶液中可得Z元素形成的单质
b.虚线相连的元素处于同一主族
c.L元素形成的单质在D元素形成的单质中燃烧生成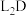
d.X、Y、M元素为同周期元素

(1)X的元素符号为
(2)M与Z两种元素形成的化合物的化学式为
(3)下列说法正确的是
a.I元素形成的单质通入LZ的溶液中可得Z元素形成的单质
b.虚线相连的元素处于同一主族
c.L元素形成的单质在D元素形成的单质中燃烧生成
d.X、Y、M元素为同周期元素
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~f6元素在周期表中的位置。
回答下列问题
(1)写出a单质的电子式________ 。
(2)画出b的原子结构示意图:__________ 。
(3)写出c单质和水反应的化学方程式:__________ 。
(4)金属性c强于d,请用原子结构理论解释原因______________
(5)已知硒(Se)与e同主族,且位于e的下一个周期,根据硒元素在元素周期表中的位置推测硒及其化合物可能具有的性质是______ 。
①最高价氧化物对应的水化物的化学式为H2SeO3
②SeO2既有氧化性又有还原性
③气态氢化物的稳定性比e元素的弱
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | a | b | ||||||
| 三 | c | d | e | f |
回答下列问题
(1)写出a单质的电子式
(2)画出b的原子结构示意图:
(3)写出c单质和水反应的化学方程式:
(4)金属性c强于d,请用原子结构理论解释原因
(5)已知硒(Se)与e同主族,且位于e的下一个周期,根据硒元素在元素周期表中的位置推测硒及其化合物可能具有的性质是
①最高价氧化物对应的水化物的化学式为H2SeO3
②SeO2既有氧化性又有还原性
③气态氢化物的稳定性比e元素的弱
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(8分)某简单微粒的结构示意图为: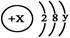 且X、Y 均为不大于20的正整数,据此回答下列问题:
且X、Y 均为不大于20的正整数,据此回答下列问题:
(1)若该微粒一般情况下不与其它元素的原子反应,这种微粒的符号是____________ ;
(2)若该微粒有很强的非金属性,且只需得到一个电子就能达到稳定结构,这种微粒的结构示意图为_______________ 。
(3)若该微粒为一价阳离子,且对应的碱为可溶性强碱,则x=_____ ,y=________ 。
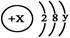 且X、Y 均为不大于20的正整数,据此回答下列问题:
且X、Y 均为不大于20的正整数,据此回答下列问题:(1)若该微粒一般情况下不与其它元素的原子反应,这种微粒的符号是
(2)若该微粒有很强的非金属性,且只需得到一个电子就能达到稳定结构,这种微粒的结构示意图为
(3)若该微粒为一价阳离子,且对应的碱为可溶性强碱,则x=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素X的最外层电子数是次外层电子数的2倍,该元素名称是________ ,画出它的原子结构示意图________ ,它的电子排布共有________ 个能层,________ 个能级。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】现有A、B、C、D、E五种元素,均为前四周期元素、它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)写出下列元素的元素符号:B:___________ C:___________ D:___________
(2)用元素符号表示A2B2的电子式为___________ 。
(3)E元素在元素周期表的位置为:___________ ,属于___________ 区,它有___________ 个能层。
(4)D原子核外电子排布式为___________ , 离子价层电子轨道表示式为
离子价层电子轨道表示式为___________ , 价层电子排布式的特点是
价层电子排布式的特点是___________ 。
(5)检验某溶液中是否含有 ,通常所用的试剂是
,通常所用的试剂是___________ 和___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C元素基态原子核外有17个不同运动状态的电子 |
| D元素位于元素周期表中的第八列,在地壳中的含量居前四位 |
| E元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)用元素符号表示A2B2的电子式为
(3)E元素在元素周期表的位置为:
(4)D原子核外电子排布式为
 离子价层电子轨道表示式为
离子价层电子轨道表示式为 价层电子排布式的特点是
价层电子排布式的特点是(5)检验某溶液中是否含有
 ,通常所用的试剂是
,通常所用的试剂是
您最近一年使用:0次

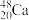 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了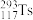 原子。已知
原子。已知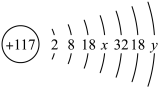 ,其中的x=
,其中的x= ”或“
”或“ ”)。
”)。

